科学探究题 适中0.65 引用1 组卷51
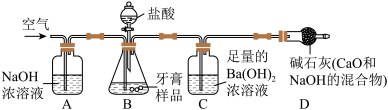
某化学兴趣小组同学为探究碳酸钠的化学性质,进行了如下实验:向盛有适量碳酸钠溶液的四支试管中分别加入下列试剂,实验现象记录如下:
试管4中发生复分解反应,该反应的化学方程式为_______ 。
化学兴趣小组的同学对反应后溶液中溶质的成分进一步探究:小组同学将试管3中的物质过滤,得到滤液A。
【提出问题】滤液A中溶质的成分是什么?
【猜想与假设】猜想一:NaOH;猜想二:NaOH和Na2CO3;猜想三:_______ ;猜想四:NaOH、Na2CO3和Ca(OH)2
【活动探究】
①小组讨论:有同学认为猜想四不成立,原因是_______ 。
②甲、乙两位同学分别用不同的方法进行实验:
 继续探究】
继续探究】
某公司生产出的纯碱经检测只含有氯化钠杂质。为测定该纯碱样品中碳酸钠的质量分数,称取26.5g该样品,加入到盛有一定质量稀盐酸的烧杯中,恰好完全反应。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)的关系如图所示。
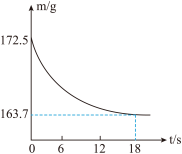
试分析并计算:
(1)生成CO2的质量为_______ g。
(2)该纯碱样品中Na2CO3的质量分数_____ 。(写出计算过程)
| 试管编号 | 1 | 2 | 3 | 4 |
| 加入试剂 | 无色酚酞试液 | 稀盐酸 | 澄清石灰水 | BaCl2溶液 |
| 实验现象 | 有气泡产生 | 有白色沉淀产生 | 有白色沉淀产生 |
化学兴趣小组的同学对反应后溶液中溶质的成分进一步探究:小组同学将试管3中的物质过滤,得到滤液A。
【提出问题】滤液A中溶质的成分是什么?
【猜想与假设】猜想一:NaOH;猜想二:NaOH和Na2CO3;猜想三:
【活动探究】
①小组讨论:有同学认为猜想四不成立,原因是
②甲、乙两位同学分别用不同的方法进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 甲:取少量滤液A于试管中,加 入过量的稀盐酸 | 有气泡生成 | 猜想 |
| 乙:取少量滤液A于试管中,加入适量的Ba(NO3)2溶液 |
 继续探究】
继续探究】某公司生产出的纯碱经检测只含有氯化钠杂质。为测定该纯碱样品中碳酸钠的质量分数,称取26.5g该样品,加入到盛有一定质量稀盐酸的烧杯中,恰好完全反应。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)的关系如图所示。

试分析并计算:
(1)生成CO2的质量为
(2)该纯碱样品中Na2CO3的质量分数
2022·江苏淮安·模拟预测
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网