科学探究题 适中0.65 引用1 组卷61
如图是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。
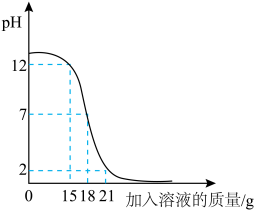
(1)根据图示判断,该实验是将_______ (填“氢氧化钠溶液”或“硫酸”)滴入到另一种溶液中;
(2)曲线上坐标为(18,7)的点表示的溶液中的离子有_______ (用化学用语表示)。
(3)小嘉发现氢氧化钠溶液与硫酸反应时有气泡产生,他认为氢氧化钠已经变质,写出氢氧化钠变质的化学方程式:_______ 。
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想与假设】小嘉对变质后的氢氧化钠溶液中的溶质作出两种猜想:
猜想一:只有碳酸钠 猜想二:_______ 。
【实验设计】为了验证上述猜想哪个正确,小嘉设计了如下方案:取少氢氧化钠溶液样品于试管中,滴入2-3滴无色酚酞试液,观察溶液颜色的变化就可以得出结论。小悦认为小嘉的实验方案不合理,理由是:_______ 。
【实验与结论】小悦另外设计实验方案并进行探究,请你帮助她完成下列实验报告:
【交流讨论】
1 写出步骤1发生反应的化学方程式:_______ ;
2 步骤1中加入的溶液能换成氢氧化钙溶液吗,请说出你的理由:_______ (只填理由)。

(1)根据图示判断,该实验是将
(2)曲线上坐标为(18,7)的点表示的溶液中的离子有
(3)小嘉发现氢氧化钠溶液与硫酸反应时有气泡产生,他认为氢氧化钠已经变质,写出氢氧化钠变质的化学方程式:
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想与假设】小嘉对变质后的氢氧化钠溶液中的溶质作出两种猜想:
猜想一:只有碳酸钠 猜想二:
【实验设计】为了验证上述猜想哪个正确,小嘉设计了如下方案:取少氢氧化钠溶液样品于试管中,滴入2-3滴无色酚酞试液,观察溶液颜色的变化就可以得出结论。小悦认为小嘉的实验方案不合理,理由是:
【实验与结论】小悦另外设计实验方案并进行探究,请你帮助她完成下列实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1、取少量氢氧化钠溶液样品于试管中,加入过量的 | 有白色沉淀产生 | 猜想 |
| 步骤2、 |
1 写出步骤1发生反应的化学方程式:
2 步骤1中加入的溶液能换成氢氧化钙溶液吗,请说出你的理由:
21-22九年级下·宁夏银川·期中
类题推荐
小明同学发现上周做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,小明邀约几个喜欢探究的同学对此进行了探究。请你完成下列实验报告。
(1)【提出问题1】该溶液变质了吗?
【猜想与假设】该溶液已经变质。
【实验探究1】
(2)【提出问题2】该溶液变质程度怎样?
【猜想与假设】猜想一:已完全变质,该溶液中溶质只含Na2CO3;
猜想二:部分变质,该溶液中溶质含有______ 。
(查阅资料:氯化钡溶液呈中性)
【实验探究2】
(3)【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体呢?
【实验探究3】为得到纯净的氢氧化钠固体,同学们取该样品并设计了如图实验方案。______ 。
②根据实验流程可知,最终所得氢氧化钠固体质量______ (选填“大于”“小于”或“等于”)变质后样品中氢氧化钠的质量。
(4)【反思与评价】在【实验探究2】中加入过量的氯化钡溶液的目的是______ 。
(1)【提出问题1】该溶液变质了吗?
【猜想与假设】该溶液已经变质。
【实验探究1】
| 实验步骤 | 实验现象 | 解释与结论 |
| 取少量该溶液放于试管中,滴加足量稀盐酸 | 有 | 说明该溶液已变质,变质的原因是 |
【猜想与假设】猜想一:已完全变质,该溶液中溶质只含Na2CO3;
猜想二:部分变质,该溶液中溶质含有
(查阅资料:氯化钡溶液呈中性)
【实验探究2】
| 实验步骤 | 实验现象 | 实验结论 |
| 先取少量该溶液放于试管中,加入过量氯化钡溶液 | 有 | 猜想二成立 |
| 静置,取上层清液于另一支试管中,加入2~3滴酚酞溶液 |
【实验探究3】为得到纯净的氢氧化钠固体,同学们取该样品并设计了如图实验方案。
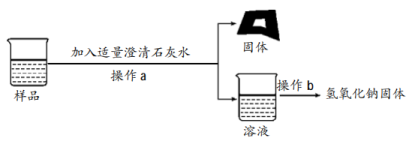
②根据实验流程可知,最终所得氢氧化钠固体质量
(4)【反思与评价】在【实验探究2】中加入过量的氯化钡溶液的目的是
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:

【提出问题】这瓶试剂可能是什么溶液呢?
【查阅资料】
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ.Na2CO3、NaHCO3溶液都呈碱性.
Ⅲ.室温(20℃)时,四种物质的溶解度的数据如下:
【得出结论】小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是_____________ 。
【作出猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl。
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,则猜想______ 错误。
(2)小强为了确定该溶液的成分,他又进行了如下实验:
老师指出该结论不严密。理由是氢氧化钠溶液在空气中敞口放置会发生变质,变质后也能产生上述现象。请写出氢氧化钠在空气中变质的化学方程式________________ 。
【继续探究】另取样加入过量的CaCl2溶液,观察到有________ 产生,设计这一步骤的目的是_________________ ;静置后,取上层清液,滴入无色酚酞试液,溶液呈红色。
【实验结论】这瓶溶液原来是____________________ 。
【探究启示】做实验时取完药品后应__________________ 。
(3)探究这瓶NaOH溶液的变质程度
【研究方案】取10g原溶液,向其中逐滴加入质量分数为7.3%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度。
【解决问题】实验测得加入稀盐酸与产生CO2气体的质量关系如下图所示。
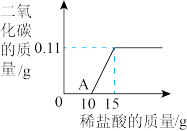
请回答:①A点溶液中所含的溶质_______________ (填化学式)。
②10g原溶液中含碳酸钠的质量__________________
③10g原溶液中未变质的氢氧化钠的质量______________ 。(不需要写出计算过程)

【提出问题】这瓶试剂可能是什么溶液呢?
【查阅资料】
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ.Na2CO3、NaHCO3溶液都呈碱性.
Ⅲ.室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
【作出猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl。
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,则猜想
(2)小强为了确定该溶液的成分,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加足量的 | 产生大量的气泡 | 猜想②正确 |
【继续探究】另取样加入过量的CaCl2溶液,观察到有
【实验结论】这瓶溶液原来是
【探究启示】做实验时取完药品后应
(3)探究这瓶NaOH溶液的变质程度
【研究方案】取10g原溶液,向其中逐滴加入质量分数为7.3%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度。
【解决问题】实验测得加入稀盐酸与产生CO2气体的质量关系如下图所示。
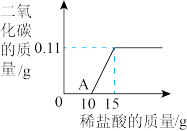
请回答:①A点溶液中所含的溶质
②10g原溶液中含碳酸钠的质量
③10g原溶液中未变质的氢氧化钠的质量
过氧化钠(Na2O2)可用作呼吸面具中的供氧剂,常用于航天或潜水等场合。实验室有一瓶放置较长时间的过氧化钠固体样品,某研究小组对其成分进行了如下探究。
【查阅资料】
①过氧化钠能与空气中的水反应生成氧气: 。
。
②过氧化钠能与空气中的二氧化碳反应: 。
。
③BaCl2溶液显中性。
【提出猜想】该固体中可能含有Na2O2、NaOH、Na2CO3中的一种或几种。
【分析交流】同学们一致认为步骤Ⅲ无法得出固体样品中含有NaOH的结论,理由是______ 。
【继续探究】为确定该固体样品中是否含有NaOH,同学们取3.0g样品,利用如图所示装置进行验证:
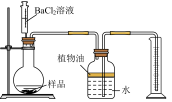
(1)装置中量筒收集到水的体积即为反应生成______ (填化学式)的体积。
(2)根据收集体积进行相关计算,得出样品中过氧化钠的质量为1.56g。
(3)将烧瓶内混合物过滤、洗涤、干燥后,称得最终所得固体质量为1.97g。
【实验结论】该固体的成分为______ 。
【反思提高】过氧化钠长时间露置在空气中会全部变质,最终转化为______ (填化学式)。
【查阅资料】
①过氧化钠能与空气中的水反应生成氧气:
②过氧化钠能与空气中的二氧化碳反应:
③BaCl2溶液显中性。
【提出猜想】该固体中可能含有Na2O2、NaOH、Na2CO3中的一种或几种。
实验步骤 | 实验现象 | 实验结论 |
I、取部分固体于试管中,加入适量水, 在试管口插入带火星的木条 | 固体中含有Na2O2 | |
II、取少量I中溶液于另一试管中,滴加 过量的BaCl2溶液 | 有白色沉淀生成 | 固体中含有 |
Ⅲ、取步骤II中的上层清液于另一支试 管中,滴入1~2滴无色酚酞溶液 | 溶液变为红色 | 固体中含有NaOH |
【继续探究】为确定该固体样品中是否含有NaOH,同学们取3.0g样品,利用如图所示装置进行验证:

(1)装置中量筒收集到水的体积即为反应生成
(2)根据收集体积进行相关计算,得出样品中过氧化钠的质量为1.56g。
(3)将烧瓶内混合物过滤、洗涤、干燥后,称得最终所得固体质量为1.97g。
【实验结论】该固体的成分为
【反思提高】过氧化钠长时间露置在空气中会全部变质,最终转化为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


