科学探究题 较难0.4 引用4 组卷201
小明和小东同学学习了酸、碱、盐的知识后,在老师的带领下来到化学实验室进行了如下实验活动。
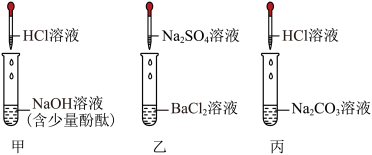
【实验活动一】两位同学按下图所示进行实验。小明同学观察到甲试管中开始无明显现象,一段时间后溶液变成______ 色:乙试管中发生反应的化学方程式为______ 。
【实验活动二】两位同学将试管中所有废液倒入废物缸中,为科学处理实验后的废渣、废液,小东同学决定先弄清其中成分,于是进行了如下实验,请帮助完成表格中相关内容。
【结论】通过上述实验得知,滤液的成分是______ (填化学式)。
【实验活动一】两位同学按下图所示进行实验。小明同学观察到甲试管中开始无明显现象,一段时间后溶液变成

【实验活动二】两位同学将试管中所有废液倒入废物缸中,为科学处理实验后的废渣、废液,小东同学决定先弄清其中成分,于是进行了如下实验,请帮助完成表格中相关内容。
| 实验步骤 | 实验现象 | 实验结论 |
| 1、将废物缸中混合物进行过滤 | 得到白色滤渣和无色滤液 | 滤渣中含有 |
| 2、取少量滤渣于试管中,加入足量的稀盐酸 | 沉淀部分溶解,有无色气泡产生 | |
| 3、另取少量无色滤液于试管中,滴加适量 | 滤液中一定含有BaCl2(酚酞除外) |
2022·山东青岛·二模
类题推荐
为探究金属活动性,某化学兴趣小组将锌和铜分别放入稀硫酸中,铜不反应而锌的表面有气泡产生。老师告诉学生,铜和稀硫酸在加热条件下也不会反应,但铜和浓硫酸在加热的条件下也能反应生成硫酸铜、水和一种气体。
【提出问题】铜与浓硫酸反应的生成物中产生的气体是什么?
【猜想假设】同学们对产生的气体作出了如下猜想:
猜想一:H2
猜想二:SO2
猜想三:SO3
【查阅资料】
a.二氧化硫能使品红溶液褪色,也能和碱性溶液发生反应。
b.在化学反应中,若有元素化合价升高,则一定有元素化合价降低。某同学根据资料判断,猜想不成立
【实验探究】师生共同设计了如下装置进行实验(部分仪器已略去)。请完成下列表格。

【实验总结】写出铜与浓硫酸反应的化学方程式 ___________ 。
【反思与拓展】(异常现象分析)随着实验的进行,装置A中气泡产生的速率由快到慢最后不再产生,请对这一现象进行解释:___________ 。
【提出问题】铜与浓硫酸反应的生成物中产生的气体是什么?
【猜想假设】同学们对产生的气体作出了如下猜想:
猜想一:H2
猜想二:SO2
猜想三:SO3
【查阅资料】
a.二氧化硫能使品红溶液褪色,也能和碱性溶液发生反应。
b.在化学反应中,若有元素化合价升高,则一定有元素化合价降低。某同学根据资料判断,猜想不成立
【实验探究】师生共同设计了如下装置进行实验(部分仪器已略去)。请完成下列表格。

| 实验步骤 | 实验现象 | 解释或结论 |
| ①点燃一段时间装置A处的酒精灯 | 装置A中的液体变为 | 反应有CuSO4生成 |
| 装置B处品红溶液褪色 | 反应有 | |
| ②点燃装置E处的酒精灯 | 装置E中 | 反应没有H2生成 |
【反思与拓展】(异常现象分析)随着实验的进行,装置A中气泡产生的速率由快到慢最后不再产生,请对这一现象进行解释:
给试管里稀盐酸和带锈铁钉加热,来除去铁钉表面的铁锈。根据此实验回答相关问题。
(1)给试管里的稀盐酸和带锈铁钉加热,实验现象为________________ 。
(2)一部分同学做实验时加热至沸腾较长时间后取出铁钉,发现铁钉上的铁锈仍没有除尽。可能原因除了加入盐酸的量不足外,沸腾时间太长也是重要的原因,因为_____________ 。
(3)几位同学仔细观察除锈后的铁钉表面是黑色的,便取黑色粉末来探究其成分。
【提出问题】黑色粉末中可能含哪些物质?
【查阅资料】氧化铁为红棕色,四氧化三铁和氧化亚铁都为黑色,细小的铁粉也可能为黑色。
只有四氧化三铁和铁能被磁铁吸引。铁的氧化物都能与稀盐酸反应。
【进行猜想】小明猜想黑色粉末应该由铁成铁的氯化物组成。小华认为小明的猜想是片面的,正确的猜想应该是______________ 。
【实验探究】
【实验结论】
黑色粉末中一定含有____________ 。四氧化三铁的化学式可以写成另一种形式: 。其与盐酸反应的化学方程式可以为
。其与盐酸反应的化学方程式可以为_______________ 。
(1)给试管里的稀盐酸和带锈铁钉加热,实验现象为
(2)一部分同学做实验时加热至沸腾较长时间后取出铁钉,发现铁钉上的铁锈仍没有除尽。可能原因除了加入盐酸的量不足外,沸腾时间太长也是重要的原因,因为
(3)几位同学仔细观察除锈后的铁钉表面是黑色的,便取黑色粉末来探究其成分。
【提出问题】黑色粉末中可能含哪些物质?
【查阅资料】氧化铁为红棕色,四氧化三铁和氧化亚铁都为黑色,细小的铁粉也可能为黑色。
只有四氧化三铁和铁能被磁铁吸引。铁的氧化物都能与稀盐酸反应。
【进行猜想】小明猜想黑色粉末应该由铁成铁的氯化物组成。小华认为小明的猜想是片面的,正确的猜想应该是
【实验探究】
| 实验步骤 | 实验现象 |
| 黑色粉末,用磁铁吸引 | 黑色粉末中的大部分被吸引 |
| 将黑色粉末放入足量的稀盐酸中,加热 | 黑色粉末中的大部分溶于酸中,无气泡,少量不溶 |
黑色粉末中一定含有
兴趣小组对“影响金属锌与稀硫酸反应速率的因素”进行了如下实验探究。
【进行实验】
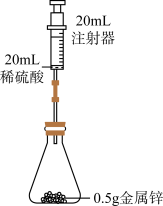
室温下,选用20mL不同溶质质量分数的硫酸(4%和8%)分别与0.5g颗粒状和粉末状的金属锌进行实验(固定夹持仪器略去)。
(1)金属锌与稀硫酸反应的化学方程式为_______________ 。
(2)按上图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是向上拉动活塞,_______________ 。
(3)老师提醒,开始实验时注射器中的稀硫酸应快速推入锥形瓶中,你认为原因是_______________ 。
(4)现需要50mL(密度为1g.mL-1)溶质质量分数为4%的稀硫酸,需要溶质质量分数为8%的稀硫酸_______________ g。
(5)实验小组进行实验后,获得的相关实验数据如下表所示:
①比较不同溶质质量分数的硫酸对反应速率的影响,可选择的实验编号是_______________ ,由此可得到的结论是_______________ 。
②从以上数据中,实验小组还打算研究的问题是_______________ 。
【拓展延伸】
(6)下表是实验时记录生成的氢气体积和对应的时间的一组实验数据(每间隔4S读数一次):
从上表记录可知该记录为实验编号_______________ 的实验数据,经分析得出反应速率的随时间的变化规律为_______________ 。
(7)你认为影响金属锌与稀硫酸反应速率的因素还有_______________ ,请设计实验方案验证你的猜想_______________ 。

【进行实验】
室温下,选用20mL不同溶质质量分数的硫酸(4%和8%)分别与0.5g颗粒状和粉末状的金属锌进行实验(固定夹持仪器略去)。
(1)金属锌与稀硫酸反应的化学方程式为
(2)按上图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是向上拉动活塞,
(3)老师提醒,开始实验时注射器中的稀硫酸应快速推入锥形瓶中,你认为原因是
(4)现需要50mL(密度为1g.mL-1)溶质质量分数为4%的稀硫酸,需要溶质质量分数为8%的稀硫酸
(5)实验小组进行实验后,获得的相关实验数据如下表所示:
| 实验编号 | 硫酸溶质质量分数(均取20mL) | 金属锌形态(均取0.5g) | 氢气体积(mL) (均收集前20S的气体) |
| a | 4% | 粉状 | 85.7 |
| b | 4% | 颗粒 | 53.0 |
| c | 8% | 粉状 | 162.2 |
| d | 8% | 颗粒 | 84.3 |
②从以上数据中,实验小组还打算研究的问题是
【拓展延伸】
(6)下表是实验时记录生成的氢气体积和对应的时间的一组实验数据(每间隔4S读数一次):
| 时间/S | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
| 气体体积/mL | 15.0 | 31.1 | 48.4 | 67.3 | 85.7 | 92.6 | 100.1 | 105.3 | 108.0 | 109.4 |
(7)你认为影响金属锌与稀硫酸反应速率的因素还有
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


