科学探究题 较难0.4 引用3 组卷232
某兴趣小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣。在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验。
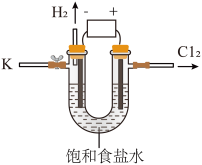
(1)电解饱和食盐水可以制得氢氧化钠、氯气(C12)和氢气,进而生产具有消毒、漂白作用的“84”消毒液。
①实验过程中与负极相连的导管口周围严禁明火,其原因是_______ 。
②写出电解饱和食盐水的化学方程式_______ 。
③制取“84”消毒液(有效成分为NaClO)的原理: ;小吴向2mL“84”消毒液中滴加2-3滴无色酚酞试液,发现溶液先变红后褪色,说明“84”消毒液显
;小吴向2mL“84”消毒液中滴加2-3滴无色酚酞试液,发现溶液先变红后褪色,说明“84”消毒液显______ 性,并有漂白性。
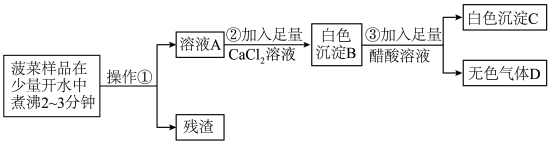
(2)该兴趣小组的同学想了解久置的“84”消毒液是否变质,设计了下列探究实验。
【查阅资料】
①品红溶液是一种红色色素。
②“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO2反应( )。NaClO溶液、HClO都具有漂白、杀菌、消毒功效,能使品红溶液褪色氯化钠和碳酸钠不能使品红溶液褪色。
)。NaClO溶液、HClO都具有漂白、杀菌、消毒功效,能使品红溶液褪色氯化钠和碳酸钠不能使品红溶液褪色。
③HClO不稳定,受热或光照会分解,分解后丧失漂白作用。
④Ca(ClO)2易溶于水
【提出问题】放置一段时间的“84”消毒液是否变质?如果变质,变质程度如何?
【提出猜想】猜想1:未变质,溶液中主要成分为NaCl、NaC1O
猜想2:部分变质,溶液中主要成分为__________ 。
猜想3:全部变质,溶液中主要成分为NaC1、Na2CO3
【实验探究】
写出实验操作①中产生白色沉淀的化学方程式_________ 。
【交流反思】实验最终确定猜想3成立。有人提出直接将这样的“84”消毒液倒掉会污染环境,为了将碳酸钠除去,我们应该向其中加入稀盐酸,直到_________ 为止。
【拓展应用】“84”消毒液存放时应注意的事项是_________ 。

(1)电解饱和食盐水可以制得氢氧化钠、氯气(C12)和氢气,进而生产具有消毒、漂白作用的“84”消毒液。
①实验过程中与负极相连的导管口周围严禁明火,其原因是
②写出电解饱和食盐水的化学方程式
③制取“84”消毒液(有效成分为NaClO)的原理:
(2)该兴趣小组的同学想了解久置的“84”消毒液是否变质,设计了下列探究实验。
【查阅资料】
①品红溶液是一种红色色素。
②“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO2反应(
③HClO不稳定,受热或光照会分解,分解后丧失漂白作用。
④Ca(ClO)2易溶于水
【提出问题】放置一段时间的“84”消毒液是否变质?如果变质,变质程度如何?
【提出猜想】猜想1:未变质,溶液中主要成分为NaCl、NaC1O
猜想2:部分变质,溶液中主要成分为
猜想3:全部变质,溶液中主要成分为NaC1、Na2CO3
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取适量该溶液于烧杯中,滴入适量氯化钙溶液 | 产生白色沉淀 | 猜想 |
| ②另取适量该溶液于试管中,滴入几滴品红溶液 | 猜想3成立 |
【交流反思】实验最终确定猜想3成立。有人提出直接将这样的“84”消毒液倒掉会污染环境,为了将碳酸钠除去,我们应该向其中加入稀盐酸,直到
【拓展应用】“84”消毒液存放时应注意的事项是
2022·江苏泰州·一模
类题推荐
实验室中有甲、乙两瓶过氧化氢溶液,均标有“10%”字样。相同条件下,用这两瓶过氧化氢溶液制取150mL氧气,所用时间明显不同。对此,同学们进行如下探究。
【猜想】两瓶过氧化氢溶液浓度不同
【进行实验】
【实验结论】
甲瓶溶液浓度大于乙瓶溶液浓度。
【分析与解释】
(1)实验2和实验3中,均发生反应的文字表达式(或符号表达式)为__________ 。
(2)实验2中,影响蜡烛燃烧明亮程度的因素是__________ 。
(3)实验3中,现象①为_____________ 。
【反思与评价】
(1)实验1未观察到现象明显不同的主要原因是_______________ 。
(2)通过以上实验得到如下启示:影响反应速率的因素有______________ ;欲使燃着的物质燃烧更旺,可采用的方法是 ___________________ 。
【猜想】两瓶过氧化氢溶液浓度不同
【进行实验】
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实 验 1 |  | 向两支试管中分别加入等量的甲、乙两瓶中的过氧化氢溶液,对比观察 | 两支试管中均有细微的气泡产生 |
| 实 验 2 |  | 将两个相同的蜡烛分别点燃后放入两个烧杯中,然后分别向两个烧杯中加入等量的甲、乙两瓶中的过氧化氢溶液,再向过氧化氢溶液中加入等量的二氧化锰固体 | 两烧杯内液体中均产生气泡、有白雾,两烧杯内蜡烛均继续燃烧,但加入甲瓶溶液的烧杯中,蜡烛燃烧得更明亮 |
| 实 验 3 | 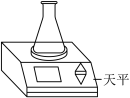 | 向装有等量二氧化锰的两个锥形瓶中分别加入等量的甲、乙两瓶中的过氧化氢溶液 | 两锥形瓶内液体中均产生气泡、有白雾,同时有现象①出现 |
甲瓶溶液浓度大于乙瓶溶液浓度。
【分析与解释】
(1)实验2和实验3中,均发生反应的文字表达式(或符号表达式)为
(2)实验2中,影响蜡烛燃烧明亮程度的因素是
(3)实验3中,现象①为
【反思与评价】
(1)实验1未观察到现象明显不同的主要原因是
(2)通过以上实验得到如下启示:影响反应速率的因素有
全世界每年因锈蚀造成浪费的金属高达产量的20%以上,但铁锈蚀原理却在日常生活中被广泛应用,例如暖宝宝、食品脱氧剂等。小组同学对暖宝宝发热产生兴趣,展开探究。
【资料信息】
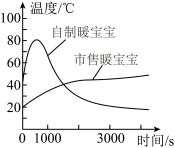
【实验1】分别取2勺铁粉和活性炭,加入无纺布袋中(与市售暖宝宝所用无纺布相同),滴加少量氯化钠溶液,混合均匀制得暖宝宝。在相同环境下,利用温度传感器测定自制与市售暖宝宝温度随时间的变化,形成图像,如图所示。通过图像可知自制暖宝宝有两点不足,分别是_______ 、_______ 。
【猜想与假设】暖宝宝成分中氯化钠、活性炭可能加快铁锈蚀速率,使反应在短时间内放出大量的热。
【实验2】小组同学通过反应过程中温度的变化,探究氯化钠、活性炭及两者共同存在对铁锈蚀速率的影响,设计完成如下4组实验。(实验在密闭容器中进行)
【解释与结论】
(1)对比实验1和2,可探究氯化钠对铁锈蚀速率的影响,表中m=_______ 。
(2)为探究活性炭对铁锈蚀速率的影响,应选择的实验组合是_______ (填编号)。
(3)综合以上4组实验得出结论:_______ 。
【拓展交流】小组同学运用该原理设计了如图所示的对比实验,测定空气中氧气的含量。
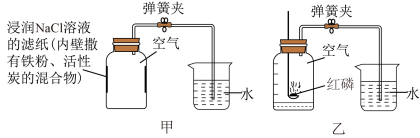
(4)红磷燃烧的化学方程式为_______ 。
(5)结合反应原理和结果思考装置甲的优点是_______ 。
【资料信息】
| 成分:铁粉、蛭石(保温)、高分子吸水树脂(供水)、氯化钠、活性炭 内袋材料:微孔透气无纺布 注意事项:不使用时请勿拆开密封包装 |

【猜想与假设】暖宝宝成分中氯化钠、活性炭可能加快铁锈蚀速率,使反应在短时间内放出大量的热。
【实验2】小组同学通过反应过程中温度的变化,探究氯化钠、活性炭及两者共同存在对铁锈蚀速率的影响,设计完成如下4组实验。(实验在密闭容器中进行)
| 实验编号 | 铁粉/g | 水/mL | 活性炭/g | 氯化钠/g | 测得10min内温度上升值/℃ |
| 1 | 2 | 5 | 0 | 0 | 0.1 |
| 2 | 2 | 5 | m | 0.1 | 3.1 |
| 3 | 2 | 5 | 0.2 | 0 | 22.0 |
| 4 | 2 | 5 | 0.2 | 0.1 | 56.3 |
(1)对比实验1和2,可探究氯化钠对铁锈蚀速率的影响,表中m=
(2)为探究活性炭对铁锈蚀速率的影响,应选择的实验组合是
(3)综合以上4组实验得出结论:
【拓展交流】小组同学运用该原理设计了如图所示的对比实验,测定空气中氧气的含量。

(4)红磷燃烧的化学方程式为
(5)结合反应原理和结果思考装置甲的优点是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网