填空与简答-填空题 适中0.65 引用5 组卷905
如图是a、b、c三种物质的溶解度曲线,据图回答下列问题:
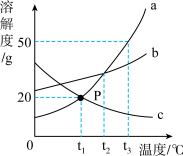
(1)三种物质的溶解度随着温度升高而减小的是______ 。
(2)t2℃时,物质a的溶解度与物质______ 的溶解度相等。
(3)t3℃时,把80g物质a加入200g水中充分搅拌、静置,形成的是______ (填“饱和”或“不饱和”)溶液。
(4)t3℃时,将等质量a和b的饱和溶液降到t1℃时,析出晶体的质量关系正确的是______(填字母序号)。
(5)如果a中混有少量固体b,若提纯a,一般采用______ 的方法。

(1)三种物质的溶解度随着温度升高而减小的是
(2)t2℃时,物质a的溶解度与物质
(3)t3℃时,把80g物质a加入200g水中充分搅拌、静置,形成的是
(4)t3℃时,将等质量a和b的饱和溶液降到t1℃时,析出晶体的质量关系正确的是______(填字母序号)。
| A.a>b | B.a=b | C.a<b | D.不能确定 |
(5)如果a中混有少量固体b,若提纯a,一般采用
21-22九年级上·山东日照·期末
类题推荐
高锰酸钾是锰的重要化合物和常用的氧化剂。如图是工业上用软锰矿(主要成分是MnO2)制备高锰酸钾流程图。
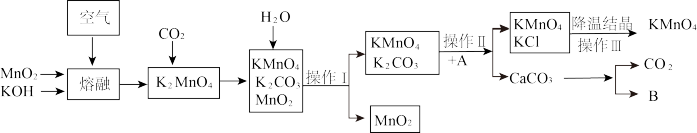
(1)MnO2、KOH在高温熔融的条件下通入空气时生成锰酸钾和水,该反应的化学方程式为___________ 。
(2)操作Ⅱ的名称是___________ 。
(3)物质A为___________ (填化学式),物质B的用途是___________ (写一种)。
(4)上述流程中可循环使用的物质有___________(填字母序号)。
(5)从操作Ⅲ分析,KMnO4的溶解度随温度的变化比KCl变化___________ (填“大”或“小”)。

(1)MnO2、KOH在高温熔融的条件下通入空气时生成锰酸钾和水,该反应的化学方程式为
(2)操作Ⅱ的名称是
(3)物质A为
(4)上述流程中可循环使用的物质有___________(填字母序号)。
| A.MnO2 | B.K2CO3 | C.CO2 | D.K2MnO4 |
分析下列溶解度相关数据和曲线,回答有关问题。
(1)在40℃,KNO3的溶解度是______ 。
(2)在KNO3和NaCl中,_____ 的溶解度受温度变化影响较大。
(3)将180gKNO3和20gNaCl固体混合物,放入100℃的热水中,充分搅拌,完全溶解,再将所得混合溶液降温到20℃时,析出的晶体是_____ 。
(4)温度在_____ 范围内,KNO3和NaCl的溶解度可能相等。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(2)在KNO3和NaCl中,
(3)将180gKNO3和20gNaCl固体混合物,放入100℃的热水中,充分搅拌,完全溶解,再将所得混合溶液降温到20℃时,析出的晶体是
(4)温度在
碳酸锶 是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90%
是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90%  ,少量
,少量 、
、 、
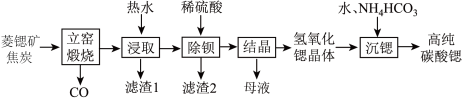
、 等)制备高纯碳酸锶的工艺流程如图:
等)制备高纯碳酸锶的工艺流程如图:
①不溶性碳酸盐高温下可以分解,生成金属氧化物和 气体。可溶性碳酸盐高温不分解。
气体。可溶性碳酸盐高温不分解。
②可溶性碱(如:NaOH)中金属元素(Na)形成的氧化物 才能与水反应生成对应的碱(NaOH),反之,不溶性碱[如Cu(OH)2]中金属元素(Cu)形成的氧化物(CuO)不能与水反应。
才能与水反应生成对应的碱(NaOH),反之,不溶性碱[如Cu(OH)2]中金属元素(Cu)形成的氧化物(CuO)不能与水反应。
③金属锶:化学性质非常活泼,可直接与水反应生成氢氧化锶和氢气。
④氢氧化锶在水中的溶解度数据如表 :
请回答以下问题:
(1)氢氧化锶的化学式为______ 。
(2)菱锶矿、焦炭混合后,为使得反应速率加快可行的方法是______ 。
(3)滤渣1含有焦炭、Cu(OH)2和______ 。
(4)“结晶”采用的是______ 结晶法,“沉锶”反应中氢氧化锶和 发生反应,产物除了碳酸锶外 ,还有水和一水合氨,该反应温度控制在65~80℃,其不低于65℃且不高于80℃的原因是
发生反应,产物除了碳酸锶外 ,还有水和一水合氨,该反应温度控制在65~80℃,其不低于65℃且不高于80℃的原因是______ 。
(5)锶铁氧体是由锶和铁的氧化物组成的符合磁性材料。要制备某种锶铁氧体(化学式为SrO·6Fe2O3,相对分子质量为1064)5.32t,不考虑过程中的损失理论上至少需要含 80%的菱锶矿石多少
80%的菱锶矿石多少______ t?
①不溶性碳酸盐高温下可以分解,生成金属氧化物和
②可溶性碱(如:NaOH)中金属元素(Na)形成的氧化物
③金属锶:化学性质非常活泼,可直接与水反应生成氢氧化锶和氢气。
④氢氧化锶在水中的溶解度数据如表 :
| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/(g/100g) | 12.5 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)氢氧化锶的化学式为
(2)菱锶矿、焦炭混合后,为使得反应速率加快可行的方法是
(3)滤渣1含有焦炭、Cu(OH)2和
(4)“结晶”采用的是
(5)锶铁氧体是由锶和铁的氧化物组成的符合磁性材料。要制备某种锶铁氧体(化学式为SrO·6Fe2O3,相对分子质量为1064)5.32t,不考虑过程中的损失理论上至少需要含
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


