科学探究题 较难0.4 引用3 组卷616
兴趣小组同学对氧气的收集进行了进一步探究:
【提出问题】不同的收集方法收集中的操作是否影响氧气的纯度?
【知识回顾】氧气能向上排空气法收集,所利用氧气的物理性质是______ ,用排水法集氧气时,判断氧气已收集满的依据是______ 。
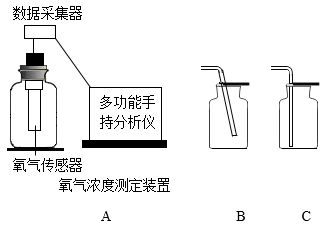
【实验设计】分别按下列方法,重复收集三瓶氧气,然后利用氧气传感器测定氧气的浓度(装置如图A),记录并取平均值。
(1)用排水法收集氧气:①导管口一冒出气泡就进行收集;②当导管口气泡连续且较均匀时进行收集。
(2)用向上排空气法收集氧气:③按图B所示,将导管伸入集气瓶中部进行收集,以能使放置在集气瓶口带火星木条复燃为氧气集满的标准;④按图C所示,将导管伸入近集气瓶底部进行收集,以能使放置在集气瓶口带火星木条复燃为氧气集满的标准;⑤按图C所示,将导管伸入近集气瓶底部进行收集,将氧气集满标准改为以能使放置在集气瓶口带火星木条复燃后再收集40s。
【实验记录】
【分析】
(1)实验中每一种收集方法、操作均收集三瓶,并取其平均值,目的是______ 。
(2)①、②均采用排水法收集,但①所得氧气浓度明显更小,其原因是______ 。
(3)对比③、④的数据,用向上排空气法收集气体时,需注意______ 。
(4)若采用向上排空气收集氧气时,要收集到较纯的氧气,可采取的措施是______ 。
【结论】收集方法、操作对收集气体的纯度有影响。
【拓展】通过探究,兴趣小组同学认为使带火星的木条复燃的氧气不一定是纯净的氧气,小组同学实验得知:先向集气瓶中加入其容积35%的水,然后用排水法利用氧气将瓶中的水排出,所得到的气体可使带火星的木条复燃,此时瓶中气体中氧气的体积分数约为______ 。
【提出问题】不同的收集方法收集中的操作是否影响氧气的纯度?
【知识回顾】氧气能向上排空气法收集,所利用氧气的物理性质是
【实验设计】分别按下列方法,重复收集三瓶氧气,然后利用氧气传感器测定氧气的浓度(装置如图A),记录并取平均值。
(1)用排水法收集氧气:①导管口一冒出气泡就进行收集;②当导管口气泡连续且较均匀时进行收集。
(2)用向上排空气法收集氧气:③按图B所示,将导管伸入集气瓶中部进行收集,以能使放置在集气瓶口带火星木条复燃为氧气集满的标准;④按图C所示,将导管伸入近集气瓶底部进行收集,以能使放置在集气瓶口带火星木条复燃为氧气集满的标准;⑤按图C所示,将导管伸入近集气瓶底部进行收集,将氧气集满标准改为以能使放置在集气瓶口带火星木条复燃后再收集40s。

【实验记录】
| 收集方法、操作 | ① | ② | ③ | ④ | ⑤ |
| 氧气平均浓度/% | 63.7 | 89.7 | 67.0 | 79.7 | 88.4 |
【分析】
(1)实验中每一种收集方法、操作均收集三瓶,并取其平均值,目的是
(2)①、②均采用排水法收集,但①所得氧气浓度明显更小,其原因是
(3)对比③、④的数据,用向上排空气法收集气体时,需注意
(4)若采用向上排空气收集氧气时,要收集到较纯的氧气,可采取的措施是
【结论】收集方法、操作对收集气体的纯度有影响。
【拓展】通过探究,兴趣小组同学认为使带火星的木条复燃的氧气不一定是纯净的氧气,小组同学实验得知:先向集气瓶中加入其容积35%的水,然后用排水法利用氧气将瓶中的水排出,所得到的气体可使带火星的木条复燃,此时瓶中气体中氧气的体积分数约为
21-22九年级上·江西南昌·阶段练习
类题推荐
某化学兴趣小组在实验室用氯酸钾(KClO3)和二氧化锰混合加热制取氧气,实验时偶然发现制得的气体有刺激性气味,老师指导小组成员对该气体成分进行探究。
查阅资料发现:
资料Ⅰ、氯酸钾与二氧化锰混合加热时,钾、锰元素不能形成气体,产生的气体均以单质的形式存在。
资料Ⅱ、氯气(Cl2)是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
(1)猜想与假设
猜想一:该气体为O2;
猜想二:该气体为______ ;
猜想三:该气体为O2和Cl2的混合物。
(2)实验探究
(3)反思与评价:为什么两种方案得出的结论不一致?哪个是正确的?
①甲同学:方案Ⅰ结论不正确,其操作不合理,理由是______ 。
②乙同学:不需要另外进行实验操作就能排除猜想一,理由是______ 。
③老师:若已排除猜想一,只需要完成其中______ 瓶(填“A”或“B”)的实验即可。
(4)拓展应用
①实验结束后,该组同学准备回收固体剩余物中的不溶物二氧化锰,实验的主要步骤为:溶解、______ 、洗涤干燥、称量。
②再次查询资料得知,氯酸钾和二氧化锰共热会发生以下变化:
第Ⅰ步。二氧化锰首先和氯酸钾反应生成高锰酸钾和氯气和氧气;
第Ⅱ步。高锰酸钾接着分解。
第Ⅲ步。锰酸钾再和氯气反应生成氯化钾、二氧化锰和氧气。
写出第Ⅰ步反应的文字表达式______ 。
(5)通过本次探究,你认为以下说法正确的是______(填字母)。
查阅资料发现:
资料Ⅰ、氯酸钾与二氧化锰混合加热时,钾、锰元素不能形成气体,产生的气体均以单质的形式存在。
资料Ⅱ、氯气(Cl2)是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
(1)猜想与假设
猜想一:该气体为O2;
猜想二:该气体为
猜想三:该气体为O2和Cl2的混合物。
(2)实验探究
方案 | 操作 | 现象 | 结论 |
方案Ⅰ | 用排水集气法收集A、B两瓶气体,将带火星的木条伸入A瓶,湿润的淀粉碘化钾试纸伸入B瓶。 | 木条复燃,淀粉碘化钾试纸 | 猜想一成立 |
方案Ⅱ | 用向上排空气法收集A、B两瓶气体,将带火星的木条伸入A瓶,湿润的淀粉碘化钾试纸伸入B瓶。 | 木条 | 猜想三成立 |
①甲同学:方案Ⅰ结论不正确,其操作不合理,理由是
②乙同学:不需要另外进行实验操作就能排除猜想一,理由是
③老师:若已排除猜想一,只需要完成其中
(4)拓展应用
①实验结束后,该组同学准备回收固体剩余物中的不溶物二氧化锰,实验的主要步骤为:溶解、
②再次查询资料得知,氯酸钾和二氧化锰共热会发生以下变化:
第Ⅰ步。二氧化锰首先和氯酸钾反应生成高锰酸钾和氯气和氧气;
第Ⅱ步。高锰酸钾接着分解。
第Ⅲ步。锰酸钾再和氯气反应生成氯化钾、二氧化锰和氧气。
写出第Ⅰ步反应的文字表达式
(5)通过本次探究,你认为以下说法正确的是______(填字母)。
| A.催化剂起催化作用过程时,可能会参加反应 |
| B.某个化学反应可能同时伴随着多个反应 |
| C.对于实验出现的意外现象,根本不要去理会 |
| D.学习物质的性质上网查询即可,没必要进行实验探究 |
小雨同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液,小雨看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
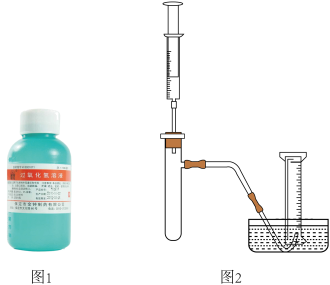
(1)小雨同学准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。
I、请写出实验室过氧化氢分解制氧气的文字表达式:______ 。
Ⅱ、小雨同学为了检验该气体是否是氧气,把导气管从水中取出,将带火星的木条放在导气管口处,观察到______ ,说明生成的气体是氧气。
(2)小雨查阅了相关资料,并进行了探究实验:
【查阅资料】
I、过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
Ⅱ、温度对化学反应的快慢有影响,人体正常体温是37℃。
【提出猜想】
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
【进行实验】
【实验反思】小雨反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
I、你认为小雨的实验中所用过氧化氢溶液除浓度相同外,体积应该是______ mL。
Ⅱ、通过这些数据,你能得出的新结论是______ 。

(1)小雨同学准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。
I、请写出实验室过氧化氢分解制氧气的文字表达式:
Ⅱ、小雨同学为了检验该气体是否是氧气,把导气管从水中取出,将带火星的木条放在导气管口处,观察到
(2)小雨查阅了相关资料,并进行了探究实验:
【查阅资料】
I、过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
Ⅱ、温度对化学反应的快慢有影响,人体正常体温是37℃。
【提出猜想】
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
【进行实验】
序号 | 实验步骤 | 实验现象 | 实验结论 |
1 | 分两次进行实验,均注入等体积过氧化氢溶液 第一次在常温下进行 第二次将试管浸在37℃的温水中 | 量筒中2分钟收集到的气体体积均为5mL | |
2 | 分两次进行实验: 第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液; 第二次 | 第一次,量筒中2分钟收集到的气体体积为 第二次,量筒中2分钟收集到的气体体积为5mL | 过氧化氢分解加快是因为过氧化氢酶的作用 |
加入过氧化氢酶 | 不加过氧化氢酶 | |||||
反应温度/℃ | 25 | 37 | 42 | 25 | 37 | 42 |
收集到气体体积/mL | 39 | 56 | 34 | 5 | 5 | 5 |
Ⅱ、通过这些数据,你能得出的新结论是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


