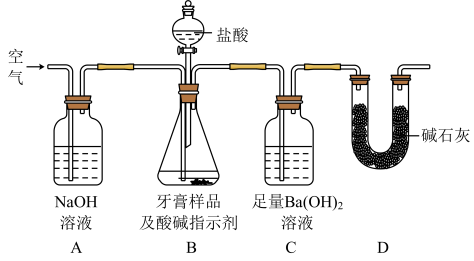
科学探究题 适中0.65 引用1 组卷67
工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。(装置气密性良好)
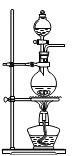
【问题讨论】某兴趣小组用草酸分解所得气体和下图所示装置进行实验,来测定某工业铁红中铁元素的质量分数:
【资料1】草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:H2C2O4·3H2O CO2↑+ CO↑+ 4H2O
CO2↑+ CO↑+ 4H2O
【资料2】碱石灰是碱石灰主要成分为CaO和NaOH,可吸收H2O和CO2。
【资料3】铁的常见氧化物中铁的质量分数:
(1)为了保证进入E中的气体是纯净、干燥的CO,则B,C,D中的试剂依次是______ 、______ ,______ (填字母编号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(2)熄灭E处酒精灯后要继续通CO目的是______ 。
(3)写出E装置中所发生反应的一个化学方程式______ 。
(4)称取铁红样品10.0g用上述装置进行实验,测定铁红中铁元素的质量分数,若实验前后称得F装置增重7.7g,则此铁红中铁元素的质量分数是______
【实验反思】
如果缺少G装置(不考虑其他因素),则测得样品中铁元素的质量分数会______ (选填“偏小”“不变”“偏大”)。

【问题讨论】某兴趣小组用草酸分解所得气体和下图所示装置进行实验,来测定某工业铁红中铁元素的质量分数:

【资料1】草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:H2C2O4·3H2O
【资料2】碱石灰是碱石灰主要成分为CaO和NaOH,可吸收H2O和CO2。
【资料3】铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
(1)为了保证进入E中的气体是纯净、干燥的CO,则B,C,D中的试剂依次是
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(2)熄灭E处酒精灯后要继续通CO目的是
(3)写出E装置中所发生反应的一个化学方程式
(4)称取铁红样品10.0g用上述装置进行实验,测定铁红中铁元素的质量分数,若实验前后称得F装置增重7.7g,则此铁红中铁元素的质量分数是
【实验反思】
如果缺少G装置(不考虑其他因素),则测得样品中铁元素的质量分数会
20-21九年级上·湖北武汉·阶段练习
类题推荐
某化学兴趣小组设计了如下实验来探究影响锌与稀硫酸反应速率的因素(实验过程中杂质不能与稀硫酸反应),实验数据记录如下表:
(1)实验_____ 和实验______ (填实验编号)的实验目的是为了研究硫酸浓度对反应速率的影响。
(2)对比实验a和实验b,可以得到的实验结论是____________________ 。
(3)计算9.8g纯硫酸与足量的锌完全反应,可制得氢气是_________ 克?请你帮他们完善计算过程:
①______________ ②____________________
| 实验编号 | 试剂 | 产生50mL氢气 的时间/s | ||
| 不同纯度的锌 | 稀硫酸的浓度 | 稀硫酸的用量/ mL | ||
| a | 纯锌 | 30% | 30 | 52 |
| b | 含杂质的锌 | 30% | 30 | 47 |
| c | 纯锌 | 20% | 30 | 68 |
| d | 纯锌 | 30% | 40 | 50 |
(2)对比实验a和实验b,可以得到的实验结论是
(3)计算9.8g纯硫酸与足量的锌完全反应,可制得氢气是
①
| 解:设9.8g硫酸与足量的锌完全反应可制得氢气的质量是X。 Zn+H2SO4=ZnSO4+H2↑ ①________ 2 9.8g X ②_____________(列出比例式) |
人类的生存离不开氧气,某校化学兴趣小组的同学在老师的指导下做了有关氧气的系列探究实验。
(1)探究一:某同学称取15.8g高锰酸钾(KMnO4)放在大试管中,将温度控制在250℃加热制取氧气(O2),理论上,该同学最多能收集到氧气(O2)的质量为________ g。实验结束时,发现收集到的氧气(O2)量大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】
猜想I:反应生成的二氧化锰(MnO2)分解放出氧气(O2)
猜想Ⅱ:反应生成的锰酸钾(K2MnO4)分解放出氧气(O2)
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想_______ 错误。
②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论。该组同学选择的实验方法是________ 。
③下列加热高锰酸钾制取氧气的部分操作示意图中,正确的是________ 。
①通过实验①和②对比可知,化学反应速率与________ 有关;从实验③和④对比可知,化学反应速率与温度的关系是:________ 。
②如果要证明MnO2是该反应的催化剂,还要补做2个实验(不需写出具体步骤):________ ;________ 。
(3)探究三:某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究。
已知:在空气中,温度超过40℃,白磷(化学符号为P)就可以自燃,即和氧气反应生成五氧化二磷。
如图是“空气中氧气体积分数测定”实验的改进装置。主要操作:在实际容积为150mL的集气瓶里,先装进50mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃。
①请写出白磷与氧气反应的化学方程式________ 。
②白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是________ ;若实验非常成功,最终集气瓶中水的体积约为________ mL。
③集气瓶里预先装进的50mL水,在实验过程中起到哪些作用?________ (填写序号,可以多选)
B.液封导气管末端,防止气体受热逸出
C.缓冲集气瓶内气压的骤然升高
(1)探究一:某同学称取15.8g高锰酸钾(KMnO4)放在大试管中,将温度控制在250℃加热制取氧气(O2),理论上,该同学最多能收集到氧气(O2)的质量为
【提出猜想】
猜想I:反应生成的二氧化锰(MnO2)分解放出氧气(O2)
猜想Ⅱ:反应生成的锰酸钾(K2MnO4)分解放出氧气(O2)
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想
②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论。该组同学选择的实验方法是
③下列加热高锰酸钾制取氧气的部分操作示意图中,正确的是
A.检查气密性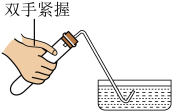
B.加热立即收集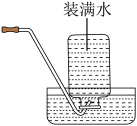
C.收满后移出集气瓶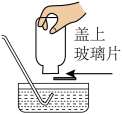
D.结束时停止加热
| 实验序号 | H2O2溶液浓度% | H2O2溶液体积mL | 温度/℃ | MnO2的用量g | 收集氧气的体积/mL | 反应所需的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
| ④ | 30 | 5 | 55 | 0 | 2 | 10.76 |
②如果要证明MnO2是该反应的催化剂,还要补做2个实验(不需写出具体步骤):
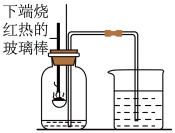
(3)探究三:某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究。
已知:在空气中,温度超过40℃,白磷(化学符号为P)就可以自燃,即和氧气反应生成五氧化二磷。
如图是“空气中氧气体积分数测定”实验的改进装置。主要操作:在实际容积为150mL的集气瓶里,先装进50mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃。
①请写出白磷与氧气反应的化学方程式
②白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是
③集气瓶里预先装进的50mL水,在实验过程中起到哪些作用?
B.液封导气管末端,防止气体受热逸出
C.缓冲集气瓶内气压的骤然升高
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网