综合应用题 较难0.4 引用4 组卷315
酸、碱、盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出_____ (填字母)。
a.H2O b.H2 c.H+ d.OH﹣
(2)检验敞口放置的氢氧化钠溶液是否变质,可以选用的一种试剂是____________________ 。
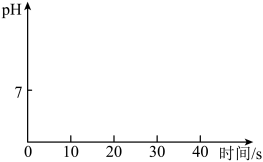
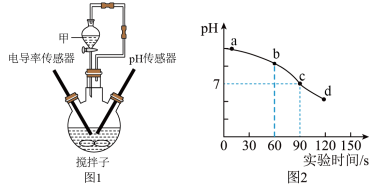
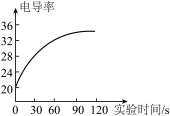
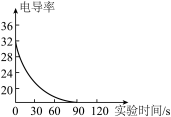
(3)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图1,当滴入溶液为V2mL时,所得溶液中溶质的化学式为__________ ,所得溶液能使紫色石蕊溶液变成____ 色。
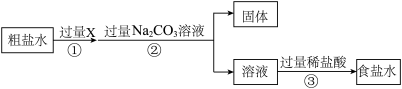
(4)氯化钠是生活中常见的盐。为除去某粗盐水中的MgSO4、CaCl2杂质,得到NaCl溶液,某化学小组设计了如图2实验方案:
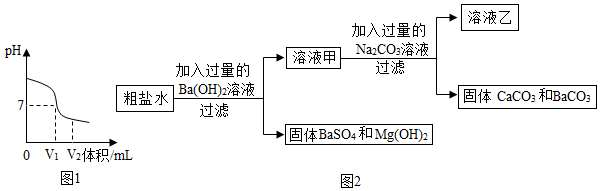
①过滤操作中所用到的玻璃仪器有烧杯、漏斗和_______ 。
②以上方案中有关反应的化学方程式为_________ (写一个即可)。
③写出溶液乙中含有的杂质,并将以上方案补充完整______ 。
(5)某实验室用20%的NaOH溶液洗涤一定量石油产品中残余的H2SO4,消耗NaOH溶液40g,洗涤后的溶液呈中性,请计算该一定量石油产品中H2SO4的质量。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出
a.H2O b.H2 c.H+ d.OH﹣
(2)检验敞口放置的氢氧化钠溶液是否变质,可以选用的一种试剂是
(3)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图1,当滴入溶液为V2mL时,所得溶液中溶质的化学式为
(4)氯化钠是生活中常见的盐。为除去某粗盐水中的MgSO4、CaCl2杂质,得到NaCl溶液,某化学小组设计了如图2实验方案:

①过滤操作中所用到的玻璃仪器有烧杯、漏斗和
②以上方案中有关反应的化学方程式为
③写出溶液乙中含有的杂质,并将以上方案补充完整
(5)某实验室用20%的NaOH溶液洗涤一定量石油产品中残余的H2SO4,消耗NaOH溶液40g,洗涤后的溶液呈中性,请计算该一定量石油产品中H2SO4的质量。
20-21九年级下·江苏连云港·阶段练习
类题推荐
氯化钠和碳酸钠在生活和生产中有着重要的作用和广泛的用途。
(1)下列不属于氯化钠的用途的是______(填字母序号)。
(2)某兴趣小组同学在盛有碳酸钠溶液的2支试管中分别进行如下实验。
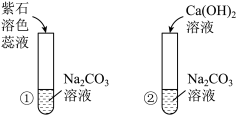
Ⅰ、试管①中的现象是______ 。
Ⅱ、试管②中有白色沉淀产生,同学们将试管②中的物质过滤,得到滤液,对滤液的成分进行了如下探究。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:NaOH 猜想二:NaOH、
猜想三:NaOH、 猜想四:NaOH、
猜想四:NaOH、 和
和
【设计与实验】
①大家认为猜想______ 一定不正确,其原因是______ 。
②甲同学取试管②中滤液样品,向其中加入足量的______ ,产生气泡,则猜想三正确;并写出反应时化学方程式______ 。
③请设计实验进一步验证试管②滤液样品中含有氢氧化钠______ 。
(3)某同学用500克质量分数为0.4%的NaOH溶液与溶质质量分数为7.3%的稀盐酸恰好完全反应,计算需要这种稀盐酸的质量是多少?
(1)下列不属于氯化钠的用途的是______(填字母序号)。
| A.配制生理盐水 | B.腌制咸菜 |
| C.冬天在公路上作融雪剂 | D.用食盐水除去热水瓶中的水垢 |

Ⅰ、试管①中的现象是
Ⅱ、试管②中有白色沉淀产生,同学们将试管②中的物质过滤,得到滤液,对滤液的成分进行了如下探究。
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:NaOH 猜想二:NaOH、
猜想三:NaOH、
【设计与实验】
①大家认为猜想
②甲同学取试管②中滤液样品,向其中加入足量的
③请设计实验进一步验证试管②滤液样品中含有氢氧化钠
(3)某同学用500克质量分数为0.4%的NaOH溶液与溶质质量分数为7.3%的稀盐酸恰好完全反应,计算需要这种稀盐酸的质量是多少?
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网