科学探究题 较难0.4 引用1 组卷51
某化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊。兴趣小组对这个异常现象进行了探究。
【提出问题】澄清石灰水为什么没有变浑浊?
【查阅资料】(1)CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2。
(2)AgCl不溶于稀硝酸。
【提出猜想】Ⅰ.石灰水已完全变质 Ⅱ._________ Ⅲ.CO2中混有HCl。
【实验方案】兴趣小组用原药品继续制取CO2,并进行探究。制备CO2的化学方程式为:___________ 。
【实验结论】制取的气体CO2中混入了HCl,澄清石灰水没有变浑浊,是因为___________ (用化学方程式表示)。
【交流讨论】若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和NaHCO3溶液和___________ 。
【拓展思考】回忆课本中收集呼出气体的操作后,同学们尝试用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊。你认为该实验成功的原因是___________ (写一点)。
【提出问题】澄清石灰水为什么没有变浑浊?
【查阅资料】(1)CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2。
(2)AgCl不溶于稀硝酸。
【提出猜想】Ⅰ.石灰水已完全变质 Ⅱ.
【实验方案】兴趣小组用原药品继续制取CO2,并进行探究。制备CO2的化学方程式为:
| 步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
| (1) | 取少量澄清石灰水于试管中,加入 | 产生白色沉淀 | 猜想Ⅰ不成立 |
| (2) | 将少量气体通入盛有澄清石灰水的试管中 | 猜想Ⅱ不成立 | |
| (3) | 将气体通入盛有 | 猜想Ⅲ成立。反应方程式为 |
【交流讨论】若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和NaHCO3溶液和
【拓展思考】回忆课本中收集呼出气体的操作后,同学们尝试用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊。你认为该实验成功的原因是
19-20九年级下·广东广州·阶段练习
类题推荐
某兴趣小组在学习了二氧化碳制取的研究课题时,探究了二氧化碳气体的收集方法。
【提出问题】二氧化碳能不能用排水法收集?
【作出猜想】
Ⅰ.不能用排水法收集,理由是_______ 。
Ⅱ.能够用排水法收集。
【查阅资料】
CO2不与碳酸氢钠反应,且难溶于饱和的碳酸氢钠溶液。
【实验设计与操作】
步骤一:小组同学用图1所示装置进行CO2气体的制取,在相同条件下,用如下3种方法,分别在三个规格相同的锥形瓶中收集产生的CO2气体。

方法①:当气体发生装置开始产生CO2气体15s后,用排水法收集CO2备用,并记录从收集到集满一瓶CO2所需的时间t;
方法②:当气体发生装置开始产生CO2气体15s后,采取与方法①相同的时间t,用向上排空气法收集一瓶CO2备用;
方法③:当气体发生装置开始产生CO2气体15s后,用向上排空气法收集,将燃着木条放在瓶口验满后,立即盖上玻璃片备用。
(1)请写出稀盐酸和石灰石反应的化学方程式_______ 。
(2)当气体发生装置开始产生CO2气体15s后,再开始收集气体的原因是_______ 。
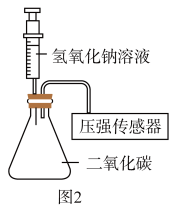
步骤二:将装有50mL5%的氢氧化钠溶液的注射器与压强传感器密封连接,再插入已经收集好CO2气体的锥形瓶中(如图2所示)。将注射器的氢氧化钠溶液注入锥形瓶中,观察瓶内压强变化情况。
【实验分析与结论】
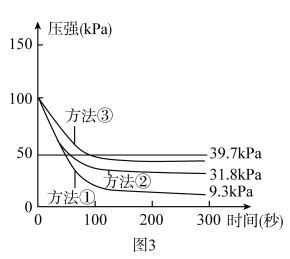
(3)用压强传感器测得密闭容器内压强随时间的变化关系如图3所示。根据实验结果可知,猜想___ (填“Ⅰ”或“Ⅱ”)成立。
(4)用燃着的木条验满CO2的方法____ (填“可靠”或“不可靠”)从收集的气体纯度考虑,方法___ (填“①”“②”或“③”)更好。
步骤三:小组同学进一步实验,比较两种收集方法收集等体积气体所需时间及纯度情况。
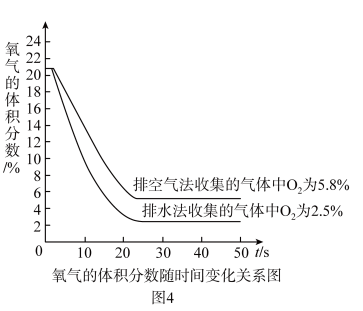
(5)小组同学用氧气传感器分别测定排空气法和排水法收集的等体积两瓶CO2气体中氧气的体积分数(数据如图4),则用排水法收集的气体中CO2体积分数约为_______ 。
(6)排水法和向上排空气法收集气体所需时间对照
小组同学分4组用排水法和排空气法分别收集1瓶(集气瓶容积相同)CO2气体,记录所需时间,如表所示。
综合上述实验,请你对CO2的两种收集方法做出评价:_______ 。
(7)实验结束后,图1中碳酸钙与稀盐酸反应后锥形瓶中的水溶液中除了生成的氯化钙外还有没有稀盐酸?请设计实验证明你的猜想(出写实验方法、现象和结论):_______ 。
(8)图1锥形瓶中饱和碳酸氢钠溶液的作用是_______ 。
(9)直接用排饱和的碳酸氢钠溶液的方法代替上图的排水法收集二氧化碳,其优点是_______ 。
【提出问题】二氧化碳能不能用排水法收集?
【作出猜想】
Ⅰ.不能用排水法收集,理由是
Ⅱ.能够用排水法收集。
【查阅资料】
CO2不与碳酸氢钠反应,且难溶于饱和的碳酸氢钠溶液。
【实验设计与操作】
步骤一:小组同学用图1所示装置进行CO2气体的制取,在相同条件下,用如下3种方法,分别在三个规格相同的锥形瓶中收集产生的CO2气体。


方法①:当气体发生装置开始产生CO2气体15s后,用排水法收集CO2备用,并记录从收集到集满一瓶CO2所需的时间t;
方法②:当气体发生装置开始产生CO2气体15s后,采取与方法①相同的时间t,用向上排空气法收集一瓶CO2备用;
方法③:当气体发生装置开始产生CO2气体15s后,用向上排空气法收集,将燃着木条放在瓶口验满后,立即盖上玻璃片备用。
(1)请写出稀盐酸和石灰石反应的化学方程式
(2)当气体发生装置开始产生CO2气体15s后,再开始收集气体的原因是
步骤二:将装有50mL5%的氢氧化钠溶液的注射器与压强传感器密封连接,再插入已经收集好CO2气体的锥形瓶中(如图2所示)。将注射器的氢氧化钠溶液注入锥形瓶中,观察瓶内压强变化情况。
【实验分析与结论】
(3)用压强传感器测得密闭容器内压强随时间的变化关系如图3所示。根据实验结果可知,猜想
(4)用燃着的木条验满CO2的方法
步骤三:小组同学进一步实验,比较两种收集方法收集等体积气体所需时间及纯度情况。


(5)小组同学用氧气传感器分别测定排空气法和排水法收集的等体积两瓶CO2气体中氧气的体积分数(数据如图4),则用排水法收集的气体中CO2体积分数约为
(6)排水法和向上排空气法收集气体所需时间对照
小组同学分4组用排水法和排空气法分别收集1瓶(集气瓶容积相同)CO2气体,记录所需时间,如表所示。
| 1 | 2 | 3 | 4 | |
| 排水法 | 35″ | 43″ | 43″ | 43″ |
| 排空气法 | 1′57″ | 1′15″ | 1′4″ | 1′12″ |
(7)实验结束后,图1中碳酸钙与稀盐酸反应后锥形瓶中的水溶液中除了生成的氯化钙外还有没有稀盐酸?请设计实验证明你的猜想(出写实验方法、现象和结论):
(8)图1锥形瓶中饱和碳酸氢钠溶液的作用是
(9)直接用排饱和的碳酸氢钠溶液的方法代替上图的排水法收集二氧化碳,其优点是
同学们选用两组不同浓度的盐酸完成图1装置中的实验。
 、
、
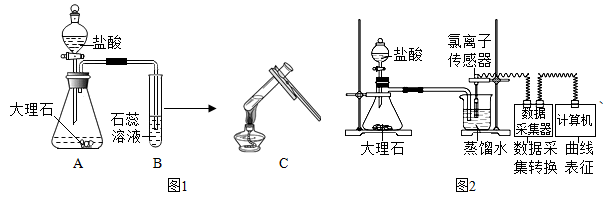
化学小组用图1装置验证二氧化碳与水的反应。
(1)A中反应的化学方程式为_____ 。
(2)乙组C中反应的化学方程式为_____ 。
【讨论与交流】同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶液。
【提出猜想】盐酸的挥发性与浓度有关。
【进行实验】用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见表。
盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
分析表中数据,能够得出盐酸的挥发性与浓度的关系是_____ 。
【得出结论】猜想正确
【实验反思】甲组石蕊溶液变红不能证明二氧化碳与水反应。
【实验改进】甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→_____ →_____ →b。饱和NaHCO3溶液的作用是_____ 。若将气体继续通入澄清石灰水,则反应的化学方程式为_____ 。
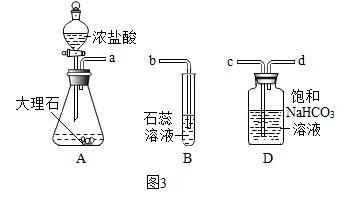
 、
、化学小组用图1装置验证二氧化碳与水的反应。
| 盐酸浓度 | 观察到的现象 | |
| 甲组 | 浓盐酸(36.5%) | B中石蕊溶液由紫色变成红色 C中石蕊溶液没有变为紫色 |
| 乙组 | 稀盐酸(13.5%) | B中石蕊溶液由紫色变为红色 C中石蕊溶液变为紫色 |
(1)A中反应的化学方程式为
(2)乙组C中反应的化学方程式为
【讨论与交流】同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶液。
【提出猜想】盐酸的挥发性与浓度有关。
【进行实验】用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见表。
盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
| 盐酸浓度(%) | 13.5 | 20 | 26.2 | 29.2 | 32.2 | 36.5 |
| 氯离子浓度(mg/L) | 1.1 | 1.4 | 3.7 | 19.0 | 59.8 | 209.2 |
分析表中数据,能够得出盐酸的挥发性与浓度的关系是
【得出结论】猜想正确
【实验反思】甲组石蕊溶液变红不能证明二氧化碳与水反应。
【实验改进】甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



