计算题 较难0.4 引用4 组卷585
某补钙剂的主要成分是碳酸钙,欲测定补钙剂中碳酸钙的质量分数,某同学进行了如图的操作: 已知:其他成分不参与反应且不溶于水
已知:其他成分不参与反应且不溶于水

(1)生成CO2的质量为_______g。
(2)计算该补钙剂中碳酸钙的质量分数。(根据化学方程式计算,写出完整步骤)
(3)反应后,向烧杯中再加入5.4g水,求所得溶液中溶质的质量分数。

(1)生成CO2的质量为_______g。
(2)计算该补钙剂中碳酸钙的质量分数。(根据化学方程式计算,写出完整步骤)
(3)反应后,向烧杯中再加入5.4g水,求所得溶液中溶质的质量分数。
2021·黑龙江·中考真题
类题推荐
为测定某种铝铜合金中铝的质量分数,探究小组按照下表进行实验:
请计算:
(1)实验______中稀盐酸和合金恰好完全反应。
(2)铝铜合金中铝的质量分数是多少?
| 实验编号 | 合金质量/g | 加入稀盐酸的质量/g | 生成H2的质量/g |
| 实验1 | 20 | 182.5 | 1 |
| 实验2 | 25 | 365 | 2 |
| 实验3 | 20 | 365 | 2 |
| 实验4 | 20 | 400 | 2 |
请计算:
(1)实验______中稀盐酸和合金恰好完全反应。
(2)铝铜合金中铝的质量分数是多少?
测定黄铜(铜锌合金)中铜的质量分数的过程如下,请回答下列问题:
(1)小华同学取50g黄铜,加入足量稀硫酸,共收集到1.0g气体,计算黄铜中铜的质量分数(写出计算过程)。
(2)小婷同学另取50g黄铜于烧杯中,将600g稀硫酸分六次加入,测得加入稀硫酸的质量和烧杯中剩余物的质量如下表:
①表中a=______ 。
②第六次实验后所得溶液的溶质是_______ (写化学式)。
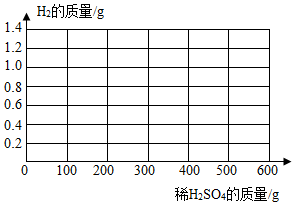
③画出加入0~600g稀硫酸过程中生成H2质量的变化图,并标注必要的数值。_____
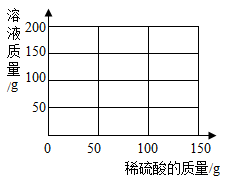
(3)请将第三组实验过程中,加入稀硫酸的质量与所形成溶液质量的关系曲线画在下图中。
(1)小华同学取50g黄铜,加入足量稀硫酸,共收集到1.0g气体,计算黄铜中铜的质量分数(写出计算过程)。
(2)小婷同学另取50g黄铜于烧杯中,将600g稀硫酸分六次加入,测得加入稀硫酸的质量和烧杯中剩余物的质量如下表:
| 次数 | 一 | 二 | 三 | 四 | 五 | 六 |
| 加入稀硫酸的质量/g | 100 | 100 | 100 | 100 | 100 | 100 |
| 烧杯中剩余物的质量/g | 149.8 | a | 349.4 | 449.2 | 549.0 | 649.0 |
②第六次实验后所得溶液的溶质是
③画出加入0~600g稀硫酸过程中生成H2质量的变化图,并标注必要的数值。

(3)请将第三组实验过程中,加入稀硫酸的质量与所形成溶液质量的关系曲线画在下图中。

菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究。取10g菱镁矿,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如下表
说明:菱镁矿中的杂质不溶于水,不与酸发生反应
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为_____。
(2)计算该菱镁矿中镁元素的质量分数____________。(写出计算过程)
(3)该实验研究中所用H2SO4溶液的溶质的质量分数是_____。
| 加入H2SO4溶液的质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加的质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
说明:菱镁矿中的杂质不溶于水,不与酸发生反应
(1)10g菱镁矿与H2SO4溶液完全反应,生成CO2的质量为_____。
(2)计算该菱镁矿中镁元素的质量分数____________。(写出计算过程)
(3)该实验研究中所用H2SO4溶液的溶质的质量分数是_____。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


