科学探究题 较难0.4 引用1 组卷143
同学们再学习额金属的化学性质后纷纷对金属的化学性质产生了兴趣,课后成立研究小组继续对金属的性质展开探究,下面是两个小组同学探究的内容:
第一组:小郝和小徐两位同学尝试着用镁条来验证金属的化学性质,两位同学的实验记录如下:
小郝:镁条灰黑色,不易点燃,放在白醋中反应很慢,较长时间以后才有气泡冒出。
小徐:镁条有银白色金属光泽,在空气中可以燃烧。在白醋中很快溶解并产生气泡,产生气泡的速率先是越来越快,后又变慢直至停止,且试管壁发烫。
已知:化学反应的剧烈程度与反应物的性质、反应物的浓度、温度、接触面积等因素有关。
(1)差异分析:你认为小郝同学在实验过程中缺少了哪一个步骤:______ 。
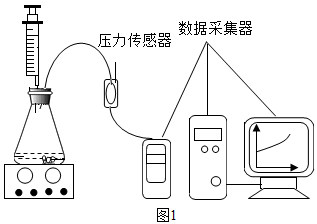
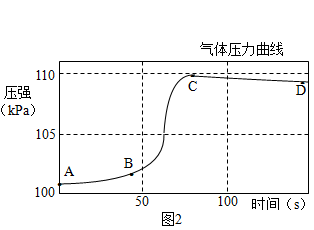
(2)小郝和小徐两位同学接着对镁条与白醋的反应进行了探究。将橡皮塞连接气体压力传感器,锥形瓶中放入一定量的镁条,针筒中放入白醋,塞紧瓶塞,将针筒中白醋推入锥形瓶并打开仪器(如图1所示)。一段时间后,得到气压压强与时间的关系曲线图(如图2所示)。到C点烧瓶内气压达到最大值说明______ ,CD段气压逐渐下降的原因是______ 。
(3)从AB段到BC段来看,反应的速率是先慢后快,导致变快的主要因素是______ (填字母)。
a、镁条的表面积 b、白醋的浓度 c、温度
第二组:第2组同学来到实验室想对锌、铜、银三种金属活动性顺序进行探究。实验桌上老师提供的药品有:锌片、铜片、银片、硫酸锌溶液、硫酸铜溶液、硝酸银溶液和稀硫酸。
【制定计划】在老师的指导下,经过讨论,同学们设计出了以下几种实验方案:
方案一:铜片、硫酸锌溶液、硝酸银溶液;
方案二:锌片、银片、硫酸铜溶液;
方案三:锌片、铜片、硫酸铜溶液、硝酸银溶液;
你的设计方案是______ 。
【进行实验】小华同学选用方案三进行如下探究,请你帮他完成表格中的空白(注:表格中实验操作一栏用文字描述或图示表示均可):
【解释与结论】根据上述实验,小华得出三种金属活动性由强到弱的顺序是______ 。
【反思与评价】探究活动结束后,同学们分享自己的收获与不足,并进行反思:
(4)有同学提出,小华的实验中不用硫酸铜溶液也能得到相同的实验结论,实验过程中选择金属用于反应的先后顺序说法正确的是______ 。
a、先锌片后铜片 b、先铜片后锌片 c、同时加入
(5)经过讨论,大家一致认为以上实验方案中,方案______ 较好。
(6)小于同学提出,试管中的金属可以回收再利用,这样做既能节约金属资源又能减少污染。
【拓展与延伸】好奇地小于同学在老师的指导下,把一定量的锌粒加入硫酸铜和硝酸银的混合溶液中,充分反应一段时间后,过滤,发现滤液呈无色。此时,滤渣中一定含有______ 。
第一组:小郝和小徐两位同学尝试着用镁条来验证金属的化学性质,两位同学的实验记录如下:
小郝:镁条灰黑色,不易点燃,放在白醋中反应很慢,较长时间以后才有气泡冒出。
小徐:镁条有银白色金属光泽,在空气中可以燃烧。在白醋中很快溶解并产生气泡,产生气泡的速率先是越来越快,后又变慢直至停止,且试管壁发烫。
已知:化学反应的剧烈程度与反应物的性质、反应物的浓度、温度、接触面积等因素有关。


(1)差异分析:你认为小郝同学在实验过程中缺少了哪一个步骤:
(2)小郝和小徐两位同学接着对镁条与白醋的反应进行了探究。将橡皮塞连接气体压力传感器,锥形瓶中放入一定量的镁条,针筒中放入白醋,塞紧瓶塞,将针筒中白醋推入锥形瓶并打开仪器(如图1所示)。一段时间后,得到气压压强与时间的关系曲线图(如图2所示)。到C点烧瓶内气压达到最大值说明
(3)从AB段到BC段来看,反应的速率是先慢后快,导致变快的主要因素是
a、镁条的表面积 b、白醋的浓度 c、温度
第二组:第2组同学来到实验室想对锌、铜、银三种金属活动性顺序进行探究。实验桌上老师提供的药品有:锌片、铜片、银片、硫酸锌溶液、硫酸铜溶液、硝酸银溶液和稀硫酸。
【制定计划】在老师的指导下,经过讨论,同学们设计出了以下几种实验方案:
方案一:铜片、硫酸锌溶液、硝酸银溶液;
方案二:锌片、银片、硫酸铜溶液;
方案三:锌片、铜片、硫酸铜溶液、硝酸银溶液;
你的设计方案是
【进行实验】小华同学选用方案三进行如下探究,请你帮他完成表格中的空白(注:表格中实验操作一栏用文字描述或图示表示均可):
| 实验操作 | 实验现象 | 分析与结论 |
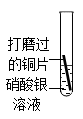 | 金属活动性:Cu (填“>”或“<”) | |
| 锌片表面附着一层红色物质,溶液由蓝色逐渐变为无色 | 金属活动性:Zn (填“>”或“<”),反应的化学方程式为 |
【解释与结论】根据上述实验,小华得出三种金属活动性由强到弱的顺序是
【反思与评价】探究活动结束后,同学们分享自己的收获与不足,并进行反思:
(4)有同学提出,小华的实验中不用硫酸铜溶液也能得到相同的实验结论,实验过程中选择金属用于反应的先后顺序说法正确的是
a、先锌片后铜片 b、先铜片后锌片 c、同时加入
(5)经过讨论,大家一致认为以上实验方案中,方案
(6)小于同学提出,试管中的金属可以回收再利用,这样做既能节约金属资源又能减少污染。
【拓展与延伸】好奇地小于同学在老师的指导下,把一定量的锌粒加入硫酸铜和硝酸银的混合溶液中,充分反应一段时间后,过滤,发现滤液呈无色。此时,滤渣中一定含有
20-21九年级上·江苏苏州·阶段练习
类题推荐
某同学对“21世纪的重要金属材料钛和钛合金”产生了兴趣,开展对钛金属与铁的活动性顺序、钛合金具有广泛用途的探究与讨论,设计并进行了如下探究,并请你一同参与:
(一)金属钛与铁的活动性顺序的探究:
(二)对物质性质决定其用途的讨论:
(1)钛是比较活泼的金属,为什么耐腐蚀性却很强?请你分析可能的原因是_____ :
(2)钛合金与人体具有很好的相容性,请你说明钛合金的用途有哪些?_____ 。
(一)金属钛与铁的活动性顺序的探究:
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量的钛金属放入试管中,加入硫酸亚铁溶液中, | 钛的表面有 | 钛的活动性顺序 |
(二)对物质性质决定其用途的讨论:
(1)钛是比较活泼的金属,为什么耐腐蚀性却很强?请你分析可能的原因是
(2)钛合金与人体具有很好的相容性,请你说明钛合金的用途有哪些?
M是生活中常见的金属,学习了金属的化学性质后,某化学兴趣小组的同学进行了下图M金属性质的相关实验。【查阅资料:MSO4溶液是无色液体】

【实验一】M、铜和铝的金属活动性顺序比较。
(1)如图1所示,甲组同学取M丝、铜丝、铝丝分别放入盛有体积和溶质质量分数均相同的稀硫酸中,实验记录如下表。
(2)同学们对同一实验出现两种不同的现象进行了讨论,实验刚开始时试管C中无气泡,是因为铝表面易形成一层致密的氧化膜,其形成的原因是______ (用化学方程式表示)。
【实验二】尝试从不同的角度探究三种金属的活动性顺序。乙组同学们取粗细相同,打磨干净的M丝,铝丝及相关溶液,进行了图2所示实验。
(3)打磨的目的是______ 。
(4)试管B中观察到的现象是______ 。
【拓展探究】在图2实验后,小桥同学将两支试管中的物质倒入同一废液缸中,充分反应后,将混合物过滤;得滤渣X和滤液Y,小桥同学对所得滤渣X和滤液Y的成分进行探究。
【实验探究】设计实验如图3所示,向滤液Y中插入M丝,观察到M丝表面无明显现象。
【评价交流】同组三位同学得出结论。
小强的结论:滤液Y中一定含Al2(SO4)3、MSO4和CuSO4
小虹的结论;滤液Y中一定含Al2(SO4)3,一定不含MSO4和CuSO4
小桥的结论:滤液Y中一定含Al2(SO4)3、可能含有MSO4,一定不含CuSO4
(5)你认为以上三位同学中,______ (填“小强”“小虹”或“小桥”)的结论是正确的。结合上述实验最终确定滤渣X中一定含有______ (填化学式)。

【实验一】M、铜和铝的金属活动性顺序比较。
(1)如图1所示,甲组同学取M丝、铜丝、铝丝分别放入盛有体积和溶质质量分数均相同的稀硫酸中,实验记录如下表。
实验操作 | M丝 | 铜丝 | 铝丝 | 实验结论 |
刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M、铜、铝的金属活动 性顺序是 |
几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 |
【实验二】尝试从不同的角度探究三种金属的活动性顺序。乙组同学们取粗细相同,打磨干净的M丝,铝丝及相关溶液,进行了图2所示实验。
(3)打磨的目的是
(4)试管B中观察到的现象是
【拓展探究】在图2实验后,小桥同学将两支试管中的物质倒入同一废液缸中,充分反应后,将混合物过滤;得滤渣X和滤液Y,小桥同学对所得滤渣X和滤液Y的成分进行探究。
【实验探究】设计实验如图3所示,向滤液Y中插入M丝,观察到M丝表面无明显现象。
【评价交流】同组三位同学得出结论。
小强的结论:滤液Y中一定含Al2(SO4)3、MSO4和CuSO4
小虹的结论;滤液Y中一定含Al2(SO4)3,一定不含MSO4和CuSO4
小桥的结论:滤液Y中一定含Al2(SO4)3、可能含有MSO4,一定不含CuSO4
(5)你认为以上三位同学中,
学习合金知识后,我们知道了黄铜是铜和锌的合金。在教师的引导下同学们分组对其性质进行了项目式探究。
【任务一】比较合金与纯金属的硬度
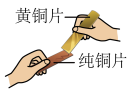
(1)将黄铜片与纯铜片相互刻画(如图),观察到铜片上划痕较深,黄铜片上划痕较浅,据此得出的结论是__________ 。
【任务二】比较黄铜中锌和铜的金属活动性强弱
【查阅资料】锌是银白色有光泽的金属,在空气中,像铝一样,其表面能产生致密的氧化膜。各小组分别设计了如下实验:
(2)比较__________ 两组同学的实验,可以得出打磨能破坏氧化锌薄膜。
(3)乙组同学的实验中发生反应的化学方程式为__________ ,据此可知金属活动性Zn_______ (选填“>”或“<”)Cu。
(4)丙组同学的实验现象引起了大家的讨论。下列是小林同学进行的分析,你认为下列分析合理的是______ (填字母)。
A.H2O破坏了氧化锌薄膜 B.C1-破坏了氧化锌薄膜
C.Cu2+破坏了氧化锌薄膜 D. 破坏了氧化锌薄膜
破坏了氧化锌薄膜
【任务三】比较锌、铜与稀硫酸的反应
(5)小组同学将锌片和铜片分别浸入相同质量、相同质量分数的稀硫酸中。观察到铜片表面无明显现象发生;一段时间后锌片的表面产生大量气泡,氢气的产生速度与反应时间的关系如图所示。
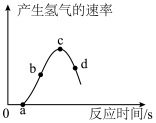
①图中O~a段未产生气体的原因是__________ 。
②b点所对应溶液的pH__________ (选填“大于”、“等于”或“小于”)7.
③c~d段产生氢气的速率下降的主要原因是__________ 。
【任务一】比较合金与纯金属的硬度
(1)将黄铜片与纯铜片相互刻画(如图),观察到铜片上划痕较深,黄铜片上划痕较浅,据此得出的结论是

【任务二】比较黄铜中锌和铜的金属活动性强弱
【查阅资料】锌是银白色有光泽的金属,在空气中,像铝一样,其表面能产生致密的氧化膜。各小组分别设计了如下实验:
| 实验小组 | 实验操作 | 实验现象 |
| 甲 | 将表面未打磨的锌片浸入CuSO4溶液中 | 无明显现象 |
| 乙 | 将表面打磨后的锌片浸入CuSO4溶液中 | 锌片表面析出红色固体 |
| 丙 | 将表面未打磨的锌片浸入CuC12溶液中 | 锌片表面析出红色固体 |
(3)乙组同学的实验中发生反应的化学方程式为
(4)丙组同学的实验现象引起了大家的讨论。下列是小林同学进行的分析,你认为下列分析合理的是
A.H2O破坏了氧化锌薄膜 B.C1-破坏了氧化锌薄膜
C.Cu2+破坏了氧化锌薄膜 D.
【任务三】比较锌、铜与稀硫酸的反应
(5)小组同学将锌片和铜片分别浸入相同质量、相同质量分数的稀硫酸中。观察到铜片表面无明显现象发生;一段时间后锌片的表面产生大量气泡,氢气的产生速度与反应时间的关系如图所示。

①图中O~a段未产生气体的原因是
②b点所对应溶液的pH
③c~d段产生氢气的速率下降的主要原因是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


