填空与简答-流程题 适中0.65 引用2 组卷219
海水中含有氯化钠、氯化钙等物质,下面是从海水中提取氯化钠的大致过程(如图1)和氯化钠、氯化钙的溶解度表与溶解度曲线。
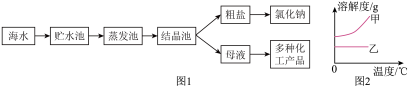
请回答下列问题:
(1)将粗盐从海水中结晶出来的方法是_____ 。
(2)经长时间日晒,氯化钙也不易大量结晶析出的原因是_____ ,40℃时,50g水中最多溶解氯化钙_____ g。
(3)根据海水晒盐的原理,下列说法中正确的是_____ (填序号)。
A 海水进入贮水池,海水的成分基本不变
B 在蒸发池里,海水中水的质量逐渐增加
C 析出晶体后的母液是氯化钠的不饱和溶液
(4)如图2溶解度曲线图中,能表示氯化钙溶解度曲线的是_____ (填“甲”或“乙”)。

| 温度/C | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 128 | |
(1)将粗盐从海水中结晶出来的方法是
(2)经长时间日晒,氯化钙也不易大量结晶析出的原因是
(3)根据海水晒盐的原理,下列说法中正确的是
A 海水进入贮水池,海水的成分基本不变
B 在蒸发池里,海水中水的质量逐渐增加
C 析出晶体后的母液是氯化钠的不饱和溶液
(4)如图2溶解度曲线图中,能表示氯化钙溶解度曲线的是
20-21九年级下·全国·课时练习
类题推荐
食盐是生活和工农业生产中最常见的物质之一。晒盐场利用晾晒海水得到粗盐和卤水。
(1)去除粗盐中难溶性的杂质,主要步骤有:溶解、过滤、_________ ;在过滤操作中,玻璃棒的作用是___________ 。
(2)在20℃时,向4个盛有200g水的烧杯中,分别加入一定质量的纯净氯化钠固体,并充分搅拌,4组实验数据记录如下
以下是关于上述实验的叙述,正确的是_______________ (填写序号)。
A ①②所得溶液是不饱和溶液
B ③④所得溶液中,溶质的质量分数相等
C 20℃时,200g水中最多可溶解氯化钠的质量为72g
D 20℃时,将④继续恒温蒸发100g水,过滤,得到36g的固体
(3)卤水的主要成分及其溶解度曲线如图,t1℃时:
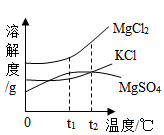
将3种图中物质的饱和溶液升温到t2℃,3种溶液溶质的质量分数由小到大的顺序是___ 。
(1)去除粗盐中难溶性的杂质,主要步骤有:溶解、过滤、
(2)在20℃时,向4个盛有200g水的烧杯中,分别加入一定质量的纯净氯化钠固体,并充分搅拌,4组实验数据记录如下
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
| 所得溶液的质量/g | 209 | 236 | 272 | 272 |
以下是关于上述实验的叙述,正确的是
A ①②所得溶液是不饱和溶液
B ③④所得溶液中,溶质的质量分数相等
C 20℃时,200g水中最多可溶解氯化钠的质量为72g
D 20℃时,将④继续恒温蒸发100g水,过滤,得到36g的固体
(3)卤水的主要成分及其溶解度曲线如图,t1℃时:

将3种图中物质的饱和溶液升温到t2℃,3种溶液溶质的质量分数由小到大的顺序是
无水氯化钙是一种用途广泛的干燥剂。某工业副产品氯化钙中含有的杂质主要是MgSO4和CaCO3,从工业副产品氯化钙中提纯氯化钙生产流程如图所示。试分析流程,回答以下问题。

(1)操作1的名称为________ 。
(2)在以上流程中,加入盐酸、BaCl2溶液和Ca(OH)2溶液应当_______ (选填“少量”或“过量”),其中加入氯化钡溶液可除去的杂质离子是______ ,该反应的化学方程式为________ 。
(3)下表是CaCl2和BaCl2在不同温度时的溶解度。为提高析出CaCl2晶体产品的纯度,操作2为_____ (选填“降温结晶”或“蒸发结晶”)。

(1)操作1的名称为
(2)在以上流程中,加入盐酸、BaCl2溶液和Ca(OH)2溶液应当
(3)下表是CaCl2和BaCl2在不同温度时的溶解度。为提高析出CaCl2晶体产品的纯度,操作2为
| 温度/℃ | 0 | 20 | 35 | 80 | 100 | |
| 溶解度/g | B aCl2 | 31.6 | 35.7 | 39.4 | 52.4 | 59.4 |
| CaCl2 | 59.5 | 74.4 | 109.5 | 147 | 159 | |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



