科学探究题 较难0.4 引用1 组卷213
学习兴趣小组对贝壳中碳酸钙的含量进行探究。
【提出问题】如何选择药品和设计装置进行测定?
【查阅资料】1贝壳的主要成分是CaCO3,其它成分对实验影响忽略不计。
2室温时碳酸钙和硫酸反应生成硫酸钙、水和二氧化碳。
3硫酸钙微溶于水,会覆盖在碳酸钙表面,阻止反应进一步的进行。
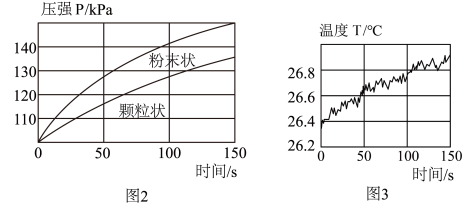
【设计与实验】实验一:选择药品。分别取等质量颗粒状和粉末状的贝壳样品与等体积、等浓度的稀盐酸在图1的三颈烧瓶中反应,采集数据。

(1)图1中反应的符号表达式是_____________ 。
(2)据图2分析,_____________ 对反应程度有影响。
(3)据图3分析,碳酸钙和盐酸反应的能量变化是_____________ (填放热或吸热)反应。
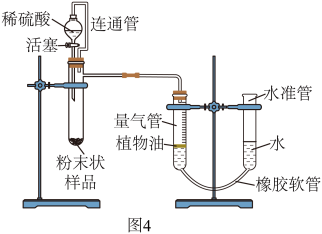
实验二:设计装置。小组设计了图4装置进行测定。
(4)图4中连通管的作用是_____________ (写出一点即可)。打开活塞,稀硫酸进入试管,观察到的现象有试管内产生气泡,_____________ 。反应结束后调平液面后再进行读数,若不调平就读数,则结果___________ (填偏大、偏小或不变)。
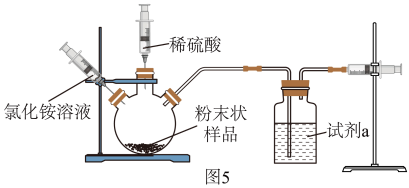
实验三:优化装置。在老师指导下,小组优化并设计了图5装置进行测定。
(5)该小组同学连接好装置后将右侧注射器向右拉,松手后,发现注射器回到原位,该操作的目的是_____________ 。
(6)已知a中的试剂是浓硫酸,浓硫酸有吸水性,如果没有a装置,测定结果会_____________ (填偏大、偏小或不变)。
(7)加入足量稀硫酸,一段时间后反应停止。再加入氯化铵溶液,发现又产生气泡,推测加入氯化铵的作用是_____________ 。
【数据处理】记录加入样品质量、加入稀硫酸体积、加入氯化铵体积、右侧针筒读数,对实验数据进行处理,测得碳酸钙的质量分数。
【反思与评价】
(8)与实验二相比,实验三的优点是_____________ 。
【提出问题】如何选择药品和设计装置进行测定?
【查阅资料】1贝壳的主要成分是CaCO3,其它成分对实验影响忽略不计。
2室温时碳酸钙和硫酸反应生成硫酸钙、水和二氧化碳。
3硫酸钙微溶于水,会覆盖在碳酸钙表面,阻止反应进一步的进行。
【设计与实验】实验一:选择药品。分别取等质量颗粒状和粉末状的贝壳样品与等体积、等浓度的稀盐酸在图1的三颈烧瓶中反应,采集数据。

(1)图1中反应的符号表达式是
(2)据图2分析,
(3)据图3分析,碳酸钙和盐酸反应的能量变化是

实验二:设计装置。小组设计了图4装置进行测定。
(4)图4中连通管的作用是


实验三:优化装置。在老师指导下,小组优化并设计了图5装置进行测定。
(5)该小组同学连接好装置后将右侧注射器向右拉,松手后,发现注射器回到原位,该操作的目的是
(6)已知a中的试剂是浓硫酸,浓硫酸有吸水性,如果没有a装置,测定结果会
(7)加入足量稀硫酸,一段时间后反应停止。再加入氯化铵溶液,发现又产生气泡,推测加入氯化铵的作用是
【数据处理】记录加入样品质量、加入稀硫酸体积、加入氯化铵体积、右侧针筒读数,对实验数据进行处理,测得碳酸钙的质量分数。
【反思与评价】
(8)与实验二相比,实验三的优点是
20-21九年级上·江苏常州·期中
类题推荐
其兴趣小组同学在老师的指导下,进入实验室对碳酸钙进行了一系列探究。回答下列问题:

Ⅰ.碳酸钙与盐酸反应
(1)装置A中仪器a的名称为_____ 。
(2)装置B中的现象是_____ 。
(3)装置C若用于检验生成的气体,其中试剂为_____ (写名称),发生反应的化学方程式为 _____ 。
Ⅱ.碳酸钙分解
碳酸钙在电炉中高温煅烧一段时间后,对剩余固体进行探究。
【提出问题】剩余固体成分是什么?
【猜想与假设】猜想一:全部是碳酸钙
猜想二:是碳酸钙和氧化钙的混合物
猜想三:全部是氧化钙
【设计并完成实验】
【实验结论】正确的猜想是 _____ 。
【交流与反思】小芳同学认为,步骤二中还可滴加其他试剂用来替代氯化铜溶液,该试剂可以是_____ (写一种即可);小华同学认为,只需完成步骤一和步骤三即可获得相同实验结论,他的依据是 _____ 。
【拓展与分析】查阅资料:生石灰质量的优劣常采用“活性度”来衡量。“活性度”的测定方法:取一定质量的生石灰,加入一定量的水,用一定溶质质量分数的盐酸中和,记录所消耗盐酸的体积(单位为mL)。消耗盐酸的体积数越大,“活性度”越高。
测得煅烧产物(CaO)的活性度,数据见如表。
石灰石煅烧的最佳温度范围一般为1100℃~1200℃的证据是 _____ 。

Ⅰ.碳酸钙与盐酸反应
(1)装置A中仪器a的名称为
(2)装置B中的现象是
(3)装置C若用于检验生成的气体,其中试剂为
Ⅱ.碳酸钙分解
碳酸钙在电炉中高温煅烧一段时间后,对剩余固体进行探究。
【提出问题】剩余固体成分是什么?
【猜想与假设】猜想一:全部是碳酸钙
猜想二:是碳酸钙和氧化钙的混合物
猜想三:全部是氧化钙
【设计并完成实验】
| 实验操作 | 实验现象 | 解释与结论 |
| 步骤一:取剩余固体于试管中,加水振荡后静置 | 底部有白色不溶物 | \ |
| 步骤二:取上层清液于另一试管中,滴加氯化铜溶液 | 有 | 上层清液中一定含有氢氧化钙 |
| 步骤三:取部分底部白色不溶物于第三支试管中,滴加过量稀盐酸 | 有气泡产生 | 白色不溶物中一定含有 |
【交流与反思】小芳同学认为,步骤二中还可滴加其他试剂用来替代氯化铜溶液,该试剂可以是
【拓展与分析】查阅资料:生石灰质量的优劣常采用“活性度”来衡量。“活性度”的测定方法:取一定质量的生石灰,加入一定量的水,用一定溶质质量分数的盐酸中和,记录所消耗盐酸的体积(单位为mL)。消耗盐酸的体积数越大,“活性度”越高。
测得煅烧产物(CaO)的活性度,数据见如表。
| 煅烧温度 活性度煅烧时间 | 1050℃ | 1100℃ | 1150℃ | 1200℃ | 1250℃ | 1300℃ |
| 12 min | 790 | 836 | 868 | 808 | 454 | 412 |
| 16 min | 793 | 856 | 871 | 845 | 556 | 530 |
| 20 min | 795 | 863 | 873 | 864 | 617 | 623 |
【科学探究】
很多同学都喜欢既别致又实用的“树叶书签”,实验小组尝试制作了书签,并对该制作过程及所用试剂进行了研究。

Ⅰ.制作“树叶书签”
小组同学首先选取了大小适当的树叶,洗净后放在一定浓度的氢氧化钠溶液中煮沸,再加以处理,除去表皮和叶肉,只剩余清晰的叶脉,取出,冲洗,将叶片压平,最后系上各色丝带,漂亮的“叶脉书签”便做好了。
(1)小组同学用如图所示的装置煮沸树叶,指出其中的一处错误:_____ 。
Ⅱ.探究制作“叶脉书签”的最佳条件
【实验1】相同煮沸时间内,将洗干净的树叶放在不同浓度的氢氧化钠溶液里,处理后叶片变化如下表。
【实验2】在10%的氢氧化钠溶液里,将洗干净的树叶在不同温度下,进行煮沸,随着时间的变化,叶片变化如下表。
(2)实验小组同学选择了10%的氢氧化钠溶液制作“叶脉书签”,原因是_____ 。
(3)通过实验2可知,制作“叶脉书签”的最佳加热的温度和时间是_____ (写一种即可)。
Ⅲ.小组同学发现所用的氢氧化钠溶液瓶口有白色固体出现,这瓶溶液中的溶质只有氢氧化钠吗?同学们展开了下面的探究:
(4)氢氧化钠溶液放置在空气中可能发生的反应的化学方程式为_____ 。
同学们经过思考、讨论,分别设计了以下两个实验方案:
方案Ⅰ:打开瓶塞,取出少量溶液,并向其中加入少量稀盐酸,若未观察到有气泡产生,证明溶液没有变质。
方案Ⅱ:打开瓶塞,取出少量溶液,并向其中加入CaCl2溶液,若未观察到有白色沉淀产生,证明溶液没有变质。
(5)你认为上述实验方案不可行的是_____ ,理由是_____ 。
(6)同学们利用可行的方案进行实验,检验出该氢氧化钠溶液确实已变质,提出使用或保存氢氧化钠溶液的注意事项:_____ (写出一点即可)。
很多同学都喜欢既别致又实用的“树叶书签”,实验小组尝试制作了书签,并对该制作过程及所用试剂进行了研究。

Ⅰ.制作“树叶书签”
小组同学首先选取了大小适当的树叶,洗净后放在一定浓度的氢氧化钠溶液中煮沸,再加以处理,除去表皮和叶肉,只剩余清晰的叶脉,取出,冲洗,将叶片压平,最后系上各色丝带,漂亮的“叶脉书签”便做好了。
(1)小组同学用如图所示的装置煮沸树叶,指出其中的一处错误:
Ⅱ.探究制作“叶脉书签”的最佳条件
【实验1】相同煮沸时间内,将洗干净的树叶放在不同浓度的氢氧化钠溶液里,处理后叶片变化如下表。
| NaOH溶液浓度 | 1% | 5% | 10% |
| 叶片变化 | 留有很多叶肉 | 留有较多叶肉 | 残留很少叶肉 |
【实验2】在10%的氢氧化钠溶液里,将洗干净的树叶在不同温度下,进行煮沸,随着时间的变化,叶片变化如下表。
| 时间 叶片变化 温度 | 5min | 15min | 20min |
| 60℃ | 无明显变化 | 留有较多叶肉 | 留有少量叶肉 |
| 80℃ | 留有较多叶肉 | 留有少量叶肉 | 残留很少叶肉 |
| 100℃ | 留有较多叶肉 | 残留很少叶肉 | 叶片卷起来,叶肉与叶脉不易分离 |
(2)实验小组同学选择了10%的氢氧化钠溶液制作“叶脉书签”,原因是
(3)通过实验2可知,制作“叶脉书签”的最佳加热的温度和时间是
Ⅲ.小组同学发现所用的氢氧化钠溶液瓶口有白色固体出现,这瓶溶液中的溶质只有氢氧化钠吗?同学们展开了下面的探究:
(4)氢氧化钠溶液放置在空气中可能发生的反应的化学方程式为
同学们经过思考、讨论,分别设计了以下两个实验方案:
方案Ⅰ:打开瓶塞,取出少量溶液,并向其中加入少量稀盐酸,若未观察到有气泡产生,证明溶液没有变质。
方案Ⅱ:打开瓶塞,取出少量溶液,并向其中加入CaCl2溶液,若未观察到有白色沉淀产生,证明溶液没有变质。
(5)你认为上述实验方案不可行的是
(6)同学们利用可行的方案进行实验,检验出该氢氧化钠溶液确实已变质,提出使用或保存氢氧化钠溶液的注意事项:
某化学实验小组用石灰石与稀盐酸反应制取二氧化碳。
【反应原理】(1)反应的化学方程式为______ 。
【提出问题】影响石灰石与稀盐酸反应速率的因素有哪些?
【猜想】影响石灰石与稀盐酸反应的速率可能有:盐酸的浓度、石灰石的颗粒大小等。
【进行实验】室温下,选用20mL不同浓度的盐酸与1g石灰石进行实验(装置如图所示)。

【处理数据】实验后获得的相关实验数据如表:
(2)要比较不同浓度的盐酸对反应速率的影响,应选择的实验编号是______ (写1组),由此得到的结论是______ 。
(3)从上述实验中得出石灰石的颗粒大小对反应速率影响的结论是:石灰石的颗粒越小,反应速率越______ (填“快”或“慢”)。
【实验延伸】表是记录生成二氧化碳气体体积和对应的时间的一组实验数据(每间隔4s
读数一次):
(4)从上表数据可以分析得出,到20s后反应速率逐渐变______ (填“快”或“慢”),其主要原因是______ 。
【反应原理】(1)反应的化学方程式为
【提出问题】影响石灰石与稀盐酸反应速率的因素有哪些?
【猜想】影响石灰石与稀盐酸反应的速率可能有:盐酸的浓度、石灰石的颗粒大小等。
【进行实验】室温下,选用20mL不同浓度的盐酸与1g石灰石进行实验(装置如图所示)。

【处理数据】实验后获得的相关实验数据如表:
| 实验 编号 | 盐酸的浓度 (均取20mL) | 石灰石固体形状 (均取1g) | 二氧化碳体积(mL) (均收集前30s的气体) |
| 甲 | 4% | 粉末状 | 64.0 |
| 乙 | 4% | 块状 | 40.4 |
| 丙 | 6% | 粉末状 | 98.2 |
| 丁 | 6% | 块状 | 65.3 |
(3)从上述实验中得出石灰石的颗粒大小对反应速率影响的结论是:石灰石的颗粒越小,反应速率越
【实验延伸】表是记录生成二氧化碳气体体积和对应的时间的一组实验数据(每间隔4s
读数一次):
| 时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
| CO2体积/mL | 16 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62 | 64.7 | 66 | 66 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


