科学探究题 较难0.4 引用1 组卷138
兴趣小组想深入探究人体呼出气体的成分,进行如下活动:

【活动一】探究人体呼出气体中是否含有CO2
向装有呼出气体的集气瓶中滴加少量澄清石灰水,振荡后观察到__________ 。
结论:人体呼出气体中含有CO2。
【活动二】探究人体呼出气体中CO2的体积分数(已知:CO2能与NaOH反应)
兴趣小组同学用图1所示装置进行实验。(锥形瓶内充满人体呼出的气体)实验前注射器内液体体积为50mL,向锥形瓶内注入少量液体后,注射器内的液体开始被自动吸入锥形瓶,完全反应后,注射器内NaOH溶液的体积为30mL。
结论:人体呼出气体中CO2的体积分数为__________ 。
【活动三】探究人体呼出气体中O2的体积分数
兴趣小组同学用图2所示装置进行实验。(注射器及玻璃管内充满人体呼出的气体)
1实验中需反复推拉注射器的目的是____________ ;
2在操作中如何判断装置中的O2是否反应完?__________ 。
结论:人体呼出气体中O2的体积分数为16%。
【实验反思】①活动三所用方法与教科书上“测定空气里O2的含量”的方法相比,优点是:_________ (答一点即可)。
②小组同学准确测量人体呼吸前后气体的体积分数如下表所示:
你认为呼吸过程中,氮气含量减少的原因是__________ 。

【活动一】探究人体呼出气体中是否含有CO2
向装有呼出气体的集气瓶中滴加少量澄清石灰水,振荡后观察到
结论:人体呼出气体中含有CO2。
【活动二】探究人体呼出气体中CO2的体积分数(已知:CO2能与NaOH反应)
兴趣小组同学用图1所示装置进行实验。(锥形瓶内充满人体呼出的气体)实验前注射器内液体体积为50mL,向锥形瓶内注入少量液体后,注射器内的液体开始被自动吸入锥形瓶,完全反应后,注射器内NaOH溶液的体积为30mL。
结论:人体呼出气体中CO2的体积分数为
【活动三】探究人体呼出气体中O2的体积分数
兴趣小组同学用图2所示装置进行实验。(注射器及玻璃管内充满人体呼出的气体)
1实验中需反复推拉注射器的目的是
2在操作中如何判断装置中的O2是否反应完?
结论:人体呼出气体中O2的体积分数为16%。
【实验反思】①活动三所用方法与教科书上“测定空气里O2的含量”的方法相比,优点是:
②小组同学准确测量人体呼吸前后气体的体积分数如下表所示:
| 氮气 | 氧气 | 二氧化碳 | 水 | 其他 | |
| 呼入气体 | 78% | 21% | 0.03% | 0.06% | 0.91% |
| 呼出气体 | 75% | 15% | 3.68% | 5.44% | 0.88% |
20-21九年级上·安徽六安·期中
类题推荐
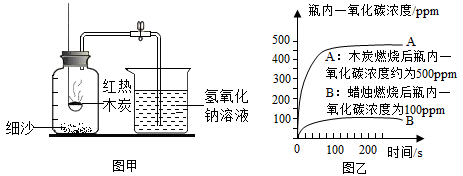
某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于1/5。
(1)教材中利用燃烧红磷法测定空气中氧气体积分数,选择该药品的原因是___________ ;
【提出问题】是什么原因导致测量不准确呢?
【猜想与假设】他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为____ 同学的猜想不合理.
【查阅资料】
①木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%;
②一氧化碳不能被氢氧化钠溶液吸收;
乙同学又利用上述装置设计了如下实验,请你横线上填空。
【交流与反思】
(2)丙同学使用了一氧化碳浓度传感器测得木炭、蜡烛分别在密闭集气瓶里燃烧停止后,瓶内一氧化碳的浓度变化曲线如图乙。根据此曲线图分析用上述装置不能准确测出氧气体积分数的原因是_________ ;

(1)教材中利用燃烧红磷法测定空气中氧气体积分数,选择该药品的原因是
【提出问题】是什么原因导致测量不准确呢?
【猜想与假设】他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为
【查阅资料】
①木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%;
②一氧化碳不能被氢氧化钠溶液吸收;
乙同学又利用上述装置设计了如下实验,请你横线上填空。
| 实验步骤 | 实验现象 | 实验结论 |
| 1.将足量木炭点燃,迅速插入集气瓶中 | / | 木炭燃烧没有消耗完集气瓶中的氧气 |
| 2.待冷却后,将燃着的 |
【交流与反思】
(2)丙同学使用了一氧化碳浓度传感器测得木炭、蜡烛分别在密闭集气瓶里燃烧停止后,瓶内一氧化碳的浓度变化曲线如图乙。根据此曲线图分析用上述装置不能准确测出氧气体积分数的原因是
“富氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗、炼钢等。某化学小组欲混制“富氧空气”并开展相关探究。
实验一:混制“富氧空气”
(1)用高锰酸钾制取氧气,反应的化学式表达式为______ 。将制取的氧气及一定体积纯氮气混合制100mL“富氧空气”。
实验二:测定“富氧空气”中氧气的含量
实验装置如图(集气瓶中“富氧空气”体积为100mL,底部留有少量水,燃烧匙内红磷足量)。操作如下:
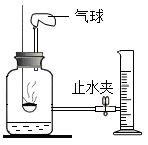
①往量筒内加入适量水,读出量筒内水的体积为80mL:
②用电点火装置点燃红磷,充分反应:
③打开止水夹,最终读出量筒内水的体积为38mL。
回答下列问题:
(2)本次实验测得“富氧空气”中氧气的含量为______ 。
(3)气球在实验中的作用______ 。
(4)若操作③量筒读数时俯视,则测得氧气的含量______ (选填“偏大”、“偏小”或“无影响”)。
实验三:研究“富氧空气”的应用
通过重油、褐煤在氧气含量不同的空气中燃烧的实验,得到有关数据如下图:

(5)结合图1,说明空气中氧气含量与燃烧产生的温度的关系______ 。
(6)结合图2,简述减少燃料燃烧尾气污染的措施______ 。
实验四:空气中氧气含量的再探究
(7)小组同学想探究用不同物质在空气中燃烧测定氧气含量方法的优劣。他们用足量的蜡烛、红磷和白磷分别在相同体积与状态的空气中燃烧,用氧气探测器测定容器中剩余氧气与时间的关系如下图。下列说法正确的是______。

实验一:混制“富氧空气”
(1)用高锰酸钾制取氧气,反应的化学式表达式为
实验二:测定“富氧空气”中氧气的含量
实验装置如图(集气瓶中“富氧空气”体积为100mL,底部留有少量水,燃烧匙内红磷足量)。操作如下:

①往量筒内加入适量水,读出量筒内水的体积为80mL:
②用电点火装置点燃红磷,充分反应:
③打开止水夹,最终读出量筒内水的体积为38mL。
回答下列问题:
(2)本次实验测得“富氧空气”中氧气的含量为
(3)气球在实验中的作用
(4)若操作③量筒读数时俯视,则测得氧气的含量
实验三:研究“富氧空气”的应用
通过重油、褐煤在氧气含量不同的空气中燃烧的实验,得到有关数据如下图:

(5)结合图1,说明空气中氧气含量与燃烧产生的温度的关系
(6)结合图2,简述减少燃料燃烧尾气污染的措施
实验四:空气中氧气含量的再探究
(7)小组同学想探究用不同物质在空气中燃烧测定氧气含量方法的优劣。他们用足量的蜡烛、红磷和白磷分别在相同体积与状态的空气中燃烧,用氧气探测器测定容器中剩余氧气与时间的关系如下图。下列说法正确的是______。

| A.三个实验效果最好的是蜡烛,因为它反应速率最快 |
| B.三个实验效果最好的是红磷,因为它消耗氧气最彻底 |
| C.三种物质中,白磷能在更低浓度的氧气中燃烧 |
| D.若用这三种物质做实验,测得空气中氧气含量偏高 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



