科学探究题 较难0.4 引用1 组卷71
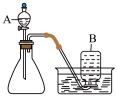
通过课后查阅资料后并在老师的指导下,小丽和小明利用如图1所示装置对氯酸钾制氧气进行了深入的探究学习。
【查阅资料】
①氯酸钾的熔点约为356℃,二氧化锰的分解温度约为535℃,用酒精灯给物质加热,受热物质的温度一般约为400℃左右;
②不同配比是指氯酸钾和二氧化锰混合物中,氯酸钾和二氧化锰的质量比;
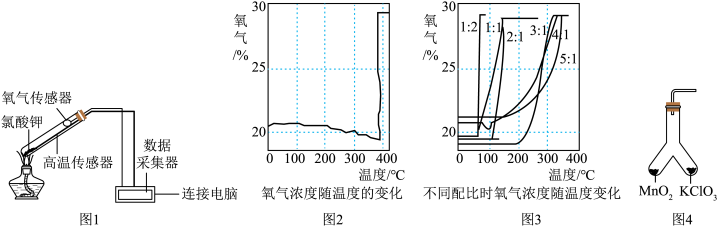
③氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图(图2)及不同配比时氧气浓度随温度的变化示意图(图3)如下:
请回答问题
(1)分析图2,氯酸钾分解温度_____ (填“高于”、“等于”或“低于”)其熔点。
(2)根据资料和分析图2,加热氯酸钾时,在图1中的试管口向上的可能原因是_________ 。
(3)分析图3,氯酸钾分解温度随物质配比变化的规律是_________ ,当物质配比为_____ 时,氯酸钾分解温度约为75℃。
(4)为证实二氧化锰的催化作用,小华利用如图4装置进行如表所示的实验:
请回答:
①完善步骤Ⅲ中的填空:加热左侧支管,可观察到______ ,加热右侧支管,可观察到________ 。
②氯酸钾制取氧气的符号表达式_______ 。小华认为根据步骤Ⅳ的实验现象就能说明二氧化锰是氯酸钾分解的催化剂,但小明不同意她的观点,小明认为还需证明在此反应中二氧化锰的___________ 不变。后来在老师的指导下,小华完善了实验方案,最终验证了自己的结论。
【查阅资料】
①氯酸钾的熔点约为356℃,二氧化锰的分解温度约为535℃,用酒精灯给物质加热,受热物质的温度一般约为400℃左右;
②不同配比是指氯酸钾和二氧化锰混合物中,氯酸钾和二氧化锰的质量比;
③氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图(图2)及不同配比时氧气浓度随温度的变化示意图(图3)如下:

请回答问题
(1)分析图2,氯酸钾分解温度
(2)根据资料和分析图2,加热氯酸钾时,在图1中的试管口向上的可能原因是
(3)分析图3,氯酸钾分解温度随物质配比变化的规律是
(4)为证实二氧化锰的催化作用,小华利用如图4装置进行如表所示的实验:
| 步骤 | 实验操作 | 实验现象 |
| Ⅰ | 检查气密性。 | |
| Ⅱ | 分别在“Y”形管两侧支管中加入少量二氧化锰和氯酸钾,塞紧橡皮塞。 | |
| Ⅲ | 分别用酒精灯先后加热二氧化锰和氯酸钾,用带火星木条放在导管口 | 加热左侧支管,观察现象___,加热右侧支管,观察现象____ |
| Ⅳ | 冷却后,将“Y”形管左侧支管中部分二氧化锰混入右侧支管中,振荡“Y”形管,加热右侧支管,用带火星木条放在导管口。 | 加热时间短于步骤Ⅲ,木条很快复燃 |
①完善步骤Ⅲ中的填空:加热左侧支管,可观察到
②氯酸钾制取氧气的符号表达式
20-21九年级上·江苏无锡·期中
类题推荐
在过氧化氢溶液的分解反应中,二氧化碳能作催化剂.下列有关催化剂的说法正确的是 _____ (填序号)
A.在化学反应后其质量减小
B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量
D.能改变化学反应速率
某化学化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想在探究其他的一些物质是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白。
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。
【实验验证】
【得出结论】氧化铜能作过氧化氢分解的催化剂。
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铜能作过氧化氢分解的催化剂,还要补充一个探究实验三:
【实验三目的】探究氧化铜在反应前后质量是否改变。
【实验步骤】①准确称量氧化铜(少量)的质量;
②完成实验二;
③待反应结束,将实验二试管里的物质进行过滤,洗涤,___________ ,称量;在过滤实验中使用的玻璃棒一起有烧杯、玻璃棒、 ____________
④对比反应前后氧化铜的质量。
【交流讨论】如果在反应前后氧化铜质量___________ ,则说明氧化铜可以作过氧化氢分解的催化剂。
【提出新的问题】但还有同学认为,要证明氧化铜能作过氧化氢分解的催化剂,上述三个实验还不够准确,还需要再增加一个探究实验四:
【实验四目的】探究________________ 。
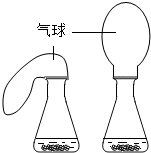
【拓展探究】同学们对二氧化锰和氧化铜对过氧化氢溶液分解的催化作用能力做了更深入的探究,设计如下四组实验进行比较,其中观察效果最差的是___________ (选填序号)
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
A.在化学反应后其质量减小
B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量
D.能改变化学反应速率
某化学化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想在探究其他的一些物质是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白。
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铜,然后将带火星的木条伸入试管中 |
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铜能作过氧化氢分解的催化剂,还要补充一个探究实验三:
【实验三目的】探究氧化铜在反应前后质量是否改变。
【实验步骤】①准确称量氧化铜(少量)的质量;
②完成实验二;
③待反应结束,将实验二试管里的物质进行过滤,洗涤,
④对比反应前后氧化铜的质量。
【交流讨论】如果在反应前后氧化铜质量
【提出新的问题】但还有同学认为,要证明氧化铜能作过氧化氢分解的催化剂,上述三个实验还不够准确,还需要再增加一个探究实验四:
【实验四目的】探究
【拓展探究】同学们对二氧化锰和氧化铜对过氧化氢溶液分解的催化作用能力做了更深入的探究,设计如下四组实验进行比较,其中观察效果最差的是
 |  |  |  |
| 第一组 | 第二组 | 第三组 | 第四组 |
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
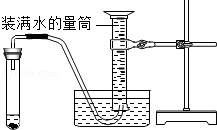
用下列微型实验进行实验探究,请你完成有关实验内容。
【实验反思】
(1)对于步骤1,下列说法正确的是__________ (选填编号)。
A.MnO2加快反应速率 B.MnO2质量和化学性质在反应前后没有改变
C.MnO2一定分解产生气体 D.反应过程中球形II比球形III内产生的气体多
(2)步骤4的结论不正确,你的理由是___________ 。
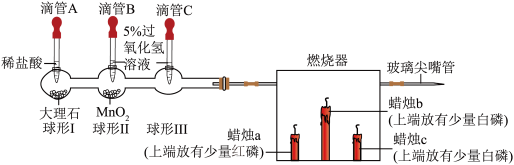
| 实验步骤 | 实验现象 | 结论或分析 |
| 1.同时挤压滴管B和C,控制相同量液体滴于球形容器中。 | ①球形Ⅱ ②蜡烛a、b、c都不燃烧。 | 球形Ⅱ反应的化学方程式是 |
| 2.微热燃烧器至50℃。 | 蜡烛b、c燃烧,a不燃烧。 | a不燃烧的原因是 |
| 3.挤压滴管A,将足量稀盐酸滴于球形I中。 | ①球形Ⅰ中有气泡放出。 ②一段时间后, | 球形Ⅰ产生的气体具有的化学性质是 |
| 4.熄灭蜡烛,将涂有澄清石灰水的小烧杯罩住玻璃尖嘴管。 | 烧杯内壁的石灰水变浑浊。 | 证明蜡烛一定含有碳元素。 |
(1)对于步骤1,下列说法正确的是
A.MnO2加快反应速率 B.MnO2质量和化学性质在反应前后没有改变
C.MnO2一定分解产生气体 D.反应过程中球形II比球形III内产生的气体多
(2)步骤4的结论不正确,你的理由是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网