科学探究题 较难0.4 引用1 组卷55
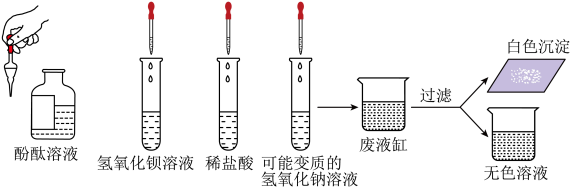
在实验室有失去标签的五瓶药品,分别是硫酸铜、碳酸钙、碳酸钠、氢氧化钠、氢氧化钙五种物质(均为纯净物),它们均为白色粉末。现将药品分别标记为A、B、C、D、E,某校化学实验小组的同学们积极思考,利用所学知识设计实验,对这些物质进行鉴别。
【查阅资料】白色的硫酸铜粉末遇水变为蓝色
【实验探究】化学实验小组的同学鉴别实验过程记录如下:
步骤1:取五种白色粉末各一药匙,分别放入五支洁净的试管中,各加蒸馏水2mL,充分振荡后静置。五支试管底部均有固体存在,只有盛放E的试管中液体呈蓝色,其他均呈无色。
步骤2:取B、C、D上层清液滴加稀盐酸,只有B的试管中有气泡产生,其他无明显现象。
步骤3:取A、C、D的上层清液放入试管中,分别滴加无色酚酞,A、C显红色。
请根据该学生的实验过程,回答下列问题:
(1)由步骤1可知E为________ (填化学式);
(2)步骤3中,D的现象是_________ ;
(3)通过上述步骤,除E外,该化学小组的同学还推断出的是B为________ (填化学式,下同)、D为________ ;
(4)对尚未鉴别出来的物质,同学设计了实验进行确定,请将如表补充完整:
【查阅资料】白色的硫酸铜粉末遇水变为蓝色
【实验探究】化学实验小组的同学鉴别实验过程记录如下:
步骤1:取五种白色粉末各一药匙,分别放入五支洁净的试管中,各加蒸馏水2mL,充分振荡后静置。五支试管底部均有固体存在,只有盛放E的试管中液体呈蓝色,其他均呈无色。
步骤2:取B、C、D上层清液滴加稀盐酸,只有B的试管中有气泡产生,其他无明显现象。
步骤3:取A、C、D的上层清液放入试管中,分别滴加无色酚酞,A、C显红色。
请根据该学生的实验过程,回答下列问题:
(1)由步骤1可知E为
(2)步骤3中,D的现象是
(3)通过上述步骤,除E外,该化学小组的同学还推断出的是B为
(4)对尚未鉴别出来的物质,同学设计了实验进行确定,请将如表补充完整:
| 实验操作 | 实验现象及结论 |
| 取两种待测物质少量于试管①、②,加足量水配制成溶液,分别向其中滴加 | 观察到①试管中有白色沉淀产生,则①中的待测物质为 |
2020·甘肃天水·一模
类题推荐
化学老师交给某学校研究性学习小组一个任务:测定实验室里一瓶久置的 固体是否变质.该小组的同学进行了如下实验探究:
固体是否变质.该小组的同学进行了如下实验探究:
提出问题:猜想 :没变质,全部是
:没变质,全部是 ;
;
猜想 :部分变质,
:部分变质,________ ;
猜想 :完全变质,全部是
:完全变质,全部是 .
.
查阅资料:部分溶液在常温下的 如下:
如下:
设计方案并进行实验:请你与他们一起共同完成,并回答所给问题.
上述步骤①中,称量氢氧化钠固体样品用到的玻璃仪器名称是________ ,滴加过量 溶液的目的是
溶液的目的是________
实验结论:通过实验,说明上述猜想中________ 是正确的.
拓展:该小组同学为测定出该 固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为
固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为 ,则原样品中
,则原样品中 的质量分数为
的质量分数为________ (保留一位小数).
反思:久置的氢氧化钠变质的原因是________ (用化学方程式表示).
提出问题:猜想
猜想
猜想
查阅资料:部分溶液在常温下的
| 盐溶液 | | ||
| 等于 | 大于 | 等于 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品 | 产生白色沉淀 | 说明久置固体中,一定含有 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块 | 说明久置固体中,还一定含有 |
实验结论:通过实验,说明上述猜想中
拓展:该小组同学为测定出该
反思:久置的氢氧化钠变质的原因是
同学们在学习碱的性质时发现:二氧化碳能和氢氧化钠反应,但它们反应时没有现象。兴趣小组的同学提出能不能用实验证明二氧化碳和氢氧化钠确实发生了反应呢?
【查资料】
二氧化碳与氢氧化钠反应,当二氧化碳量不足时生成碳酸钠,如果继续通入过量二氧化碳,二氧化碳可进一步和水及碳酸钠反应生成碳酸氢钠。
【实验(一)】设计实验直接观察现象。
【进行实验】
同学们在老师指导下,查到氢氧化钠和碳酸钠在无水酒精和水中的溶解度如下表:
根据表中信息,他们选取了一种溶剂配制了饱和氢氧化钠溶液,然后向该饱和溶液中通入适量二氧化碳气体,他们看到了明显的现象,从而直接证明了二氧化碳和氢氧化钠确实发生了反应。
(1)他们选取的这种溶剂是______________ ,观察到的现象是___________ 。
【实验(二)】探究二氧化碳通入氢氧化钠溶液后有新物质生成。
【进行实验】
同学们设计了如下实验装置:
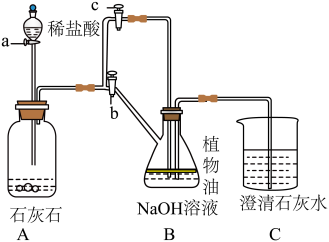
(2)第一步:实验时他们先关闭b,打开a、c,观察到A中有大量气泡产生,B、C中没有明显变化。写出A中发生的化学反应方程式_________________ 。
(3)第二步:接下来他们进行了一个操作,观察到C中澄清石灰水变浑浊,从而证明了第一步时B中氢氧化钠确实与来自于A中的二氧化碳发生了反应生成了新物质。他们进行的这个操作是_________________ ,写出C中澄清石灰水变浑浊的化学方程式_________________ 。
(4)同学们讨论后发现如果把C中的澄清石灰水换成酸或盐,也能证明第一步时B中氢氧化钠与来自于A中的二氧化碳确实发生了反应生成了新物质。如果把C中的澄清石灰水换成酸,完成第二步实验时C中出现的现象是_________________ ;如果把C中的澄清石灰水换成盐,则不能选择下列哪种盐(选填编号)_________________ 。
①.CaCl2②.BaCl2③.K2SO4④. Ba(NO3)2
【实验(三)】同学们用pH传感器测定氢氧化钠溶液通入二氧化碳后pH的变化。
【进行实验】
如下图,瓶中装入了50g8%的NaOH溶液,均匀缓慢地通入二氧化碳气体,每100秒通入2.2g二氧化碳气体,总共通入了4.4g二氧化碳(通入的二氧化碳气体全部被瓶中溶液吸收)

从上图可得出当通入二氧化碳后,瓶中溶液的pH不断变小,这充分说明二氧化碳和氢氧化钠确实发生了反应。
(5)写出前100秒溶液中发生的化学反应方程式_________ 。
(6)写出200秒后溶液中溶质的化学式___________ ,该溶质的质量是___________ g。
【查资料】
二氧化碳与氢氧化钠反应,当二氧化碳量不足时生成碳酸钠,如果继续通入过量二氧化碳,二氧化碳可进一步和水及碳酸钠反应生成碳酸氢钠。
【实验(一)】设计实验直接观察现象。
【进行实验】
同学们在老师指导下,查到氢氧化钠和碳酸钠在无水酒精和水中的溶解度如下表:
| 氢氧化钠 | 碳酸钠 | |||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109 g | 129 g | 21.8 g | 49 g |
| 无水酒精 | 17.3 g | 40 g | 不溶 | 不溶 |
根据表中信息,他们选取了一种溶剂配制了饱和氢氧化钠溶液,然后向该饱和溶液中通入适量二氧化碳气体,他们看到了明显的现象,从而直接证明了二氧化碳和氢氧化钠确实发生了反应。
(1)他们选取的这种溶剂是
【实验(二)】探究二氧化碳通入氢氧化钠溶液后有新物质生成。
【进行实验】
同学们设计了如下实验装置:

(2)第一步:实验时他们先关闭b,打开a、c,观察到A中有大量气泡产生,B、C中没有明显变化。写出A中发生的化学反应方程式
(3)第二步:接下来他们进行了一个操作,观察到C中澄清石灰水变浑浊,从而证明了第一步时B中氢氧化钠确实与来自于A中的二氧化碳发生了反应生成了新物质。他们进行的这个操作是
(4)同学们讨论后发现如果把C中的澄清石灰水换成酸或盐,也能证明第一步时B中氢氧化钠与来自于A中的二氧化碳确实发生了反应生成了新物质。如果把C中的澄清石灰水换成酸,完成第二步实验时C中出现的现象是
①.CaCl2②.BaCl2③.K2SO4④. Ba(NO3)2
【实验(三)】同学们用pH传感器测定氢氧化钠溶液通入二氧化碳后pH的变化。
【进行实验】
如下图,瓶中装入了50g8%的NaOH溶液,均匀缓慢地通入二氧化碳气体,每100秒通入2.2g二氧化碳气体,总共通入了4.4g二氧化碳(通入的二氧化碳气体全部被瓶中溶液吸收)

从上图可得出当通入二氧化碳后,瓶中溶液的pH不断变小,这充分说明二氧化碳和氢氧化钠确实发生了反应。
(5)写出前100秒溶液中发生的化学反应方程式
(6)写出200秒后溶液中溶质的化学式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网