解答题 较难0.4 引用1 组卷71
金属是现代生活和工业生产中应用极为普遍的一类材料。已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究。小金查阅资料得Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应。
(1)请完成证明金属粉末中存在Fe和Cu的实验设计;为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,求:
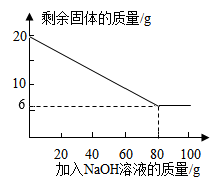
(2)该金属粉末中Al的质量分数为________ ;
(3)加入的NaOH溶液的溶质质量分数________ (结果精确到0.1%)。
| 实验操作 | 实验现象 | 结论 |
| Ⅰ取少量的金属粉末于试管中,加入足量的 | 有气泡产生 | 仅除去铝 |
| Ⅱ将试管静置,弃去上层清液,加入足量的稀硫酸 | 证明含有铁 | |
| Ⅲ将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
(1)请完成证明金属粉末中存在Fe和Cu的实验设计;为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,求:

(2)该金属粉末中Al的质量分数为
(3)加入的NaOH溶液的溶质质量分数
19-20九年级下·浙江杭州·阶段练习
类题推荐
某学生用一定浓度的稀硫酸做氧化铜和硫酸制取硫酸铜的实验,其中五次结果如下表所示:
根据实验结果填写下列空格:
(1)哪次反应氧化铜有剩余 ;
(2)表中的x是 。
(3)若硫酸的用量一定,以反应物氧化铜的质量为横坐标,以生成物硫酸铜的质量为纵坐标,则下列函数图像中, 符合实验事实。
A. B.
B.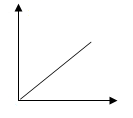 C.
C. D.
D.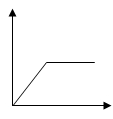
(4)试计算该硫酸溶液的质量分数是多少?
| 实验次序 | 氧化铜(克) | 硫酸溶液(克) | 硫酸铜(克) |
| 1 | 2.0 | 100 | 4.0 |
| 2 | 4.0 | 100 | 8.0 |
| 3 | 6.0 | 100 | 9.6 |
| 4 | 6.0 | 200 | x |
根据实验结果填写下列空格:
(1)哪次反应氧化铜有剩余 ;
(2)表中的x是 。
(3)若硫酸的用量一定,以反应物氧化铜的质量为横坐标,以生成物硫酸铜的质量为纵坐标,则下列函数图像中, 符合实验事实。
A.
 B.
B. C.
C. D.
D.
(4)试计算该硫酸溶液的质量分数是多少?
某化学小组同学按下图所示装置和表中所给试剂进行实验(图中铁架台等夹持仪器均已略去):

(1)在试管I中加入试剂后,塞紧橡皮塞,关闭止水夹a,打开止水夹b,试管II中液面上升,溶液变浑浊。符合以上实验现象的试剂是_____ 组,此时II中发生反应的化学方程式为_____ 。
(2)在试管I中加入试剂后,塞紧橡皮塞,立即打开止水夹a,关闭止水夹b,II中有气泡冒出,溶液变浑浊。符合以上实验现象的试剂是_____ 组。

| 组别 | A组 | B组 | C组 | D组 |
| 试管I | 稀 | 稀 | 稀 | 稀 |
| 试管Ⅱ |
(1)在试管I中加入试剂后,塞紧橡皮塞,关闭止水夹a,打开止水夹b,试管II中液面上升,溶液变浑浊。符合以上实验现象的试剂是
(2)在试管I中加入试剂后,塞紧橡皮塞,立即打开止水夹a,关闭止水夹b,II中有气泡冒出,溶液变浑浊。符合以上实验现象的试剂是
黄铜是锌和铜的合金,可以用来制造机器零件及日常用品.为了测定粉末状黄铜样品中锌的质量分数,取10g这种样品放入烧杯中,再将40g稀盐酸分四次加入该烧杯中,均充分反应测得的实验数据如下表:
分析表中数据,完成下列问题:
(1)在第_____ 次实验结束时样品中的锌就已完全反应。
(2)计算该黄铜样品中锌的质量分数_____ 。
(3)计算所用稀盐酸的溶质质量分数_____ 。
| 实验次数 | 1 | 2 | 3 | 4 |
| 稀盐酸的用量 | 10g | 10g | 10g | 10g |
| 剩余固体的质量 | 8.7g | 7.4g | 6.7g | 6.7g |
分析表中数据,完成下列问题:
(1)在第
(2)计算该黄铜样品中锌的质量分数
(3)计算所用稀盐酸的溶质质量分数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


