解答题-工业流程题 较难0.4 引用1 组卷154
二氧化锰无论在实验室还是在生产、生活中均有广泛应用。工业上可以用制备对苯二酚的废液为原料生产二氧化锰。此工艺对节约资源、保护环境、提高经济效益有着重要意义。
(1)经分析知该废液中含有硫酸锰、硫酸铵、硫酸以及Fe2+、Co2+、Ni2+等金属离子。以此为原料制备化学二氧化锰的流程如图所示。
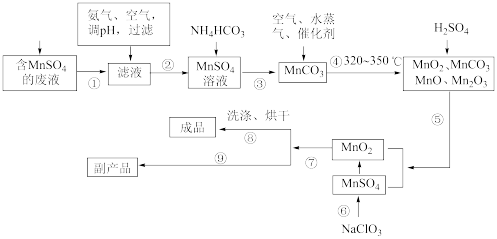
①常温下几种有关难溶硫化物的溶度积常数如下表,若除去Fe2+后的废液中Mn2+浓度为1mol/L,欲使Co2+和Ni2+完全沉淀,而Mn2+不受损失,S2-的浓度范围应控制在___ mol/L。
②步骤⑥的化学方程式为___ 。
③步骤①~⑨中涉及到过滤的操作有___ 。(填序号)
④步骤⑨得到的副产品的化学式为___ ,其重要的用途之一是___ 。得到该副产品的操作是___ 。
(2)生产电解二氧化锰的原理是在93℃左右以石墨为电极电解硫酸锰和硫酸的混合溶液,写出阳极的电极反应式___ ,若电解过程中的电压为3V,理论上生产1tMnO2消耗电能___ kw·h。(1kw·h=3.6×106J)
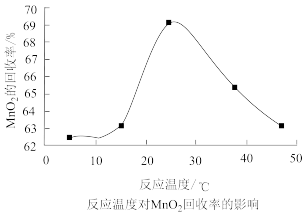
(3)双氧水氧化法制备二氧化锰时所发生的反应为MnSO4+2NH3+H2O2→MnO2+(NH4)2SO4,在溶液的pH、过氧化氢的用量和反应时间一定的情况下,温度对实验结果的影响如图所示。MnO2的回收率随着温度升高先增大后减小的可能原因是___ 。
(1)经分析知该废液中含有硫酸锰、硫酸铵、硫酸以及Fe2+、Co2+、Ni2+等金属离子。以此为原料制备化学二氧化锰的流程如图所示。

①常温下几种有关难溶硫化物的溶度积常数如下表,若除去Fe2+后的废液中Mn2+浓度为1mol/L,欲使Co2+和Ni2+完全沉淀,而Mn2+不受损失,S2-的浓度范围应控制在
| 化合物 | MnS | CoS(α型) | NiS |
| Ksp | 2.5×10-10 | 4×10-21 | 1.07×10-21 |
②步骤⑥的化学方程式为
③步骤①~⑨中涉及到过滤的操作有
④步骤⑨得到的副产品的化学式为
(2)生产电解二氧化锰的原理是在93℃左右以石墨为电极电解硫酸锰和硫酸的混合溶液,写出阳极的电极反应式
(3)双氧水氧化法制备二氧化锰时所发生的反应为MnSO4+2NH3+H2O2→MnO2+(NH4)2SO4,在溶液的pH、过氧化氢的用量和反应时间一定的情况下,温度对实验结果的影响如图所示。MnO2的回收率随着温度升高先增大后减小的可能原因是

19-20高三下·山西太原·阶段练习
类题推荐
锰是生产各种合金的重要元素。工业上以含锰矿石(主要成分为 ,还含有铁、钴、镍、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
,还含有铁、钴、镍、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
表一
表二
回答下列问题:
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有_______ (写两种)。
(2)“氧化”步骤发生反应的离子方程式为_______ 。
(3)滤渣1的主要成分是_______ ,实验室中为了加快固液混合物的分离,常采用的操作是_______ 。
(4)有同学提出,加入(NH4)2S除钴、除镍的步骤可以放在“除杂1”之前,你是否赞同?请说明理由:_______ 。
(5)由 晶体制备CuCl2的方法是
晶体制备CuCl2的方法是_______ 。
(6)25℃时,分离出滤渣3所得的滤液中 =
=_______ ,欲使沉钴后的溶液中 ,需要控制溶液的pH至少为
,需要控制溶液的pH至少为_______ 。(已知
(7)电解废液中还含有少量Mn2+,向其中加入饱和N 溶液,有沉淀和气体生成,该反应的离子方程式为
溶液,有沉淀和气体生成,该反应的离子方程式为_______ 。

表一
| 物质 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp |
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 6.4 | 10.4 |
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有
(2)“氧化”步骤发生反应的离子方程式为
(3)滤渣1的主要成分是
(4)有同学提出,加入(NH4)2S除钴、除镍的步骤可以放在“除杂1”之前,你是否赞同?请说明理由:
(5)由
(6)25℃时,分离出滤渣3所得的滤液中
(7)电解废液中还含有少量Mn2+,向其中加入饱和N
一水合硫酸锰(MnSO4·H2O)主要用于饲料添加剂和植物合成叶绿素的催化剂。一种以软锰矿(主要成分是MnO2,还有CaO、MgO、Al2O3、SiO2等杂质)和废铁屑(主要成分是Fe,还含有少量Cu)为原料制备MnSO4·H2O的工艺流程如下:
回答下列问题:
(1)滤渣I与NaOH溶液反应的离子方程式为___________ 。
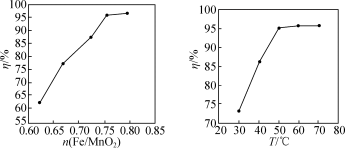
(2)“浸出”时,锰的浸出率随Fe/MnO2摩尔比、反应温度的变化曲线如下图所示,则最佳的反应条件为___________ 。
①Fe、稀硫酸、MnO2发生总反应的离子方程式为___________ 。
②反应过程中硫酸不能过量太多的原因是___________ 。
(4)“氧化”时,过氧化氢的实际消耗量大于理论消耗量的原因是___________ 。
(5)“除铁、铝”调节溶液的pH不小于___________ (保留1位小数;已知离子浓度小于1.0×10-5 mol·L-1时,可认为该离子沉淀完全)。
(6)滤渣Ⅳ的主要成分是___________ (填化学式)。
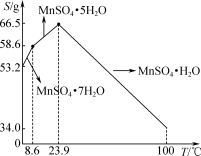
(7)硫酸锰在不同温度下的溶解度和一定温度范围内析出晶体的组成如图所示,“除杂”所得滤液控制温度在80~90 ℃之间蒸发结晶,___________ (填操作名称),得到MnSO4·H2O。

| 物质 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 |
| Ksp | 1.0×10-33 | 5×10-17 | 1.0×10-38 | 2.0×10-13 |
(1)滤渣I与NaOH溶液反应的离子方程式为
(2)“浸出”时,锰的浸出率随Fe/MnO2摩尔比、反应温度的变化曲线如下图所示,则最佳的反应条件为
| 离子 | Mn2+ | Fe2+ | Fe3+ | Cu2+ | H+ |
| c/(mol·L-1) | 0.601 | 0.15 | 0.3 | 0.001 | 0.1 |
②反应过程中硫酸不能过量太多的原因是
(4)“氧化”时,过氧化氢的实际消耗量大于理论消耗量的原因是
(5)“除铁、铝”调节溶液的pH不小于
(6)滤渣Ⅳ的主要成分是
(7)硫酸锰在不同温度下的溶解度和一定温度范围内析出晶体的组成如图所示,“除杂”所得滤液控制温度在80~90 ℃之间蒸发结晶,
用生产钛白的副产品FeSO4与软锰矿(主要成分是MnO2)可制备高纯MnO2

(1)步骤①中研磨的目的是______________________ 。
(2)步骤②中主要发生的反应是FeSO4与MnO2转化为MnSO4与__________ 。
(3)步骤②中Mn2+浸出率受初始H2SO4浓度与温度的影响如下图所示。
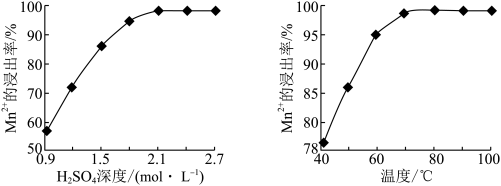
软锰矿粉酸浸的适宜条件是________________ 。
(4)步骤②中,若硫酸初始浓度小于1.8mol/L,反应进行一段时间后,有红褐色固体析出,其原因是____________ 。
(5)已知MnSO4粗液中还含有Al3+、Fe3+和Ni2+离子,溶液中离子生成氢氧化物的pH如下表:
注:金属离子的起始浓度为0.1mol·L-1
步骤③进行的操作是:调节pH=5.4,过滤,滤渣中含_____________________ 。
(6)已知:几种难溶物的溶解平衡常数K
步骤③还需加入的除杂试剂是_______ 固体(填序号)。
A.Na2CO3 B.MnCO3 C.Na2S D.MnS
(7)步骤⑤中焙烧MnCO3制MnO2,发生反应的化学方程式是_____________ 。

(1)步骤①中研磨的目的是
(2)步骤②中主要发生的反应是FeSO4与MnO2转化为MnSO4与
(3)步骤②中Mn2+浸出率受初始H2SO4浓度与温度的影响如下图所示。

软锰矿粉酸浸的适宜条件是
(4)步骤②中,若硫酸初始浓度小于1.8mol/L,反应进行一段时间后,有红褐色固体析出,其原因是
(5)已知MnSO4粗液中还含有Al3+、Fe3+和Ni2+离子,溶液中离子生成氢氧化物的pH如下表:
| Al(OH)3 | Fe(OH)3 | Ni(OH)2 | Mn(OH)2 | |
| 开始沉淀时pH | 3.4 | 1.5 | 6.9 | 8.2 |
| 完全沉淀时pH | 4.7 | 2.8 | 8.9 | 10.2 |
注:金属离子的起始浓度为0.1mol·L-1
步骤③进行的操作是:调节pH=5.4,过滤,滤渣中含
(6)已知:几种难溶物的溶解平衡常数K
| 化学式 | MnCO3 | NiCO3 | MnS | NiS |
| K | 2.24×10-11 | 1.42×10-7 | 4.65×10-14 | 1.07×10-21 |
步骤③还需加入的除杂试剂是
A.Na2CO3 B.MnCO3 C.Na2S D.MnS
(7)步骤⑤中焙烧MnCO3制MnO2,发生反应的化学方程式是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


