解答题-原理综合题 适中0.65 引用8 组卷308
中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,其反应如下:2CH4(g)⇌C2H4(g)+2H2(g) ΔH>0
(1)已知相关化学键的键能如上表,甲烷制备乙烯反应的ΔH=____________ (用含a、b、c、d的代数式表示)。
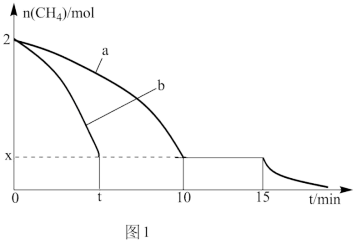
(2)T1温度时,向1 L的恒容反应器中充入2mol CH4,仅发生上述反应,反应过程中 0~15min CH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
①0~10min内CH4表示的反应速率为__________ mol/(L·min)。
②若图1中曲线a、曲线b分别表示在温度T1时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(CH4)变化曲线,其中表示催化剂表面积较大的曲线是________ (填“a”或 “b”)。
③15min时,若改变外界反应条件,导致n(CH4)发生图1中所示变化,则改变的条件可能是_____________________________________ (任答一条即可)。
(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2)其中k正、k逆为速率常数仅与温度有关,T1温度时k正与k逆的比值为______ (填数值)。若将温度由T1升高到T2,则反应速率增大的倍数v正____ v逆(填“>”“=”或“<”),判断的理由是_________________ 。
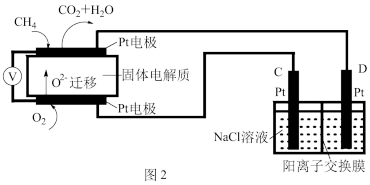
(4)科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了 Y2O3与 ZrO2的固体,可在高温下传导O2-。
①C极的Pt为______ 极(填“阳”或“阴” )。
②该电池工作时负极反应方程式为_____________________ 。
③用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为112mL,则阴极区所得溶液在25℃时pH=_______ (假设电解前后NaCl溶液的体积均为500mL)。
| 化学键 | H—H | C—H | C=C | C—C |
| E(kJ/mol) | a | b | c | d |
(1)已知相关化学键的键能如上表,甲烷制备乙烯反应的ΔH=


(2)T1温度时,向1 L的恒容反应器中充入2mol CH4,仅发生上述反应,反应过程中 0~15min CH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
①0~10min内CH4表示的反应速率为
②若图1中曲线a、曲线b分别表示在温度T1时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(CH4)变化曲线,其中表示催化剂表面积较大的曲线是
③15min时,若改变外界反应条件,导致n(CH4)发生图1中所示变化,则改变的条件可能是
(3)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2)其中k正、k逆为速率常数仅与温度有关,T1温度时k正与k逆的比值为
(4)科研人员设计了甲烷燃料电池并用于电解。如图2所示,电解质是掺杂了 Y2O3与 ZrO2的固体,可在高温下传导O2-。
①C极的Pt为
②该电池工作时负极反应方程式为
③用该电池电解饱和食盐水,一段时间后收集到标况下气体总体积为112mL,则阴极区所得溶液在25℃时pH=
2019·陕西宝鸡·三模
类题推荐
甲烷是一种重要的化工原料,广泛应用于工业中。回答下列问题:
(1)甲烷在工业上可用于制备合成气: ,在某密闭容器中通入
,在某密闭容器中通入 和
和 ,在不同条件下发生反应。测得平衡时
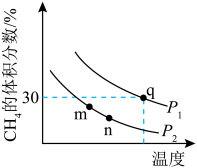
,在不同条件下发生反应。测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。
___________ (填“<”、“>”或“=”下同)P2,
___________ 0。
② 三点的化学平衡常数大小关系为
三点的化学平衡常数大小关系为___________ 。
③ 点甲烷的转化率为
点甲烷的转化率为___________ 。
(2)甲烷在一定条件下脱氢可生成乙烯,其反应如下: 。
。 温度下,在体积为
温度下,在体积为 的刚性密闭容器中充入
的刚性密闭容器中充入 甲烷进行上述反应,容器内的总压强
甲烷进行上述反应,容器内的总压强 随时间
随时间 的变化如下表所示:
的变化如下表所示:
①下列有关说法正确的是___________ 。
A.当混合气的密度不变时,表明该反应已达到平衡状态
B.反应进行到第10分钟时刚好达到平衡
C.升温既可提高反应速率也能提高甲烷的转化率
D.使用适当的催化剂既可提高反应速率也能提高甲烷的转化率
E.该反应在较高温度下可自发进行
②前10min内,平均速率v(H2)=___________ kPa·min-1,实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2),其中k正、k逆为速率常数,仅与温度有关,T1温度时,k正/k逆=___________ (填数值)。
(3)科研人员设计了甲烷燃料电池电解饱和食盐水装置如图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。___________ 。
②用该电池电解100mL饱和食盐水,若电解一段时间后,两极产生的气体体积分别为0.224L和0.336L(均为标准状况),则电解所得溶液的pH=___________ (忽略气体溶解和溶液体积变化)。
(1)甲烷在工业上可用于制备合成气:
②
③
(2)甲烷在一定条件下脱氢可生成乙烯,其反应如下:
| 反应时间/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| 总压强P/kPa | 10.0 | 11.5 | 12.3 | 13.0 | 13.6 | 14.0 | 14.0 |
A.当混合气的密度不变时,表明该反应已达到平衡状态
B.反应进行到第10分钟时刚好达到平衡
C.升温既可提高反应速率也能提高甲烷的转化率
D.使用适当的催化剂既可提高反应速率也能提高甲烷的转化率
E.该反应在较高温度下可自发进行
②前10min内,平均速率v(H2)=
(3)科研人员设计了甲烷燃料电池电解饱和食盐水装置如图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。
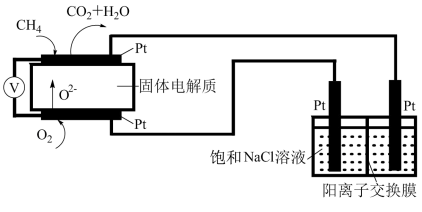
②用该电池电解100mL饱和食盐水,若电解一段时间后,两极产生的气体体积分别为0.224L和0.336L(均为标准状况),则电解所得溶液的pH=
中科院大连化物所研究员在《Sciance》刊文报道了甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯。其反应为 △H>0.回答下列问题:
△H>0.回答下列问题:
(1)已知相关化学键的键能(E)见下表,甲烷制备乙烯反应的△H=___________ 。(用含a、b、c、d的代数式表示)。
(2)当甲烷分解时,几种气体平衡时分压对数lgp分(P分单位MPa)与温度(K)的关系如图甲所示。
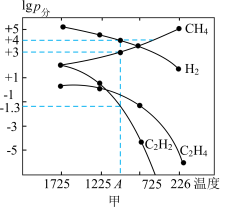
①T1℃时,向1L刚性恒容密闭容器中充入1.2 mol CH4,只发生反应 ,达到平衡时,测得c(C2H4)=c(CH4)。则CH4的平衡转化率为
,达到平衡时,测得c(C2H4)=c(CH4)。则CH4的平衡转化率为___________ (保留小数点后一位)。实验测得v正=k正·c2(CH4),v逆=k逆·c(C2H4)·c2(H2),其中k正、k逆为速率常数仅与温度有关,则 =
=___________ (填数值)。若将温度由T1℃升高到T2℃,反应速率v正___________ v,逆(填“>”“=”或“<”),判断的理由是___________ 。
②反应 在图中A点温度时的分压平衡常数Kp=
在图中A点温度时的分压平衡常数Kp=___________ (不写单位,已知lg0.05=-1.3)。
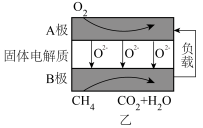
(3)一种甲烷新型燃料电池的工作原理如图乙所示,电解质是掺杂了Y2O3与ZrO3的固体,可在高温下传导O2-。则B极的名称为___________ ,其电极反应式为___________ 。
(1)已知相关化学键的键能(E)见下表,甲烷制备乙烯反应的△H=
| 化学键 | H-H | C-H | C=C | C-C |
| E(kJ·mol-1) | a | b | c | d |
(2)当甲烷分解时,几种气体平衡时分压对数lgp分(P分单位MPa)与温度(K)的关系如图甲所示。

①T1℃时,向1L刚性恒容密闭容器中充入1.2 mol CH4,只发生反应
②反应
(3)一种甲烷新型燃料电池的工作原理如图乙所示,电解质是掺杂了Y2O3与ZrO3的固体,可在高温下传导O2-。则B极的名称为

温度为T1时,向1L的恒容反应器中充入2molCH4,只发生2CH4(g) C2H4(g)+2H2(g) ΔH>0,上述反应过程中0~15minCH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
C2H4(g)+2H2(g) ΔH>0,上述反应过程中0~15minCH4的物质的量随时间变化如图1,测得10~15min时H2的浓度为1.6mol/L。
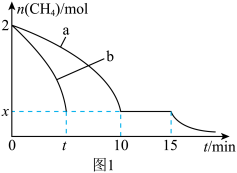
(1)0~10min内CH4表示的反应速率为___________ mol/(L·min)。
(2)下列叙述能证明该反应已经达到化学平衡状态的是(填序号)___________。
(3)若图1中曲线a、曲线b分别表示在温度T1时,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(CH4)变化曲线,其中表示催化剂表面积较大的曲线是___________ (填“a”或“b”)。
(4)15min时,若改变外界反应条件,导致n(CH4)发生图1中所示变化,则改变的条件可能是___________
(5)实验测得v正=k正c2(CH4),v逆=k逆c(C2H4)·c2(H2)其中k正、k逆为速率常数仅与温度有关,T1温度时k正与k逆的比值为___________ (填数值)。若将温度由T1升高到T2,则反应速率增大的倍数v正___________ v逆(填“>”“=”或“<”),判断的理由是___________ 。

(1)0~10min内CH4表示的反应速率为
(2)下列叙述能证明该反应已经达到化学平衡状态的是(填序号)___________。
| A.容器内混合气体密度不再变化 |
| B.容器内气体压强不再变化 |
| C.2v(CH4)正=v(C2H4)逆 |
| D.单位时间内消耗1molCH4同时消耗1molH2 |
(4)15min时,若改变外界反应条件,导致n(CH4)发生图1中所示变化,则改变的条件可能是___________
| A.升高温度 | B.改用高效催化剂 | C.扩大容器的体积 | D.增加CH4的浓度 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


