解答题-原理综合题 适中0.65 引用2 组卷120
氮氧化物( )和硫氧化物(主要是
)和硫氧化物(主要是 )是重要的大气污染物,怎样处理?一能解决环境污染问题,二能变废为宝,提高资源利率用,正是化学学科的研究领域与研究意义所在。请思考并回答下列问题:
)是重要的大气污染物,怎样处理?一能解决环境污染问题,二能变废为宝,提高资源利率用,正是化学学科的研究领域与研究意义所在。请思考并回答下列问题:
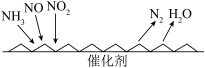
(1) 的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的
的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的 。用氨水吸收
。用氨水吸收 ,然后经氧化最终生成硫酸铵,共总反应可表示为:
,然后经氧化最终生成硫酸铵,共总反应可表示为: ,上述反应又经历了下面几个过程,请回答问题:
,上述反应又经历了下面几个过程,请回答问题:
① ;
;
②

________ ;
③ 。
。
(2) 的排放主要来自于汽车尾气,有人利用反应
的排放主要来自于汽车尾气,有人利用反应 ;
; ,用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率
,用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 随温度的变化如图所示:
随温度的变化如图所示:
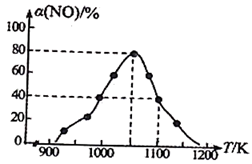
①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是___________ 。
②已知:气体分压=气体总压×体积分数。用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作 )。在1100K,
)。在1100K, 时,该反应的化学平衡常数
时,该反应的化学平衡常数
___________ 。
(3)在高效催化剂的作用下用 还原
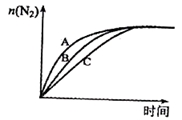
还原 ,也可消除氮氧化物的污染。在相同条件下,选用A、B、C三种不同催化剂进行反应,生成
,也可消除氮氧化物的污染。在相同条件下,选用A、B、C三种不同催化剂进行反应,生成 的物质的量与时间变化关系如图所示,其中活化能最小的是
的物质的量与时间变化关系如图所示,其中活化能最小的是_______ (填字母标号)。
(4)在汽车尾气的净化装置中CO和NO发生反应:
 。实验测得,v正=k正
。实验测得,v正=k正 ,v逆=k逆
,v逆=k逆 (k正、k逆为速率常数,只与温度有关)。
(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数_________ (填“>”、“<”或“=”) k逆增大的倍数。
②若在1L的密闭容器中充入1mol CO和1mol NO,在一定温度下达到平衡时,CO的转化率为40%,则
_________ (保留2位有效数字)。
(1)
①
②
③
(2)

①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是
②已知:气体分压=气体总压×体积分数。用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作
(3)在高效催化剂的作用下用

(4)在汽车尾气的净化装置中CO和NO发生反应:
①达到平衡后,仅升高温度,k正增大的倍数
②若在1L的密闭容器中充入1mol CO和1mol NO,在一定温度下达到平衡时,CO的转化率为40%,则
19-20高二·浙江·期末
类题推荐
研究处理NOx对环境保护有着重要的意义。回答下列问题:
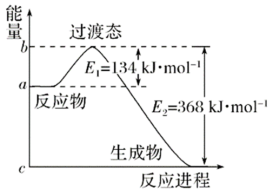
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1__ (填“增大”“减小”或“不变”,下同),△H__ 。请写出NO2和CO反应的热化学方程式:___ 。
(2)一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160kJ•mol-1
下列选项正确的是__ (填标号)。
(3)利用反应C(s)+2NO(g)=N2(g)+CO2(g) △H=-34.0kJ•mol-1,一定条件下消除NO的污染。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率α(NO)随温度的变化如图所示:
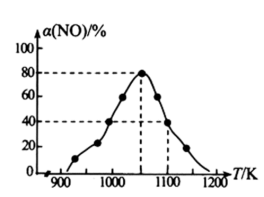
①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是__ ;在1100K时,CO2的体积分数为__ 。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=__ (已知:气体分压=气体总压×体积分数)。
(4)在汽车尾气的净化装置中CO和NO发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H2=-746.8kJ•mol-1。实验测得,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。
N2(g)+2CO2(g) △H2=-746.8kJ•mol-1。实验测得,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数__ (填">”、“<”或“=”)k逆增大的倍数。
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为40%,则 =
=__ (保留2位有效数字)。
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1

(2)一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160kJ•mol-1
下列选项正确的是
| A.CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ•mol-1 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) △H3>△H1 |
| C.若用0.2molCH4还原NO2至N2,则反应中放出的热量一定为173.4kJ |
| D.若用标准状况下2.24LCH4还原NO2至N2,整个过程中转移的电子为1.6mol |

①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=
(4)在汽车尾气的净化装置中CO和NO发生反应:2NO(g)+2CO(g)
①达到平衡后,仅升高温度,k正增大的倍数
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为40%,则
“绿水青山就是金山银山”,因此研究 、
、 等大气污染物的妥善处理具有重要意义。
等大气污染物的妥善处理具有重要意义。
(1) 的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的
的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的 。已知吸收过程中相关反应的热化学方程式如下:
。已知吸收过程中相关反应的热化学方程式如下:
①
 ;
;
②
 ;
;
③
 。
。
则反应 的
的
_____ 
(2)燃煤发电厂常利用反应
 对煤进行脱硫处理来减少
对煤进行脱硫处理来减少 的排放。对于该反应,在
的排放。对于该反应,在 时,借助传感器测得反应在不同时间点上各物质的浓度如下:
时,借助传感器测得反应在不同时间点上各物质的浓度如下:
① 内,平均反应速率
内,平均反应速率
________  ;当升高温度,该反应的平衡常数K
;当升高温度,该反应的平衡常数K________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
② 后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是
后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是________  填字母
填字母 。
。
A.加入一定量的粉状碳酸钙
B.通入一定量的
C.适当缩小容器的体积
D.加入合适的催化剂
(3) 的排放主要来自于汽车尾气,有人利用反应
的排放主要来自于汽车尾气,有人利用反应


 ,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压,测得NO的转化率随温度的变化如图所示:
,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压,测得NO的转化率随温度的变化如图所示:
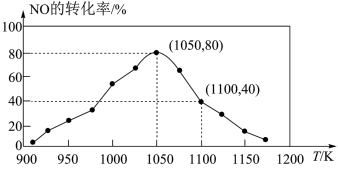
由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为________ ;在1100K时, 的体积分数为
的体积分数为________ 。
(4)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数 记作
记作 。在1050K、
。在1050K、 时,该反应的化学平衡常数
时,该反应的化学平衡常数
________  已知:气体分压
已知:气体分压 气体总压
气体总压 体积分数
体积分数 。
。
(5)为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应


 ,生成无毒的
,生成无毒的 和
和 。实验测得,
。实验测得, ,
, 、
、 为速率常数,只与温度有关
为速率常数,只与温度有关 。
。
①达到平衡后,仅升高温度, 增大的倍数
增大的倍数________  填“
填“ ”“
”“ ”或“
”或“ ”
” 增大的倍数。
增大的倍数。
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为 ,则
,则
__________ 。
(1)
①
②
③
则反应
(2)燃煤发电厂常利用反应
| 0 | 10 | 20 | 30 | 40 | 50 | |
| O2 | 1.00 | 0.79 | 0.60 | 0.60 | 0.64 | 0.64 |
| CO2 | 0 | 0.42 | 0.80 | 0.80 | 0.88 | 0.88 |
①
②
A.加入一定量的粉状碳酸钙
B.通入一定量的
C.适当缩小容器的体积
D.加入合适的催化剂
(3)

由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为
(4)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数
(5)为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应
①达到平衡后,仅升高温度,
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网