解答题-原理综合题 较难0.4 引用5 组卷404
甲硅烷广泛用于电子工业、汽车领域,三氯氢硅( )是制备甲硅烷的重要原料。回答下列问题:
)是制备甲硅烷的重要原料。回答下列问题:
(1)工业上以硅粉和氯化氢气体为原料生产 时伴随发生的反应有:
时伴随发生的反应有:
①
②
以硅粉和氯化氢气体生产 的热化学方程式是
的热化学方程式是_______________________ 。
(2)工业上可用四氯化硅和氢化铝锂( )制甲硅烷,反应后得甲硅烷及两种盐。该反应的化学方程式为
)制甲硅烷,反应后得甲硅烷及两种盐。该反应的化学方程式为_________________________________________________ 。
(3)三氯氢硅歧化也可制得甲硅烷。反应 为歧化制甲硅烷过程的关键步骤,此反应采用一定量的
为歧化制甲硅烷过程的关键步骤,此反应采用一定量的 催化剂,在不同反应温度下测得
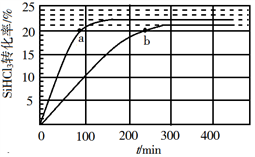
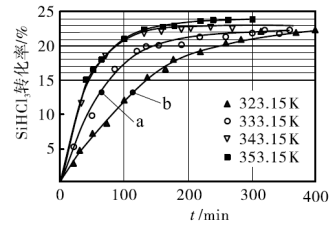
催化剂,在不同反应温度下测得 的转化率随时间的变化关系如图所示。
的转化率随时间的变化关系如图所示。
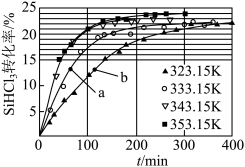
① 时,平衡转化率为
时,平衡转化率为_________ 。该反应是__________ 反应(填“放热”或“吸热”)。
② 时,要缩短反应达到平衡的时间,可采取的措施有
时,要缩短反应达到平衡的时间,可采取的措施有________________________ 。(答一种即可)
③比较a、b处反应速率的大小:
_______________  (填“>”“<”或“=”)。已知反应速率
(填“>”“<”或“=”)。已知反应速率 分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在
分别是正、逆反应的速率常数,与反应温度有关,x为物质的量分数,则在 时
时
___________ (保留3位小数)。
(1)工业上以硅粉和氯化氢气体为原料生产
①
②
以硅粉和氯化氢气体生产
(2)工业上可用四氯化硅和氢化铝锂(
(3)三氯氢硅歧化也可制得甲硅烷。反应

①
②
③比较a、b处反应速率的大小:
2020·四川绵阳·二模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

 SiH2Cl2(g)+ SiCl4(g)
SiH2Cl2(g)+ SiCl4(g)