解答题-工业流程题 较难0.4 引用1 组卷266
硫酸铁铵[(NH4)xFey(SO4)z∙nH2O]是一种重要铁盐,实验室采用废铁屑来制备硫酸铁铵的流程如下:
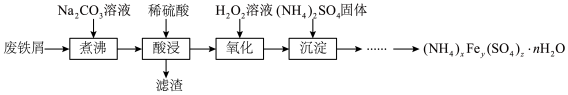
(1)将废铁屑和Na2CO3溶液混合煮沸可除去铁屑表面的油脂,原理是_____________ 。
(2)“氧化”过程需使用足量的H2O2,同时溶液要保持pH小于0.5,目的是__________ 。
(3)化学兴趣小组用如下方法测定硫酸铁铵晶体的化学式:
步骤1:准确称取样品28.92 g,溶于水配成100 mL溶液。
步骤2:准确量取25.00 mL步骤1所得溶液于锥形瓶中,加入适量稀硫酸,滴加过量的SnCl2溶液(Sn2+与Fe3+反应生成Sn4+和Fe2+),充分反应后除去过量的Sn2+。用0.1000mol∙L-1的K2Cr2O7溶液滴定Fe2+,滴定至终点时消耗K2Cr2O7溶液25.00 mL。(滴定过程中Cr2O72-转化成Cr3+)
步骤3:准确量取25.00 mL步骤1所得溶液于锥形瓶中,加入过量的BaCl2溶液,将所得白色沉淀过滤、洗涤、干燥后称量,所得固体质量为6.99 g。
①排除装有K2Cr2O7溶液的滴定管尖嘴处气泡的方法是_________ 。
②通过计算确定该硫酸铁铵的化学式____________ (写出计算过程)。

(1)将废铁屑和Na2CO3溶液混合煮沸可除去铁屑表面的油脂,原理是
(2)“氧化”过程需使用足量的H2O2,同时溶液要保持pH小于0.5,目的是
(3)化学兴趣小组用如下方法测定硫酸铁铵晶体的化学式:
步骤1:准确称取样品28.92 g,溶于水配成100 mL溶液。
步骤2:准确量取25.00 mL步骤1所得溶液于锥形瓶中,加入适量稀硫酸,滴加过量的SnCl2溶液(Sn2+与Fe3+反应生成Sn4+和Fe2+),充分反应后除去过量的Sn2+。用0.1000mol∙L-1的K2Cr2O7溶液滴定Fe2+,滴定至终点时消耗K2Cr2O7溶液25.00 mL。(滴定过程中Cr2O72-转化成Cr3+)
步骤3:准确量取25.00 mL步骤1所得溶液于锥形瓶中,加入过量的BaCl2溶液,将所得白色沉淀过滤、洗涤、干燥后称量,所得固体质量为6.99 g。
①排除装有K2Cr2O7溶液的滴定管尖嘴处气泡的方法是
②通过计算确定该硫酸铁铵的化学式
2020·江苏南通·模拟预测
类题推荐
草酸合铜酸钾是一种重要的化工原料,其晶体组成可表示为KxCuy(C2O4)z·wH2O。
(1)实验室用CuSO4溶液和NaOH溶液混合制备Cu(OH)2,再将所得Cu(OH)2与KHC2O4溶液混合,可制备草酸合铜酸钾晶体。
已知:室温下,Ksp[Cu(OH)2]=2.2×10-20。制备Cu(OH)2的过程中,pH=7时,溶液中c(Cu2+)=_______ 。
(2)一种测定草酸合铜酸钾晶体组成的方法如下:
步骤Ⅰ:准确称取1.7700 g样品,充分加热,剩余固体为K2CO3与CuO的混合物,质量为1.0900 g。
步骤Ⅱ:准确称取1.7700 g样品,用NH3·H2O-NH4Cl溶液溶解、加水稀释,定容至100 mL。
步骤Ⅲ:准确量取步骤Ⅱ所得溶液25.00 mL于锥形瓶中,滴入指示剂,用浓度为0.05000 mol·L-1的EDTA标准溶液滴定至终点。(已知Cu2+ 与EDTA反应的化学计量数之比为1:1)。重复上述滴定操作两次,有关数据记录如表:
①第一次滴定消耗的EDTA标准溶液的体积明显偏大,其可能的原因有_______ 。
A.锥形瓶水洗后未干燥
B.滴定过程锥形瓶中有液体溅出
C.装EDTA标准溶液的滴定管水洗后未润洗
D.开始滴定时,滴定管尖嘴部分未充满液体
②通过计算确定该样品的化学式为______ (写出计算过程)。
(1)实验室用CuSO4溶液和NaOH溶液混合制备Cu(OH)2,再将所得Cu(OH)2与KHC2O4溶液混合,可制备草酸合铜酸钾晶体。
已知:室温下,Ksp[Cu(OH)2]=2.2×10-20。制备Cu(OH)2的过程中,pH=7时,溶液中c(Cu2+)=
(2)一种测定草酸合铜酸钾晶体组成的方法如下:
步骤Ⅰ:准确称取1.7700 g样品,充分加热,剩余固体为K2CO3与CuO的混合物,质量为1.0900 g。
步骤Ⅱ:准确称取1.7700 g样品,用NH3·H2O-NH4Cl溶液溶解、加水稀释,定容至100 mL。
步骤Ⅲ:准确量取步骤Ⅱ所得溶液25.00 mL于锥形瓶中,滴入指示剂,用浓度为0.05000 mol·L-1的EDTA标准溶液滴定至终点。(已知Cu2+ 与EDTA反应的化学计量数之比为1:1)。重复上述滴定操作两次,有关数据记录如表:
| 第一次滴定 | 第二次滴定 | 第三次滴定 | |
| 消耗EDTA标准溶液的体积/mL | 25.92 | 24.99 | 25.01 |
A.锥形瓶水洗后未干燥
B.滴定过程锥形瓶中有液体溅出
C.装EDTA标准溶液的滴定管水洗后未润洗
D.开始滴定时,滴定管尖嘴部分未充满液体
②通过计算确定该样品的化学式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网