解答题-结构与性质 适中0.65 引用1 组卷69
根据反应:2Na2CO3+ SnO2+4S Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:
Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:
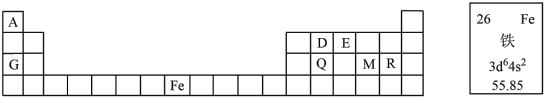
(1)上述反应涉及的元素中,非金属性最强的元素的最外层电子排布式为_____________ 在上述反应的生成物中,属于分子晶体的结构式___________________ 。
(2)在上述反应中单质物质的原子核外共有______ 种不同运动状态的电子,有_____ 种不同能量的电子。
(3)上述反应中,金属性最强的元素与铝元素相比较,可作为判断金属性强弱依据的是__________ (选填编号)。
a.能否置换出铝盐溶液中铝
b.Al(OH)3能否溶解在该元素最高价氧化物对应水化物中
c.单质与氢气化合的难易程度
d.单质与同浓度的稀盐酸发生反应的快慢程度
(4)常温下,测得Na2SnS3溶液pH>7,请用离子方程式表示其原因:___ 。
(1)上述反应涉及的元素中,非金属性最强的元素的最外层电子排布式为
(2)在上述反应中单质物质的原子核外共有
(3)上述反应中,金属性最强的元素与铝元素相比较,可作为判断金属性强弱依据的是
a.能否置换出铝盐溶液中铝
b.Al(OH)3能否溶解在该元素最高价氧化物对应水化物中
c.单质与氢气化合的难易程度
d.单质与同浓度的稀盐酸发生反应的快慢程度
(4)常温下,测得Na2SnS3溶液pH>7,请用离子方程式表示其原因:
2013·上海闵行·一模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 Na2SO4 + Na2SnS3+2CO2↑回答下列问题:
Na2SO4 + Na2SnS3+2CO2↑回答下列问题: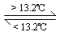 Sn(s、白) -2.1 kJ,根据以上信息得出的结论正确的是
Sn(s、白) -2.1 kJ,根据以上信息得出的结论正确的是