填空题 适中0.65 引用1 组卷105
苯分子等芳香烃化合物里的氢原子被硫酸分子里的磺酸基(—SO3H)所取代的反应,称为磺化反应。浓硫酸有时也用SO3代替浓硫酸,其优点是____________________ 、____________________________________ 。(至少写出两点),用浓硫酸吸收SO3可得发烟硫酸(H2SO4·SO3)。某化工厂用1.5m3 98.3%的浓硫酸(密度为1.84g/mL)吸收SO3形成发烟硫酸,再与水混合,可得到95%的硫酸(密度为1.79g/mL)_____________ m3(保留2位小数)。
2014·上海·零模
类题推荐
人胃酸(主要成分是盐酸)过多,会引起很多胃病,需服用抗酸药治疗。抗酸药胃舒平的主要成分是氢氧化铝,某同学为测定该药中氢氧化铝的质量分数进行如下几步操作(设该药片中的其他成分不与盐酸或氢氧化钠反应):
步聚1:取1粒药片(每片药片的质量为0.50g)研碎
步聚2:将上研碎的药片粉末加入到40.00mL0.40mol/L稀盐酸中溶解
步聚3:用0.40mol/LNaOH溶液中和过量稀盐酸,记录消耗NaOH溶液的体积;
请回答下列问题。
(1)实验室用密度为 质量分数为36.5%的浓盐酸配制该0.40mol/L盐酸溶液240mL,应用量筒量取
质量分数为36.5%的浓盐酸配制该0.40mol/L盐酸溶液240mL,应用量筒量取___________ mL浓盐酸。
(2)实验用到的玻璃仪器有烧杯、玻璃棒、量筒和___________ 。
(3)下列操作会使配制的溶液浓度偏低的有___________ 。
A.转移溶液时,未洗涤玻璃棒和烧杯内壁
B.配制溶液前容量瓶底部有少量蒸馏水残留
C.摇匀后发现液面下降,再加水至刻度线
D.定容时俯视刻度线
E.溶液未冷却即转移到容量瓶中
(4)某同学4次测定所消耗的NaOH溶液的体积如下:
根据这个同学的实验数据,计算这种药片中氢氧化铝的质量分数为___________ %(结果保留小数点后两位)。
步聚1:取1粒药片(每片药片的质量为0.50g)研碎
步聚2:将上研碎的药片粉末加入到40.00mL0.40mol/L稀盐酸中溶解
步聚3:用0.40mol/LNaOH溶液中和过量稀盐酸,记录消耗NaOH溶液的体积;
请回答下列问题。
(1)实验室用密度为
(2)实验用到的玻璃仪器有烧杯、玻璃棒、量筒和
(3)下列操作会使配制的溶液浓度偏低的有
A.转移溶液时,未洗涤玻璃棒和烧杯内壁
B.配制溶液前容量瓶底部有少量蒸馏水残留
C.摇匀后发现液面下降,再加水至刻度线
D.定容时俯视刻度线
E.溶液未冷却即转移到容量瓶中
(4)某同学4次测定所消耗的NaOH溶液的体积如下:
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V[NaOH(aq)]/mL | 16.04 | 15.96 | 16.20 | 16.00 |
四氧化三铁(Fe3O4)俗称磁性氧化铁,在工业上应用广泛,可作催化剂、磁记录材料等。Fe3O4的一种制备方法如下:
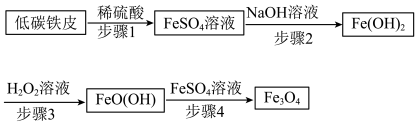
(1)低碳铁皮与稀硫酸反应时,会形成许多微小原电池。
①形成原电池时,Fe作___________ 。
A.正极 B.负极
②反应过程中,溶液的pH___________ 。
A.变大 B.变小 C.不变
(2)检验步骤1得到的FeSO4溶液中是否存在 ,可选用的试剂是___________。
,可选用的试剂是___________。
(3)实验室测定FeSO4溶液的浓度,常用K2Cr2O7标准溶液进行滴定。现称量2.940gK2Cr2O7( )固体,配制成
)固体,配制成 K2Cr2O7标准溶液。
K2Cr2O7标准溶液。
①称量时,需用到的仪器有___________ 。
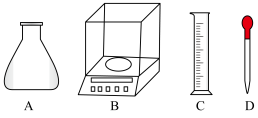
②根据计算,选用的容量瓶规格应为___________ 。
A.100mL B.250mL C.500mL D.1000mL
(4)步骤2用下图所示装置制备 。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
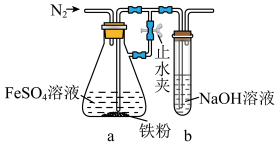
止水夹关闭前后,通入N2的作用分别为___________ 、___________ 。
(5)步骤3的反应原理为: 。反应中每消耗34gH2O2,转移的电子数为
。反应中每消耗34gH2O2,转移的电子数为___________ 。
(6)步骤4在不同时刻得到的Fe3O4粒径大小如下图所示。
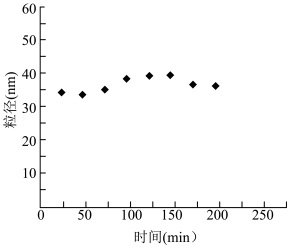
①实验过程中,Fe3O4不易形成沉淀,结合上图分析原因___________ 。
②写出一种可使Fe3O4较快形成沉淀的方法___________ 。

(1)低碳铁皮与稀硫酸反应时,会形成许多微小原电池。
①形成原电池时,Fe作
A.正极 B.负极
②反应过程中,溶液的pH
A.变大 B.变小 C.不变
(2)检验步骤1得到的FeSO4溶液中是否存在
| A.KSCN溶液 | B.KMnO4溶液 | C.稀硝酸 | D.BaCl2溶液 |
①称量时,需用到的仪器有

②根据计算,选用的容量瓶规格应为
A.100mL B.250mL C.500mL D.1000mL
(4)步骤2用下图所示装置制备

止水夹关闭前后,通入N2的作用分别为
(5)步骤3的反应原理为:
(6)步骤4在不同时刻得到的Fe3O4粒径大小如下图所示。

①实验过程中,Fe3O4不易形成沉淀,结合上图分析原因
②写出一种可使Fe3O4较快形成沉淀的方法
按要求回答问题
(1) KAl(SO4)2的电离方程式_______________________ 。
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是______________ 、_________________ (填微粒符号)。
(3) 实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取_______________ ml 该浓盐酸。
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L (标况) SO2时,转移的电子是__________ mol。
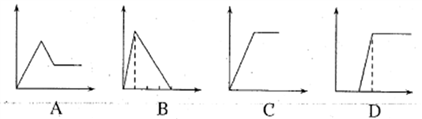
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。
(1) KAl(SO4)2的电离方程式
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是
(3) 实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L (标况) SO2时,转移的电子是
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。

溶液 | 加入的物质 | 序号 |
①AlCl3溶液 | 通入过量的NH3 | |
②Na2CO3和NaOH的溶液 | 滴入过量的盐酸 | |
③NaAlO2溶液 | 滴加稀硫酸至过量 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


