填空题 适中0.65 引用1 组卷201
硅是重要的半导体材料,构成现代电子工业的基础。硅及其化合物在工业中应用广泛,在国防和航天工业中亦有许多用途。
(1)硅原子中最外层电子排布式为___ ,该层电子的电子云有___ 种不同的伸展方向。
(2)温石棉矿是一种硅酸盐类矿物,化学式写作氧化物形式为6MgO•4SiO2•4H2O,其中原子半径最大的元素在周期表中的位置是___ 。SiO2存在与金刚石结构类似的晶体,其中硅氧原子之间以___ 相结合。
a.离子键 b.极性键 c.非极性键 d.范德华力
(3)甲硅烷(SiH4)是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下,10gSiH4自燃放出热量446kJ,请写出其燃烧的热化学方程式:___ ;
(4)SiH4的热稳定性不如CH4,其原因是___ 。
工业上硅铁可以用于冶镁。以煅白(CaO•MgO)为原料与硅铁(含硅75%的硅铁合金)混合,置于密闭设备中于1200℃发生反应:2(CaO•MgO)(s)+Si(s)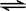 Ca2SiO4(l)+2Mg(g)
Ca2SiO4(l)+2Mg(g)
(5)常温下镁的还原性强于硅。上述方法能够获得镁的原因是:___ 。
(6)若上述反应在容积为aL的密闭容器中发生,一定能说明反应已达平衡的是___ (选填编号)。
a.反应物不再转化为生成物
b.炉内Ca2SiO4与CaO•MgO的质量比保持不变
c.反应放出的总热量不再改变
d.单位时间内,n(CaO•MgO)消耗:n(Ca2SiO4)生成=2:1
若bg煅白经tmin反应后转化率达70%,该时段内Mg的生成速率是___ 。
(1)硅原子中最外层电子排布式为
(2)温石棉矿是一种硅酸盐类矿物,化学式写作氧化物形式为6MgO•4SiO2•4H2O,其中原子半径最大的元素在周期表中的位置是
a.离子键 b.极性键 c.非极性键 d.范德华力
(3)甲硅烷(SiH4)是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下,10gSiH4自燃放出热量446kJ,请写出其燃烧的热化学方程式:
(4)SiH4的热稳定性不如CH4,其原因是
工业上硅铁可以用于冶镁。以煅白(CaO•MgO)为原料与硅铁(含硅75%的硅铁合金)混合,置于密闭设备中于1200℃发生反应:2(CaO•MgO)(s)+Si(s)
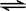 Ca2SiO4(l)+2Mg(g)
Ca2SiO4(l)+2Mg(g)(5)常温下镁的还原性强于硅。上述方法能够获得镁的原因是:
(6)若上述反应在容积为aL的密闭容器中发生,一定能说明反应已达平衡的是
a.反应物不再转化为生成物
b.炉内Ca2SiO4与CaO•MgO的质量比保持不变
c.反应放出的总热量不再改变
d.单位时间内,n(CaO•MgO)消耗:n(Ca2SiO4)生成=2:1
若bg煅白经tmin反应后转化率达70%,该时段内Mg的生成速率是
2015·上海·模拟预测
类题推荐
硅是重要的半导体材料,构成现代电子工业的基础。磷及其化合物在工业中应用广泛,在国防和航天工业中亦有许多用途。在工业上,高纯硅可以通过下列流程制取:
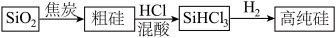
(1)基态硅原子核外电子的运动状态有___________ 种,占据的最高能层符号为___________ 。
(2)流程中由 制粗硅的反应不能说明碳的非金属性强于硅,原因是
制粗硅的反应不能说明碳的非金属性强于硅,原因是___________ 。请写出一个能说明碳的非金属性强于硅的化学方程式___________ 。
(3) 甲硅烷 是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下,
是一种无色的液体,遇到空气能爆炸性自燃,生成二氧化硅固体和水。在室温下, 自燃放出热量
自燃放出热量 ,请写出其燃烧的热化学方程式:
,请写出其燃烧的热化学方程式:___________ 。
(4) 的热稳定性不如
的热稳定性不如 ,其原因是
,其原因是___________ 。
(5)工业上硅铁可以用于冶镁。以煅白 为原料与硅铁(含硅
为原料与硅铁(含硅 的硅铁合金)混合,置于密闭设备中于
的硅铁合金)混合,置于密闭设备中于 发生反应:
发生反应: ,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:
,已知常温下镁的还原性强于硅。利用平衡移动原理解释上述方法能够获得镁的原因:___________ 。
(6)有关碳和硅的有关化学键链能如下所示。
硅也有系列氢化物,如甲硅烷等。但硅烷在种类和数量上都远不如烷烃多,原因是___________ 。

(1)基态硅原子核外电子的运动状态有
(2)流程中由
(3) 甲硅烷
(4)
(5)工业上硅铁可以用于冶镁。以煅白
(6)有关碳和硅的有关化学键链能如下所示。
| 化学键 | ||||||
| 键能/ | 356 | 413 | 336 | 226 | 318 | 452 |
镁元素在自然界分布广泛,是人体的必需元素之一。工业上可用硅热法(Pidgeon法)冶炼镁,以煅白(CaO·MgO,M = 96 g/mol)为原料与硅铁(含硅75%)混合置于密闭还原炉,1200℃下发生反应:2(CaO·MgO)(s) + Si(s)⇌Ca2SiO4 (l)+2Mg(g);完成下列填空:
(1)已知还原性Mg > Si,上述反应仍能发生的原因是_______ 。
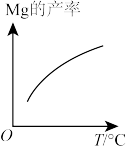
(2)由图推测上述反应正向为_______ (填“吸热”或“放热”)反应。
(3)若还原炉体积不变,能证明上述反应达到平衡的是_______ (选填序号)。
a.平衡常数到达最大值
b.反应物不再转化为生成物
c.炉内Ca2SiO4与CaO·MgO的质量比保持不变
d.单位时间内,n(CaO·MgO)消耗 :n(Ca2SiO4)生成 = 2:1
(4)平衡后若其他条件不变,将还原炉体积缩小一半,则达到新平衡时Mg(g)的浓度将_______ (填“升高”“降低”或“不变”)。
(5)若还原炉容积为400 m3,原料中煅白质量为9600 kg,5小时后,测得煅白的转化率为50%,计算这段时间内Mg的生成速率_______ mol/(L·h)。
(6)工业上也可用电解法来制备镁。相关化合物的熔点如表所示:
①镁原子核外有_______ 种能量不同的电子,它们的运动状态有_______ 种。
②MgCl2的电子式为_______ ;
③判断工业上应选择MgCl2还是MgO作为电解原料并说明理由_______
(1)已知还原性Mg > Si,上述反应仍能发生的原因是
(2)由图推测上述反应正向为

(3)若还原炉体积不变,能证明上述反应达到平衡的是
a.平衡常数到达最大值
b.反应物不再转化为生成物
c.炉内Ca2SiO4与CaO·MgO的质量比保持不变
d.单位时间内,n(CaO·MgO)消耗 :n(Ca2SiO4)生成 = 2:1
(4)平衡后若其他条件不变,将还原炉体积缩小一半,则达到新平衡时Mg(g)的浓度将
(5)若还原炉容积为400 m3,原料中煅白质量为9600 kg,5小时后,测得煅白的转化率为50%,计算这段时间内Mg的生成速率
(6)工业上也可用电解法来制备镁。相关化合物的熔点如表所示:
| MgCl2 | MgO | |
| 熔点/℃ | 712 | 2850 |
①镁原子核外有
②MgCl2的电子式为
③判断工业上应选择MgCl2还是MgO作为电解原料并说明理由
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 2TiCl4(g)+ 2FeCl3(g) + 6CO(g) – Q (Q>0)
2TiCl4(g)+ 2FeCl3(g) + 6CO(g) – Q (Q>0)

