解答题-无机推断题 适中0.65 引用2 组卷159
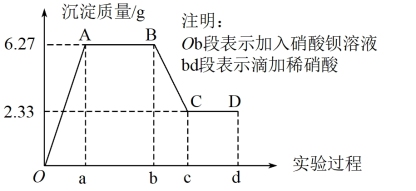
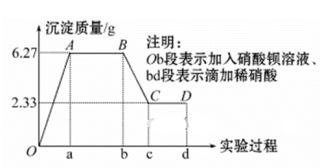
Ⅰ.下列是某研究性学习小组对某无色水样成分的检测过程,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子,该小组同学取了100ml水样进行实验:向水样中先滴加硝酸钡溶液,再滴加1mol·L-1硝酸,实验过程中沉淀质量与所加试剂量的关系变化如下图所示:
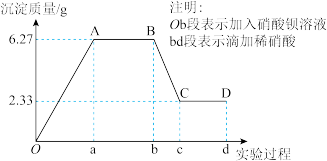
(1)仅凭观察 可知该水样中一定不含有的阳离子是____ 。
(2)由B点到C点变化过程中消耗硝酸的体积为___ mL。
(3)试根据实验结果推测K+是否存在___ (填“是”或“否”)若存在,其物质的量浓度的范围是___ mol·L-1(若不存在,则不必回答)。
(4)设计简单实验验证原水样中可能存在的离子_____________ (写出实验步骤、现象和结论)。
Ⅱ.湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
(1)写出并配平湿法制高铁酸钾反应的离子方程式:____________ 。
(2)若反应过程中转移了0.3mol电子,则还原产物的物质的量为___ mol。
(3)低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),原因是______ 。

(1)
(2)由B点到C点变化过程中消耗硝酸的体积为
(3)试根据实验结果推测K+是否存在
(4)设计简单实验验证原水样中可能存在的离子
Ⅱ.湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
(1)写出并配平湿法制高铁酸钾反应的离子方程式:
(2)若反应过程中转移了0.3mol电子,则还原产物的物质的量为
(3)低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),原因是
20-21高三上·福建莆田·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网