解答题-工业流程题 适中0.65 引用1 组卷101
某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
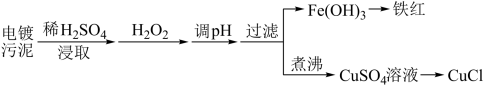
(1)酸浸后加入H2O2的目的是__ ,调pH的最适宜范围为__ 。
(2)调pH过程中加入的试剂最好是__ 。
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
(3)煮沸CuSO4溶液的原因是__ 。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式__ 。
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是__ 。
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol﹒L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol﹒L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数___ 。

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是
(2)调pH过程中加入的试剂最好是
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
(3)煮沸CuSO4溶液的原因是
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是
(5)称取所制备的CuCl样品0.2500g置于一定量的0.5mol﹒L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol﹒L-1的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液25.00mL。有关的化学反应为Fe3++CuCl=Fe2++Cu2++Cl-,Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数
19-20高二上·云南曲靖·期末
类题推荐
某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

(1)酸浸后加入H2O2的目的是_____________ 。调pH步骤中加入的试剂最好是_____________ (填化学式)。实验室进行过滤操作所用到的玻璃仪器有_____________ 。
(2)向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式_____________ 。
(3)CuCl产品中CuCl的质量分数大于96.50%为国家合格标准。称取所制备的CuCl样品0.2500g置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol/L的Ce(SO4)2溶液滴定,到达滴定终点时消耗Ce(SO4)2溶液24.60mL。有关的化学反应为: Fe3++CuCl═Fe2++Cu2++Cl-,Ce4++Fe2+═Fe3++Ce3+,通过计算说明该CuCl样品_______________ (填“符合”或“不符合”)国家标准。
(4)25℃时,Ksp[Fe(OH]3]=4.0×10-38.Fe3+发生水解反应Fe3++3H2O Fe(OH)3+3H+,该反应的平衡常数为
Fe(OH)3+3H+,该反应的平衡常数为_____________ .

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(2)向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式
(3)CuCl产品中CuCl的质量分数大于96.50%为国家合格标准。称取所制备的CuCl样品0.2500g置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol/L的Ce(SO4)2溶液滴定,到达滴定终点时消耗Ce(SO4)2溶液24.60mL。有关的化学反应为: Fe3++CuCl═Fe2++Cu2++Cl-,Ce4++Fe2+═Fe3++Ce3+,通过计算说明该CuCl样品
(4)25℃时,Ksp[Fe(OH]3]=4.0×10-38.Fe3+发生水解反应Fe3++3H2O
 Fe(OH)3+3H+,该反应的平衡常数为
Fe(OH)3+3H+,该反应的平衡常数为 某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

(1)酸浸后加入H2O2的目的是_________________ 。
(2)向CuSO4 溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl 沉淀,写出该反应的离子方程式____________________ 。
(3)为保证产品的纯度,调节pH 的范围为___________ ,调pH 值可以选用(填字母)_______ 。
a.Cu(OH)2 b.H2SO4 c.NH3•H2O d.Na2CO3 e.CuO
(4)煮沸硫酸铜溶液的原因是____________ 。
(5)CuCl产品中CuCI的质量分数大于96.50%为国家合格标准。称取所制备的CuCl样品0.2500g置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000 mol /L 的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液24.80 mL。有关的化学反应为Fe3+ +CuCl=Fe2++Cu2+ +Cl-,Ce4++Fe2+=Fe3++Ce3+。则CuCl 产品中CuCl 的质量分数为_____ 。
(6)已知Fe(OH)3 能与次氯酸钾碱性溶液发生反应生成具有强氧化性的高铁酸钾(K2FeO4),高铁酸钾可作为新型多功能水处理剂的原因是___________________ 。

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(2)向CuSO4 溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl 沉淀,写出该反应的离子方程式
(3)为保证产品的纯度,调节pH 的范围为
a.Cu(OH)2 b.H2SO4 c.NH3•H2O d.Na2CO3 e.CuO
(4)煮沸硫酸铜溶液的原因是
(5)CuCl产品中CuCI的质量分数大于96.50%为国家合格标准。称取所制备的CuCl样品0.2500g置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000 mol /L 的Ce(SO4)2溶液滴定,到达终点时消耗Ce(SO4)2溶液24.80 mL。有关的化学反应为Fe3+ +CuCl=Fe2++Cu2+ +Cl-,Ce4++Fe2+=Fe3++Ce3+。则CuCl 产品中CuCl 的质量分数为
(6)已知Fe(OH)3 能与次氯酸钾碱性溶液发生反应生成具有强氧化性的高铁酸钾(K2FeO4),高铁酸钾可作为新型多功能水处理剂的原因是
某工厂的电镀污泥中含有铜、铁等金属化合物,为实现资源的回收利用并有效防止环境污染,设计如图工艺流程。
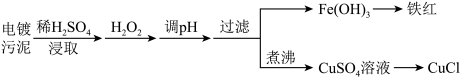
(1)酸浸后加入H2O2的目的是___ ,调pH的最适宜范围为__ 。
(2)调pH过程中加入的试剂最好是__ 。
A .NaOH B .CuO C .NH3·H2O D .HCl
(3)煮沸CuSO4溶液的原因是__ 。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式___ 。

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(2)调pH过程中加入的试剂最好是
A .NaOH B .CuO C .NH3·H2O D .HCl
(3)煮沸CuSO4溶液的原因是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


