解答题-实验探究题 较难0.4 引用1 组卷138
草酸 溶液与酸性
溶液与酸性 溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
【查阅资料】 溶液氧化
溶液氧化 的反应历程为:
的反应历程为:
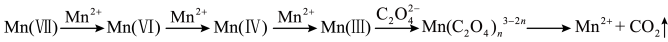
【提出假设】假设1:该反应为放热
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是______ 。
【设计、完成实验】
 称取
称取______ g草酸晶体 ,配置500mL
,配置500mL
 溶液。
溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和______ 。
②下列操作会使所配溶液浓度偏低的是______  填下列选项的字母序号
填下列选项的字母序号 。
。
A 称取草酸晶体时,将草酸晶体放在托盘天平右盘
B 定容时俯视刻度线
C 将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D 摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
 完成探究,记录数据
完成探究,记录数据
则
______ ,假设______ 成立。
 由于
由于 能氧化水中有机物等因素,配置好稳定的
能氧化水中有机物等因素,配置好稳定的 溶液,其浓度需标定.取
溶液,其浓度需标定.取

 溶液于锥形瓶中,加入10mL
溶液于锥形瓶中,加入10mL 稀硫酸,用
稀硫酸,用 中
中 溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗
溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗 溶液
溶液 ,则草酸溶液与酸性
,则草酸溶液与酸性 溶液反应的离子方程式为:
溶液反应的离子方程式为:______ ,上述实验中 溶液的物质的量浓度为
溶液的物质的量浓度为______ 。
【查阅资料】
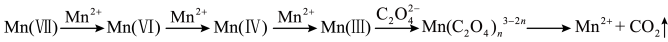
【提出假设】假设1:该反应为放热
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是
【设计、完成实验】
①在上述过程中必须用到的2种定量仪器是托盘天平和
②下列操作会使所配溶液浓度偏低的是
A 称取草酸晶体时,将草酸晶体放在托盘天平右盘
B 定容时俯视刻度线
C 将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D 摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
| 实验 编号 | 烧杯中所加试剂及用量 | 控制条件 | 溶液褪 色时间 | |||
| 等浓度 | 稀硫酸 | |||||
| 1 | 30 | 20 | 30 | 20 | 18 | |
| 2 | 30 | 20 | 30 | 20 | 水浴控制温度 | 15 |
| 3 | 30 | 20 | 30 | 20 | 加入少量 | |
| 4 | 30 | 20 | x | 20 | 加入5mL | 18 |
2020高三·全国·专题练习
类题推荐
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,存在与自然界的植物中,其晶体(H2C2O4·2H2O)无色,101℃开始熔化,易溶于水,受热脱水、升华,170℃时开始分解,其钠盐和钾盐易溶于水。而其钙盐难溶于水。
(1)依据表中给出的数据判断下列化学方程式可能正确的是_____________ (填序号)
两种多元酸是电离常数(25℃)
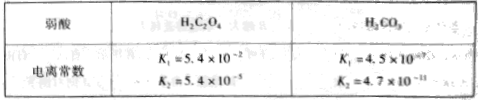

(2)某化学兴趣小组的同学选用如图所示的部分装置(可以重复选用)进行商业,验证草酸的分解产物(已知:H2C2O4 CO2↑+CO↑+H2O↑)
CO2↑+CO↑+H2O↑)
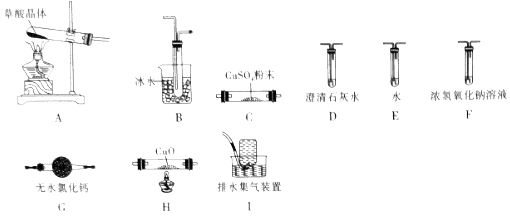
如果气体流向为从左到右,装置依次连接的合理顺序为_____________ 。
(3)草酸溶液能使酸性高锰酸钾溶液褪色,其反应历程为:

①称取_____________ g草酸晶体,配制250mL0.10mol/LH2C2O4溶液
②在上述过程中必须用到的2种定量仪器是_____________ 和_____________ 。
③下列操作会使所配溶液浓度偏高的是_____________ (填序号)
④写出草酸溶液与酸性KMnO4溶液反应的离子方程式:_____________ 。
⑤由于KMnO4能氧化水中的有机物等因素,为了配制稳定的KMnO4溶液,其浓度需标定,取10.00mL0.10mol/LH2C2O4溶液于锥形瓶中,加入10mL0.50mol/LH2SO4溶液、用KMnO4溶液滴定至锥形瓶中溶液颜色恰好_____________ ,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液40.00mL,则上述实验中KMnO4溶液的物质的量浓度为_____________ 。
(1)依据表中给出的数据判断下列化学方程式可能正确的是
两种多元酸是电离常数(25℃)

(2)某化学兴趣小组的同学选用如图所示的部分装置(可以重复选用)进行商业,验证草酸的分解产物(已知:H2C2O4
 CO2↑+CO↑+H2O↑)
CO2↑+CO↑+H2O↑)
如果气体流向为从左到右,装置依次连接的合理顺序为
(3)草酸溶液能使酸性高锰酸钾溶液褪色,其反应历程为:

①称取
②在上述过程中必须用到的2种定量仪器是
③下列操作会使所配溶液浓度偏高的是
| A.称取草酸晶体时,将草酸晶体放在托盘天平右盘 |
| B.定容时俯视刻度线 |
| C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水 |
| D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容 |
④写出草酸溶液与酸性KMnO4溶液反应的离子方程式:
⑤由于KMnO4能氧化水中的有机物等因素,为了配制稳定的KMnO4溶液,其浓度需标定,取10.00mL0.10mol/LH2C2O4溶液于锥形瓶中,加入10mL0.50mol/LH2SO4溶液、用KMnO4溶液滴定至锥形瓶中溶液颜色恰好
高锰酸钾是一种重要的化学试剂,其溶液不很稳定,在酸性条件下会分解生成二氧化锰和氧气,在中性或弱碱性溶液中分解速度很慢,见光分解速度加快。
(1)酸性条件下高锰酸钾溶液分解的离子方程式____________________________ 。
(2)请配平高锰酸钾溶液与草酸钠Na2C2O4溶液在酸性条件下反应的离子方程式:
______MnO +______C2O
+______C2O +______H+=______Mn2++______CO2↑+____
+______H+=______Mn2++______CO2↑+____
________
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如下表:
请分析高锰酸钾溶液褪色时间变化的原因__________ 。
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠Na2C2O4(相对分子质量134.0)来标定高锰酸钾溶液的浓度。他们准确称取1.340g纯净的草酸钠配成250mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4溶液滴定。
① 高锰酸钾溶液应装在_____________ (填下图中的仪器编号)。
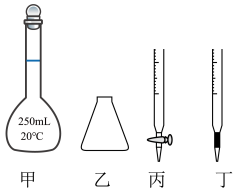
② 为了防止高锰酸钾在酸性条件下分解而造成误差,滴定时应注意的是_____________ 。
③当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为_________________ 。
④若在实验过程中存在下列操作,其中会使所测KMnO4浓度偏低的是______________ 。
A. 未润洗盛放KMnO4的滴定管
B. 滴定前尖嘴部分无气泡,滴定终点时出现气泡
C. 定容时,俯视刻度线
D. 锥形瓶用水洗之后未用待测液润洗
(1)酸性条件下高锰酸钾溶液分解的离子方程式
(2)请配平高锰酸钾溶液与草酸钠Na2C2O4溶液在酸性条件下反应的离子方程式:
______MnO
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如下表:
| 滴入高锰酸钾溶液的次序(每滴溶液的体积相同) | 高锰酸钾溶液紫色褪去的时间 |
| 先滴入第1滴 | 1min |
| 褪色后再滴入第2滴 | 15s |
| 褪色后再滴入第3滴 | 3s |
| 褪色后再滴入第4滴 | 1s |
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠Na2C2O4(相对分子质量134.0)来标定高锰酸钾溶液的浓度。他们准确称取1.340g纯净的草酸钠配成250mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4溶液滴定。
① 高锰酸钾溶液应装在

② 为了防止高锰酸钾在酸性条件下分解而造成误差,滴定时应注意的是
③当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为
④若在实验过程中存在下列操作,其中会使所测KMnO4浓度偏低的是
A. 未润洗盛放KMnO4的滴定管
B. 滴定前尖嘴部分无气泡,滴定终点时出现气泡
C. 定容时,俯视刻度线
D. 锥形瓶用水洗之后未用待测液润洗
回归、改进、拓展教材实验,是高考化学实验考查的常见形式。
I.甲组同学在进行《必修二》实验2-5“Fe3+离子在H2O2溶液分解实验中的催化作用”时,进行了以下探究。基于目前学过的元素周期表的相关知识,该小组推测了同为第四周期第VIII族的Fe、Co、Ni可能有相似的催化机理。
【查阅资料】:钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。其中CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)也可用作H2O2分解的催化剂,具有较高的活性。
(1)写出H2O2溶液在Fe3+催化下分解的化学方程式__________________________________。
(2)①该催化剂中铁元素的化合价为 。
②下图表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高,由此推测Co2+、Ni2+两种离子中催化效果更好的是 。

II.乙组同学在进行《选修四》实验2-2“草酸溶液浓度对酸性高锰酸钾溶液褪色时间的影响”时,发现溶液褪色总是先慢后快,该小组设计了如下过程探究其原因:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为(流程中“III”等为Mn的价态):

【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+ 对该反应有催化作用
假设3:K+ 对该反应有催化作用
【设计、完成实验】
(3)称取 g草酸晶体(H2C2O4·2H2O),配制500 mL 0.10 mol/L H2C2O4溶液。在上述过程中必须用到的2种定量仪器是托盘天平和
(4)完成探究,记录数据
仔细阅读分析表中数据,回答问题:
x = mL,假设__________成立(填“1” 、“2”或“3”)
I.甲组同学在进行《必修二》实验2-5“Fe3+离子在H2O2溶液分解实验中的催化作用”时,进行了以下探究。基于目前学过的元素周期表的相关知识,该小组推测了同为第四周期第VIII族的Fe、Co、Ni可能有相似的催化机理。
【查阅资料】:钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。其中CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)也可用作H2O2分解的催化剂,具有较高的活性。
(1)写出H2O2溶液在Fe3+催化下分解的化学方程式__________________________________。
(2)①该催化剂中铁元素的化合价为 。
②下图表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高,由此推测Co2+、Ni2+两种离子中催化效果更好的是 。

II.乙组同学在进行《选修四》实验2-2“草酸溶液浓度对酸性高锰酸钾溶液褪色时间的影响”时,发现溶液褪色总是先慢后快,该小组设计了如下过程探究其原因:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为(流程中“III”等为Mn的价态):

【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+ 对该反应有催化作用
假设3:K+ 对该反应有催化作用
【设计、完成实验】
(3)称取 g草酸晶体(H2C2O4·2H2O),配制500 mL 0.10 mol/L H2C2O4溶液。在上述过程中必须用到的2种定量仪器是托盘天平和
(4)完成探究,记录数据
| 实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s) | |||
| 0.10 mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50 mol/L 稀硫酸 | |||
| 1 | 30 | 20 | 30 | 20 | 18 | |
| 2 | 30 | 20 | 30 | 20 | 水浴控制温度65 ℃ | 15 |
| 3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
| 4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/L K2SO4溶液 | 18 |
仔细阅读分析表中数据,回答问题:
x = mL,假设__________成立(填“1” 、“2”或“3”)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


