解答题-实验探究题 较难0.4 引用2 组卷463
以环己醇(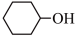 )为原料制取己二酸[HOOC(CH2)4COOH]的实验流程如下:
)为原料制取己二酸[HOOC(CH2)4COOH]的实验流程如下:
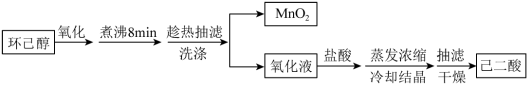
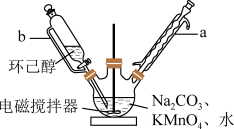
其中“氧化”的实验过程:在250mL四口烧瓶中加入50mL水和3.18g碳酸钠,低速搅拌至碳酸钠溶解,缓慢加入9.48g(约0.060mol)高锰酸钾,按图示搭好装置,打开电动搅拌,加热至35℃,滴加3.2mL(约0.031mol)环己醇,发生的主要反应为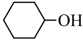
 KOOC(CH2)4COOK ΔH<0
KOOC(CH2)4COOK ΔH<0
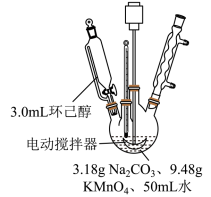
(1)“氧化”过程应采用___________ 加热。(填标号)
A.热水浴 B.酒精灯 C.煤气灯 D.电炉
(2)“氧化”过程,不同环己醇滴加速度下,溶液温度随时间变化曲线如图,为保证产品纯度,应选择的滴速为___________ s/滴。
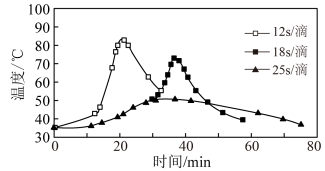
(3)为证明“氧化”反应已结束,在滤纸上点1滴混合物,若观察到_____ ,则表明反应已经完成.
(4)“趁热抽滤”后,用________ 进行洗涤。
(5)室温下,相关物质溶解度如表。“蒸发浓缩”过程中,为保证产品纯度及产量,应浓缩溶液体积至__ (填标号)。
A.5mL B. 10mL C. 15mL D. 20mL
(6)称取己二酸(Mr=146g/mol)样品0.2920g,用新煮沸的50mL热水溶解,滴入2滴酚酞试液,用0.2000 mol/LNaOH溶液滴定至终点,进行平行实验及空白实验后,消耗NaOH的平均体积为19.70mL.
①NaOH溶液应装于_______ (填仪器名称).
②己二酸样品的纯度为___________ .
 )为原料制取己二酸[HOOC(CH2)4COOH]的实验流程如下:
)为原料制取己二酸[HOOC(CH2)4COOH]的实验流程如下:
其中“氧化”的实验过程:在250mL四口烧瓶中加入50mL水和3.18g碳酸钠,低速搅拌至碳酸钠溶解,缓慢加入9.48g(约0.060mol)高锰酸钾,按图示搭好装置,打开电动搅拌,加热至35℃,滴加3.2mL(约0.031mol)环己醇,发生的主要反应为


(1)“氧化”过程应采用
A.热水浴 B.酒精灯 C.煤气灯 D.电炉
(2)“氧化”过程,不同环己醇滴加速度下,溶液温度随时间变化曲线如图,为保证产品纯度,应选择的滴速为

(3)为证明“氧化”反应已结束,在滤纸上点1滴混合物,若观察到
(4)“趁热抽滤”后,用
(5)室温下,相关物质溶解度如表。“蒸发浓缩”过程中,为保证产品纯度及产量,应浓缩溶液体积至
| 化学式 | 己二酸 | NaCl | KCl |
| 溶解度g/100g 水 | 1.44 | 35.1 | 33.3 |
(6)称取己二酸(Mr=146g/mol)样品0.2920g,用新煮沸的50mL热水溶解,滴入2滴酚酞试液,用0.2000 mol/LNaOH溶液滴定至终点,进行平行实验及空白实验后,消耗NaOH的平均体积为19.70mL.
①NaOH溶液应装于
②己二酸样品的纯度为
20-21高三上·福建厦门·期末
类题推荐
(1)装置图中仪器A的名称为___________ 。
(2)“氧化”过程应采用___________加热(填标号)。
(3)“氧化”过程中,当环己醇滴速不同时,溶液温度随时间变化曲线如下图所示,实验过程中应选择的环己醇滴速为___________ 滴/min。___________ (填化学式)。
(5)已知:不同温度下,相关物质在水中的溶解度如下表:
①己二酸晶体“洗涤”的方法为___________ (填字母)。
A.用乙醇洗涤 B.用热水洗涤 C.用冷水洗涤
②除去己二酸晶体中含有的氯化钠杂质通常采取的实验方法为___________ 。
(6)实验时称取10.0g环己醇(M=100g/mol),最终得到纯净的己二酸(M=146g/mol)晶体11.68g,则该实验中己二酸的产率为___________ (保留两位有效数字)。
以环己醇(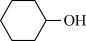 )为原料制取己二酸[ HOOC (CH2)4COOH]的实验流程如图:
)为原料制取己二酸[ HOOC (CH2)4COOH]的实验流程如图:

I.己二酸的制备:
其中“氧化”的实验过程为:250mL三颈烧瓶中加入50mL水和3.18g碳酸钠,低速搅拌至碳酸钠溶解,缓慢加入9. 48g (约0. 06mol)高锰酸钾,按图示1组装好装置,打开磁力搅拌器,加热至35°C,滴加3. 2mL (约0. 031mol)环己醇,发生的主要反应为: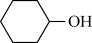
 KOOC (CH2)4COOK△H<0
KOOC (CH2)4COOK△H<0
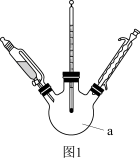
(1)图1中a仪器的名称为___________ 。
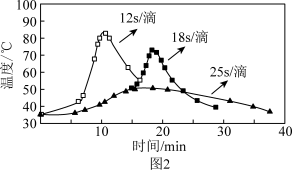
(2)“氧化”过程,不同环己醇滴加速度下,溶液温度随时间变化曲线如图2,为保证产品纯度,应选择的滴速为___________ s/滴(“s/滴”指两滴间的间隔时间),选择的理由是___________ 。
(3)采取“趁热抽滤”的原因是:___________ 。
(4)室温下,相关物质溶解度g/100g水为:己二酸-1.44g,NaCl-35. 1g,KCl-33.3g。“蒸发浓缩”过程中,为保证产品纯度及产量,应浓缩溶液体积至___________ (填标号)。
II.己二酸纯度的测定
称取己二酸(Mr= 146g/mol)样品wg,用新煮沸的一定量热水溶解,滴入2滴酚酞试液,用amol/LNaOH溶液滴定至终点,进行平行实验及空白实验后,消耗NaOH的平均体积为bmL。
(5)滴定终点的现象是___________ 。请计算己二酸样品的纯度___________ 。(用题目中所给的字母表达)
 )为原料制取己二酸[ HOOC (CH2)4COOH]的实验流程如图:
)为原料制取己二酸[ HOOC (CH2)4COOH]的实验流程如图:
I.己二酸的制备:
其中“氧化”的实验过程为:250mL三颈烧瓶中加入50mL水和3.18g碳酸钠,低速搅拌至碳酸钠溶解,缓慢加入9. 48g (约0. 06mol)高锰酸钾,按图示1组装好装置,打开磁力搅拌器,加热至35°C,滴加3. 2mL (约0. 031mol)环己醇,发生的主要反应为:


(1)图1中a仪器的名称为
(2)“氧化”过程,不同环己醇滴加速度下,溶液温度随时间变化曲线如图2,为保证产品纯度,应选择的滴速为

(3)采取“趁热抽滤”的原因是:
(4)室温下,相关物质溶解度g/100g水为:己二酸-1.44g,NaCl-35. 1g,KCl-33.3g。“蒸发浓缩”过程中,为保证产品纯度及产量,应浓缩溶液体积至___________ (填标号)。
| A.5mL | B.15mL | C.30mL | D.50mL |
II.己二酸纯度的测定
称取己二酸(Mr= 146g/mol)样品wg,用新煮沸的一定量热水溶解,滴入2滴酚酞试液,用amol/LNaOH溶液滴定至终点,进行平行实验及空白实验后,消耗NaOH的平均体积为bmL。
(5)滴定终点的现象是
己二酸[HOOC(CH2)4COOH]是一种重要的工业原料,通常为白色结晶体,微溶于冷水,易溶于热水和乙醇。实验室以环己醇(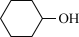 )为原料制取己二酸实验流程如图:
)为原料制取己二酸实验流程如图:
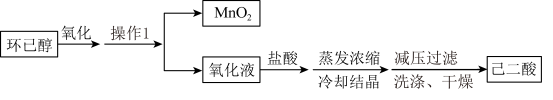
已知:“氧化”过程发生的主要反应为:
KOOC(CH2)4 COOK △H<0
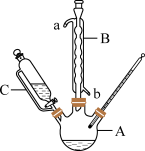
(1)装置图中仪器A的名称为
(2)“氧化”过程应采用___________加热(填标号)。
| A.酒精灯 | B.水浴 | C.油浴 | D.电炉 |
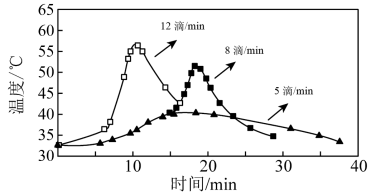
(5)已知:不同温度下,相关物质在水中的溶解度如下表:
| 物质 | 己二酸 | 氯化钠 | 氯化钾 |
| 25℃时溶解度/g | 2.1 | 36.1 | 34.3 |
| 70℃时溶解度/g | 68 | 37.8 | 48 |
| 100℃时溶解度/g | 160 | 39.5 | 56.3 |
A.用乙醇洗涤 B.用热水洗涤 C.用冷水洗涤
②除去己二酸晶体中含有的氯化钠杂质通常采取的实验方法为
(6)实验时称取10.0g环己醇(M=100g/mol),最终得到纯净的己二酸(M=146g/mol)晶体11.68g,则该实验中己二酸的产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网