解答题-工业流程题 较难0.4 引用1 组卷141
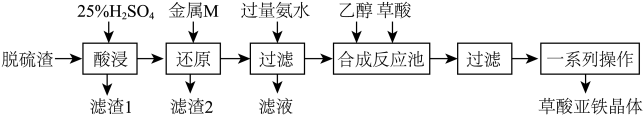
草酸亚铁是合成锂离子电池正极材料磷酸亚铁锂的原料。某工厂以炼钢厂的脱硫渣(主要成分是Fe2O3)为原料生产电池级草酸亚铁晶体的工艺流程如下:
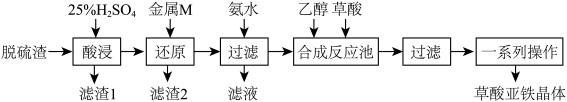
(1)要提高“酸浸”速率,宜采取的措施有___ (填两条)。
(2)写出“还原”过程中既是化合反应又是氧化还原反应的离子方程式___ 。
(3)滤渣2中含有的TiOSO4在热水中易水解,生成H2TiO3,该反应的化学方程式为___ 。
(4)“滤液”经处理后得到一种化肥,其化学式为___ 。“一系列操作”指___ 。
(5)已知:298K时,Ksp[Fe(OH)2]=4.0×10-17,当离子浓度≤1.0×10-5mol∙L-1时,视该离子已完全沉淀。上述流程中,加“氨水”调pH的范围为___ (lg2≈0.3)。
(6)草酸亚铁晶体(FeC2O4∙2H2O)纯度的测定:准确称取mg草酸亚铁晶体于锥形瓶中,加入一定量的稀硫酸溶液,并加热至50℃,用cmol∙L-1KMnO4标准溶液滴定,达到滴定终点时,用去标准溶液VmL。滴定反应(未配平):FeC2O4∙2H2O+KMnO4+H2SO4→Fe2(SO4)3+CO2+MnSO4+K2SO4+H2O;则样品中FeC2O4∙2H2O的纯度为___ %(用含有m、c、V的代数式表示);若草酸亚铁晶体失去部分结晶水,测得的结果___ (填“偏高”“偏低”或“无影响”)。

(1)要提高“酸浸”速率,宜采取的措施有
(2)写出“还原”过程中既是化合反应又是氧化还原反应的离子方程式
(3)滤渣2中含有的TiOSO4在热水中易水解,生成H2TiO3,该反应的化学方程式为
(4)“滤液”经处理后得到一种化肥,其化学式为
(5)已知:298K时,Ksp[Fe(OH)2]=4.0×10-17,当离子浓度≤1.0×10-5mol∙L-1时,视该离子已完全沉淀。上述流程中,加“氨水”调pH的范围为
(6)草酸亚铁晶体(FeC2O4∙2H2O)纯度的测定:准确称取mg草酸亚铁晶体于锥形瓶中,加入一定量的稀硫酸溶液,并加热至50℃,用cmol∙L-1KMnO4标准溶液滴定,达到滴定终点时,用去标准溶液VmL。滴定反应(未配平):FeC2O4∙2H2O+KMnO4+H2SO4→Fe2(SO4)3+CO2+MnSO4+K2SO4+H2O;则样品中FeC2O4∙2H2O的纯度为
2020高三·全国·专题练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

 ”应进行的操作步骤的名称是
”应进行的操作步骤的名称是