解答题-结构与性质 较难0.4 引用1 组卷154
坦桑石是一种世界公认的新兴宝石,这种宝石于1967年首次在赤道雪山脚下的阿鲁沙地区被发现。坦桑石的主要化学成分为 ,还可含有V、Cr、Mn等元素。
,还可含有V、Cr、Mn等元素。
 下列状态的铝中,电离最外层的一个电子所需能量最大的是
下列状态的铝中,电离最外层的一个电子所需能量最大的是________  填序号
填序号 。
。
①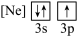 ②
②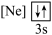 ③
③ ④
④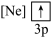
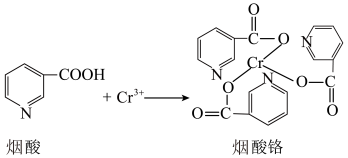
 烟酸铬是铬的一种化合物,其合成过程如下:
烟酸铬是铬的一种化合物,其合成过程如下:
 核外电子排布式为
核外电子排布式为________ 。
 、C、N、O的电负性由大到小的顺序是
、C、N、O的电负性由大到小的顺序是_________ 。
 烟酸中碳、氮原子的杂化方式分别为
烟酸中碳、氮原子的杂化方式分别为________ 、________ 。
 分子中的大
分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数
键的电子数 如二氧化碳分子中的大
如二氧化碳分子中的大 键可表示为
键可表示为 ,则烟酸中的大
,则烟酸中的大 键应表示为
键应表示为___________ 。
 、
、 都极易水解。
都极易水解。 、
、 都属于
都属于______  填“极性”或“非极性”
填“极性”或“非极性” 分子,其熔点的关系为
分子,其熔点的关系为
________  填“
填“ ”“
”“ ”或“
”或“ ”
” 。
。
 将Mn掺入GaAs晶体
将Mn掺入GaAs晶体 图甲
图甲 可得到稀磁性半导体材料
可得到稀磁性半导体材料 图乙
图乙 ,图甲、图乙晶体结构不变。
,图甲、图乙晶体结构不变。
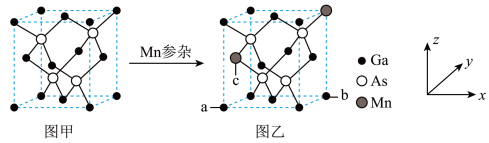
 图乙中a点和b点的原子坐标参数分别为
图乙中a点和b点的原子坐标参数分别为 0,
0, 和
和 1,
1, ,则c点的原子坐标参数为
,则c点的原子坐标参数为________ 。
 设图甲晶体的密度为
设图甲晶体的密度为 ,用
,用 表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为
表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为________________ pm。
①
 ②
②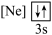 ③
③ ④
④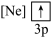


2020高三·全国·专题练习
类题推荐
Mn能改善钢材热加工性能,并改善钢材的冷脆倾向,同时不显著降低钢材的塑性、冲击韧性。根据要求回答下列问题:
(1) 的核外电子排布式为
的核外电子排布式为_______ ,
基态Mn原子能级最高的电子的电子云轮廓图形状为_______ 。
(2)Fe、Mn元素的部分电离能数据如下表:
从上表两元素部分电离能数据的比较可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,原因是
再失去一个电子难,原因是_______ 。
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与 形成黄色的配合物,其结构为
形成黄色的配合物,其结构为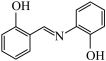 。
。
①锰试剂分子中,电负性最大的原子是_______ ,采取 杂化的原子是
杂化的原子是_______ ;
②锰试剂分子中能与 形成配位键的原子是
形成配位键的原子是_______ 。
(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。
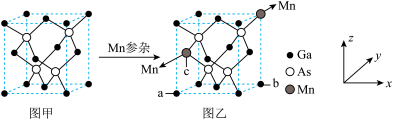
①图乙中a点和c点的原子坐标参数分别为(0,0,0)和 ,则b点的原子坐标参数为
,则b点的原子坐标参数为_______ ;
②设图甲晶体的密度为 ,设
,设 表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为
表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为_______ pm(用含 、
、 的关系式表示最简化的计算式即可)。
的关系式表示最简化的计算式即可)。
(1)
基态Mn原子能级最高的电子的电子云轮廓图形状为
(2)Fe、Mn元素的部分电离能数据如下表:
| 元素 | Fe | Mn | |
| 电离能/( | 759 | 717 | |
| 1561 | 1509 | ||
| 2957 | 3248 | ||
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与
 。
。①锰试剂分子中,电负性最大的原子是
②锰试剂分子中能与
(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。

①图乙中a点和c点的原子坐标参数分别为(0,0,0)和
②设图甲晶体的密度为
磷酸亚铁锂(LiFeO4)是新型锂离子电池的首选电极材料,该电池具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 、氮化硼、LiCl和苯胺等作为原料制备。回答下列问题:
、氮化硼、LiCl和苯胺等作为原料制备。回答下列问题:
(1)基态Fe原子的核外电子排布式为_______ ,有______ 个未成对电子。
(2)苯胺( )分子中C原子与N原子的杂化方式分别为
)分子中C原子与N原子的杂化方式分别为_______ 、______ ,苯胺与甲苯(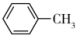 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点( ℃)、沸点(110.6℃),原因是
℃)、沸点(110.6℃),原因是______ 。分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如 分子中的大π键可表示为
分子中的大π键可表示为 ),则
),则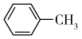 分子中的大π键应表示为
分子中的大π键应表示为_______ 。
(3)下列碳原子电子排布图表示的状态中,能量最低的是___________(填标号)。
(4)氮化硼(BN)是一种重要的功能陶瓷材料。可通过下列反应得到:B2O3+2□ 2BN+3H2O
2BN+3H2O
①□内物质的空间构型为______ 。
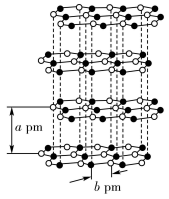
②在与石墨结构相似的六方氮化硼晶体中,晶体的层间距为apm,N-B键键长为bpm,则六方氮化硼晶体的密度为______  (用NA表示阿伏加德罗常数的值)。
(用NA表示阿伏加德罗常数的值)。
(1)基态Fe原子的核外电子排布式为
(2)苯胺(
 )分子中C原子与N原子的杂化方式分别为
)分子中C原子与N原子的杂化方式分别为 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点( 分子中的大π键应表示为
分子中的大π键应表示为(3)下列碳原子电子排布图表示的状态中,能量最低的是___________(填标号)。
A. | B. |
C. | D. |
①□内物质的空间构型为
②在与石墨结构相似的六方氮化硼晶体中,晶体的层间距为apm,N-B键键长为bpm,则六方氮化硼晶体的密度为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网