填空题 适中0.65 引用2 组卷90
碳是形成化合物种类最多的元素,其单质及形成的化合物是人类生产生活的主要能源物质。
(1)有机物M经过太阳光光照可转化成物质N,其能量变化如图所示。则M、N相比,较稳定的是_____ (填“M”或“N”)。

(2)已知:C(s)+H2O(l)=CO(g)+H2(g) ΔH1=a kJ·mol-1,2CO(g)+O2(g)=2CO2(g) ΔH2=b kJ·moL-1,2H2(g)+O2(g)=2H2O(l) ΔH3=c kJ·moL-1,则C(s)+O2(g)=CO2(g) ΔH=____ (用a、b、c表示)kJ·moL-1。
(3)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热ΔH=____ 。
(1)有机物M经过太阳光光照可转化成物质N,其能量变化如图所示。则M、N相比,较稳定的是

(2)已知:C(s)+H2O(l)=CO(g)+H2(g) ΔH1=a kJ·mol-1,2CO(g)+O2(g)=2CO2(g) ΔH2=b kJ·moL-1,2H2(g)+O2(g)=2H2O(l) ΔH3=c kJ·moL-1,则C(s)+O2(g)=CO2(g) ΔH=
(3)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热ΔH=

| 化学键 | C—H | C—F | H—F | F—F |
| 键能(kJ·mol-1) | 414 | 489 | 565 | 155 |
18-19高二·黑龙江大兴安岭地·期末
类题推荐
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。
(1)有机物M经过太阳光光照可转化成N,转化过程如图:
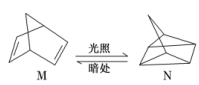 ΔH=+88.6 kJ∙mol−1
ΔH=+88.6 kJ∙mol−1
则M、N相比,较稳定的是___ (填M或N)。
(2)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热ΔH=___ 。
(3)使Cl2(g)和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:___ 。
(4)H2S的燃烧热ΔH=-a kJ∙mol−1,则H2S燃烧反应的热化学方程式___ 。
(5)①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ∙mol−1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ∙mol−1
③H2(g)+ O2(g)=H2O(1) ΔH3=-285.8 kJ∙mol−1
O2(g)=H2O(1) ΔH3=-285.8 kJ∙mol−1
则:2C(s)+O2(g)+2H2(g)=CH3COOH(l) ΔH=____ (用含ΔH1、ΔH2、ΔH3的式子表示并计算出结果)。
(1)有机物M经过太阳光光照可转化成N,转化过程如图:
 ΔH=+88.6 kJ∙mol−1
ΔH=+88.6 kJ∙mol−1则M、N相比,较稳定的是
(2)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热ΔH=
| 化学键 | C−H | C−F | H−F | F−F |
| 键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
(3)使Cl2(g)和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
(4)H2S的燃烧热ΔH=-a kJ∙mol−1,则H2S燃烧反应的热化学方程式
(5)①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ∙mol−1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ∙mol−1
③H2(g)+
则:2C(s)+O2(g)+2H2(g)=CH3COOH(l) ΔH=
碳是形成化合物种类最多的元素,其单质和化合物是人类生活的主要能源物质。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH =+88.6 kJ·mol-1,则M、N相比,较稳定的是__________
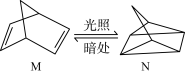
(2)根据下列热化学方程式分析,C(s)的燃烧热△H等于_____________ (用△H1 、△H2、△H3表示)
C(s)+H2O(l)=CO(g)+H2(g); △H1
2CO(g)+O2(g)=2CO2(g); △H2
2H2(g)+O2(g)=2H2O(l); △H3
(3)根据键能数据估算CH4(g)+4F2(g)= CF4(g)+4HF(g)的反应热ΔH=________
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:____________________________
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH =+88.6 kJ·mol-1,则M、N相比,较稳定的是

(2)根据下列热化学方程式分析,C(s)的燃烧热△H等于
C(s)+H2O(l)=CO(g)+H2(g); △H1
2CO(g)+O2(g)=2CO2(g); △H2
2H2(g)+O2(g)=2H2O(l); △H3
(3)根据键能数据估算CH4(g)+4F2(g)= CF4(g)+4HF(g)的反应热ΔH=
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 ΔH=+88.6kJ·mol-1。,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1。,则M、N相比,较稳定的是

