解答题-原理综合题 适中0.65 引用1 组卷106
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______ c(HCO3 -)(填“>”、“<”或“=”)。
②常温下,pH相同的三种溶液A.CH3COONa B.NaCN C.Na2CO3,其物质的量浓度由大到小的顺序是________ (填编号)。
③室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是________________ ,溶液中
___________ 。
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示。
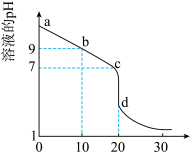
①d点所示的溶液中离子浓度由大到小的顺序依次为_____________ 。
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=__________ (用溶液中的其它离子浓度表示)。
③pH =10的氨水与pH =4的NH4C1溶液中,由水电离出的c(H+)之比为____ 。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka = 1.8×10-5 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)
②常温下,pH相同的三种溶液A.CH3COONa B.NaCN C.Na2CO3,其物质的量浓度由大到小的顺序是
③室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示。

①d点所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=
③pH =10的氨水与pH =4的NH4C1溶液中,由水电离出的c(H+)之比为
19-20高二上·山西朔州·期末
类题推荐
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表
①室温下,一定浓度的HCOONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是_______ 。
②0.1mol·L-1NaCN溶液和0.1mol·L-1NaHCO3溶液中,c(CN-)_______ c(HCO )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
③常温下,pH相同的三种溶液a、HCOONab、NaCNc、Na2CO3,其物质的量浓度由大到小的顺序是_______ (填编号)。
④将少量CO2通入NaCN溶液,反应的离子方程式是_______ 。
(2)室温下,用0.100mol·L-1盐酸溶液滴定20.00mL0.100mol·L-1的某氨水溶液,滴定曲线如图所示:
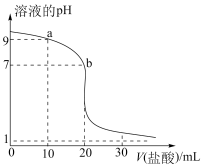
①b点液中离子浓度大小的关系式为_______ 。
②a点所示的溶液中电荷守恒式为_______ 。
(3)已知Ksp(BaCO3)=2.6×10-9,Ksp(BaSO4)=1.1×10-10
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为_______ mol·L-1
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中
_______ (保留三位有效数字)。
(1)已知部分弱酸的电离常数如下表
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka=1.77×10-4 | Ka=4.3×10-10 | Ka1=5.0×10-7 Ka2=5.6×10-11 |
①室温下,一定浓度的HCOONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
②0.1mol·L-1NaCN溶液和0.1mol·L-1NaHCO3溶液中,c(CN-)
③常温下,pH相同的三种溶液a、HCOONab、NaCNc、Na2CO3,其物质的量浓度由大到小的顺序是
④将少量CO2通入NaCN溶液,反应的离子方程式是
(2)室温下,用0.100mol·L-1盐酸溶液滴定20.00mL0.100mol·L-1的某氨水溶液,滴定曲线如图所示:

①b点液中离子浓度大小的关系式为
②a点所示的溶液中电荷守恒式为
(3)已知Ksp(BaCO3)=2.6×10-9,Ksp(BaSO4)=1.1×10-10
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如表:
①0.1mol/LNaCN溶液和0.1mol/LCH3COONa溶液中,
______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
②常温下,物质的量浓度相同的三种溶液:A. CH3COONa B. NaCN C. Na2CO3,其pH由大到小的顺序是______ (填编号)。
③将少量CO2通入NaCN溶液,反应的离子方程式是______ 。
④室温下,一定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是______ ,溶液中c(CH3COO-)/c(CH3COOH) =______ 。
(2)常温下,向20.00mL0.1000mol/L的醋酸溶液中逐滴加入0.1000mol/L的NaOH溶液,pH值随NaOH溶液体积的变化如图所示。

①d点(NaOH溶液为20mL时)所示的溶液中离子浓度由大到小的顺序依次为______ 。
②b点所示的溶液中c(CH3COO-)-c(CH3COOH)=______ (写表达式)。
(1)已知部分弱酸的电离常数如表:
| 弱酸 | |||
| 电离常数(25℃) |
②常温下,物质的量浓度相同的三种溶液:A. CH3COONa B. NaCN C. Na2CO3,其pH由大到小的顺序是
③将少量CO2通入NaCN溶液,反应的离子方程式是
④室温下,一定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
(2)常温下,向20.00mL0.1000mol/L的醋酸溶液中逐滴加入0.1000mol/L的NaOH溶液,pH值随NaOH溶液体积的变化如图所示。

①d点(NaOH溶液为20mL时)所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中c(CH3COO-)-c(CH3COOH)=
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题.
(1)已知部分弱酸的电离常数如表:
① 溶液和
溶液和 溶液中,
溶液中,
______________  (填“>”、“<”或=”)
(填“>”、“<”或=”)
②常温下, 相同的三种溶液:a.
相同的三种溶液:a. b.
b. c.
c. ,其物质的量浓度由大到小的顺序是
,其物质的量浓度由大到小的顺序是______________ (填编号).
③室温下,一定浓度的 溶液
溶液 ,用离子方程式表示溶液呈碱性的原因是
,用离子方程式表示溶液呈碱性的原因是______________ ,溶液中
______________ .
(2)某温度下, 的盐酸中
的盐酸中 .该温度下,
.该温度下, 的
的 与
与 的
的 混合后
混合后 变为9,则硫酸与氢氧化钠的体积比为
变为9,则硫酸与氢氧化钠的体积比为______________ .
(3)室温下,用 盐酸溶液滴定
盐酸溶液滴定 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积).
的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积).
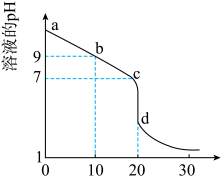
ⅰ.c点所示的溶液中离子浓度由大到小的顺序依次为______________ .
ⅱ. 点所示的溶液中
点所示的溶液中
______________ (写出准确值).
(1)已知部分弱酸的电离常数如表:
| 弱酸 | |||
| 电离常数 |
②常温下,
③室温下,一定浓度的
(2)某温度下,
(3)室温下,用

ⅰ.c点所示的溶液中离子浓度由大到小的顺序依次为
ⅱ.
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


