解答题-原理综合题 较难0.4 引用3 组卷582
随着科技进步和人类环保意识的增强,如何利用CO2已经成为世界各国特别关注的问题。
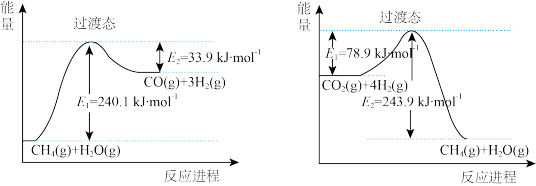
已知:CO2与CH4经催化重整制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g)△H
2CO(g)+2H2(g)△H
(1)降低温度,该反应速率会_______________ (填“增大”或“减小”);一定压强下,由最稳定单质生1 mol化合物的焓变为该物质的摩尔生成焓。已知CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395 kJ/mol、-74.9 kJ/mol、-110.4 kJ/mol。则上述重整反应的ΔH=____________ kJ/mol。
(2)T1℃时,在两个相同刚性密闭容器中充入CH4和CO2分压均为20 kPa,加入催化剂Ni/α-Al2O3并分别在T1℃和T2℃进行反应,测得CH4转化率随时间变化如图Ⅰ所示。
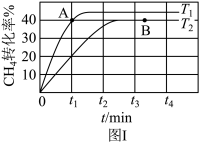
①A点处v正_______ B点处(填“<”、“>”或“=”)
②研究表明CO的生成速率v生成(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1,A点处v生成(CO)=__________ mol·g-1·s-1。
(3)上述反应达到平衡后,若改变某一条件,下列变化能说明平衡一定正向移动的是________________ (填代号)。
A.正反应速率增大B.生成物的百分含量增大C.平衡常数K增大
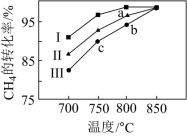
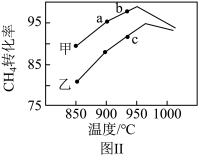
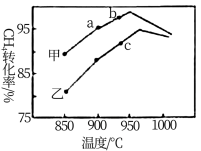
(4)其他条件相同,在甲、乙两种不同催化剂作用下,相同时间内测得CH4转化率与温度变化关系如图Ⅱ,C点___________________ (填“可能”、“一定”或“一定未”)达到平衡状态,理由是_____________ ;CH4的转化率b点高于a点的可能原因是_________________________________ 。
已知:CO2与CH4经催化重整制得合成气:CH4(g)+CO2(g)
(1)降低温度,该反应速率会
(2)T1℃时,在两个相同刚性密闭容器中充入CH4和CO2分压均为20 kPa,加入催化剂Ni/α-Al2O3并分别在T1℃和T2℃进行反应,测得CH4转化率随时间变化如图Ⅰ所示。

①A点处v正
②研究表明CO的生成速率v生成(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1,A点处v生成(CO)=
(3)上述反应达到平衡后,若改变某一条件,下列变化能说明平衡一定正向移动的是
A.正反应速率增大B.生成物的百分含量增大C.平衡常数K增大
(4)其他条件相同,在甲、乙两种不同催化剂作用下,相同时间内测得CH4转化率与温度变化关系如图Ⅱ,C点

2019·四川成都·一模
类题推荐
随着科技进步和人类环保意识的增强,如何利用CO2已经成为世界各国特别关注的问题。
已知:CO2与CH4经催化重整制得合成气:CO2(g)+CH4(g) 2CO(g)+2H2(g)△H
2CO(g)+2H2(g)△H
(1)一定压强下,由最稳定单质生成lrnol化合物的焓变为该物质的摩尔生成焓。已知CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395kJ/mol、-74.9kJ/mol、-110.4kJ/mol。则上述重整反应的△H=___ kJ/mol。
(2)其他条件相同,在甲、乙两种不同催化剂作用下,相同时间内测得CH4转化率与温度变化关系如图。c点___ (填“可能”、“一定”或“一定未”)达到平衡状态,CH4的转化率b点高于a点的可能原因是___ 。
(3)CH4超干重整CO2技术可得到富含CO的气体,用于生产多种化工产品。目前科学家研究CH4超干重整CO2的催化转化原理示意图如图:
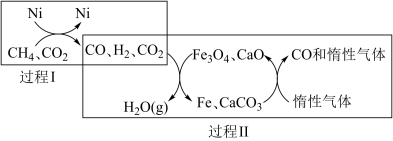
该技术中的总化学反应方程式为:___ 。
(4)CO2在Cu—ZnO催化下,可同时发生如下的反应I、II其可作为解决温室效应及能源短缺的重要手段。
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H1=-57.8kJ/mol
CH3OH(g)+H2O(g)△H1=-57.8kJ/mol
Il.CO2(g)+H2(g) CO(g)+H2O(g)△H2=+41.2kJ/mol
CO(g)+H2O(g)△H2=+41.2kJ/mol
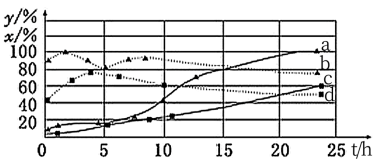
①其他条件相同,分别进行H2的初始浓度为2mol•L-1和4mol•L-1的实验。测得CO2的消耗百分率(x%,实线)和生成物中CH3OH的百分含量(y%虚线)随时间(t)的变化关系如图。图中表示H2起始浓度为2mol•L-1时CO2的消耗百分率、CH3OH的百分含量的变化曲线分别是___ (填字母)。
②保持温度T不变,在一刚性密闭容器中,充入一定量的CO2及H2,起始及达平衡时,容器内各气体物质的量如下表:
则表中n1=___ ;反应I的平衡常数Kp=___ (无需带单位,用含总压p的式子表示)。
已知:CO2与CH4经催化重整制得合成气:CO2(g)+CH4(g)
 2CO(g)+2H2(g)△H
2CO(g)+2H2(g)△H(1)一定压强下,由最稳定单质生成lrnol化合物的焓变为该物质的摩尔生成焓。已知CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395kJ/mol、-74.9kJ/mol、-110.4kJ/mol。则上述重整反应的△H=
(2)其他条件相同,在甲、乙两种不同催化剂作用下,相同时间内测得CH4转化率与温度变化关系如图。c点

(3)CH4超干重整CO2技术可得到富含CO的气体,用于生产多种化工产品。目前科学家研究CH4超干重整CO2的催化转化原理示意图如图:

该技术中的总化学反应方程式为:
(4)CO2在Cu—ZnO催化下,可同时发生如下的反应I、II其可作为解决温室效应及能源短缺的重要手段。
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H1=-57.8kJ/mol
CH3OH(g)+H2O(g)△H1=-57.8kJ/molIl.CO2(g)+H2(g)
 CO(g)+H2O(g)△H2=+41.2kJ/mol
CO(g)+H2O(g)△H2=+41.2kJ/mol①其他条件相同,分别进行H2的初始浓度为2mol•L-1和4mol•L-1的实验。测得CO2的消耗百分率(x%,实线)和生成物中CH3OH的百分含量(y%虚线)随时间(t)的变化关系如图。图中表示H2起始浓度为2mol•L-1时CO2的消耗百分率、CH3OH的百分含量的变化曲线分别是

②保持温度T不变,在一刚性密闭容器中,充入一定量的CO2及H2,起始及达平衡时,容器内各气体物质的量如下表:
| CO2 | H2 | CH3OH(g) | CO | H2O(g) | 总压/kPa | |
| 起始/mol | 4.0 | 8.0 | 0 | 0 | 0 | 1.5p |
| 平衡/mol | n1 | 3.0 | p |
则表中n1=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网