解答题-结构与性质 适中0.65 引用1 组卷110
短周期主族元素X、Y、Z、M、W的原子序数依次递增,X的简单阴离子与He原子具有相同的电子层结构,Y基态原子未成对电子数在所处周期中最多,M是地壳中含量最多的金属元素,W原子最外层电子数是K层电子数的3倍,Z、W同主族。
(1)下列说法正确的是______ 。
A.原子半径:
B.X、Y、Z三种元素只能形成共价化合物
C.W的简单气态氢化物的热稳定性比Z的强
D.M的单质能溶于W的最高氧化物对应水化物的稀溶液
(2)X、Y、Z、M、W五种元素中:
①电负性最小的元素是______  填元素的符号,下同
填元素的符号,下同 ,第一电离能最大的元素是
,第一电离能最大的元素是______ 。
②Z原子的电子排布图 轨道表示式
轨道表示式 为
为______ ,W的电子排布式为______ 。
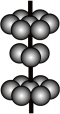
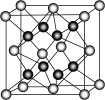
③如图可以表示Y单质分子中电子云重叠方式的是______ 。
A. B.
B.  C.
C.  D.
D. 
1mol Y单质分子中含有 键的数目为
键的数目为______ 。
④Y的简单气态氢化物极易溶于水,其原因是______ ;一种含碳元素的阴离子R与Y的简单气态氢化物互为等电子体,写出R的电子式:______ 。
⑤向W的简单气态氢化物的水溶液中通入Z的单质,有W的单质析出,可以验证Z 的非金属性强于W,该反应的离子方程式为______ 。
(3)向含有M简单离子的溶液中加入过量NaOH溶液,可生成 。
。
①不考虑空间构型 要标出配位键,M要用元素符号表示
要标出配位键,M要用元素符号表示 ,
, 的结构可用示意图表示为
的结构可用示意图表示为______ 。
② 的空间构型为
的空间构型为______ ,其M原子轨道的杂化类型为______ 。
(4)铁、铜和Y元素可生成晶胞结构图1 所示的化合物,该化合物的化学式为______ 。
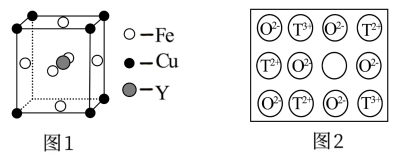
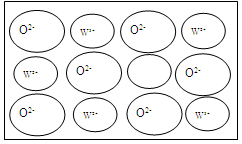
 天然的和绝大部分人工制备的晶体都存在各种缺陷。如某过渡元素T的基态原子中的未成对电子数恰好等于最外层电子数;而其3d能级上的电子数等于最外层电子数的4倍。这种T的氧化物的晶胞结构就存在缺陷
天然的和绝大部分人工制备的晶体都存在各种缺陷。如某过渡元素T的基态原子中的未成对电子数恰好等于最外层电子数;而其3d能级上的电子数等于最外层电子数的4倍。这种T的氧化物的晶胞结构就存在缺陷 如图2所示
如图2所示 。
。
①基态 的外围电子排布式为
的外围电子排布式为______ ;若该T的氧化物晶体中每有1个 空缺,则应有
空缺,则应有______ 个 倍
倍 所取代,才能使晶体仍呈电中性。
所取代,才能使晶体仍呈电中性。
②若某T的氧化物晶体样品中 与
与 的离子数之比为1:11,则该晶体的化学式为
的离子数之比为1:11,则该晶体的化学式为______ 。
(1)下列说法正确的是
A.原子半径:
B.X、Y、Z三种元素只能形成共价化合物
C.W的简单气态氢化物的热稳定性比Z的强
D.M的单质能溶于W的最高氧化物对应水化物的稀溶液
(2)X、Y、Z、M、W五种元素中:
①电负性最小的元素是
②Z原子的电子排布图
③如图可以表示Y单质分子中电子云重叠方式的是
A.
 B.
B.  C.
C.  D.
D. 
1mol Y单质分子中含有
④Y的简单气态氢化物极易溶于水,其原因是
⑤向W的简单气态氢化物的水溶液中通入Z的单质,有W的单质析出,可以验证Z 的非金属性强于W,该反应的离子方程式为
(3)向含有M简单离子的溶液中加入过量NaOH溶液,可生成
①不考虑空间构型
②
(4)铁、铜和Y元素可生成晶胞结构图1 所示的化合物,该化合物的化学式为

①基态
②若某T的氧化物晶体样品中
2020高三·全国·专题练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网