计算题 适中0.65 引用1 组卷118
1)22.0g K2R中含有0.4mol钾离子,则该物质的摩尔质量为________ ,R的相对原子质量为________ 。
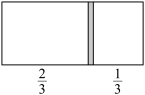
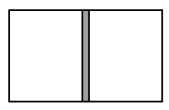
(2)在恒温条件下的密闭容器中,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当在左边充入1 mol N2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置。

①隔板左右两边气体的气体的分子数之比为______ 。
②右边混合气体中CO和CO2物质的量分别为________ 、________ ,该混合气体平均相对分子质量为______ 。
(3)现有20°C的饱和硫酸铜溶液,其质量分数为16%、密度为1.25g/cm3。则:
①20°C时,硫酸铜的溶解度为________ ;
②该饱和硫酸铜溶液的物质的量浓度为____ ;
③实验室需要250mL 0.5mol/LCuSO4溶液。在配制该溶液时需要称取胆矾(CuSO4·5H2O)的质量为____ ;
④取20mL 0.5mol/LCuSO4溶液恰好与50mLNaOH溶液反应,使Cu2+完全转化为沉淀。请计算氢氧化钠溶液的物质的量浓度(写出过程)____ 。
(2)在恒温条件下的密闭容器中,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当在左边充入1 mol N2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置。

①隔板左右两边气体的气体的分子数之比为
②右边混合气体中CO和CO2物质的量分别为
(3)现有20°C的饱和硫酸铜溶液,其质量分数为16%、密度为1.25g/cm3。则:
①20°C时,硫酸铜的溶解度为
②该饱和硫酸铜溶液的物质的量浓度为
③实验室需要250mL 0.5mol/LCuSO4溶液。在配制该溶液时需要称取胆矾(CuSO4·5H2O)的质量为
④取20mL 0.5mol/LCuSO4溶液恰好与50mLNaOH溶液反应,使Cu2+完全转化为沉淀。请计算氢氧化钠溶液的物质的量浓度(写出过程)
19-20高一上·广东深圳·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网