解答题-工业流程题 适中0.65 引用2 组卷138
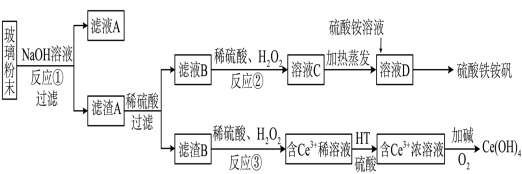
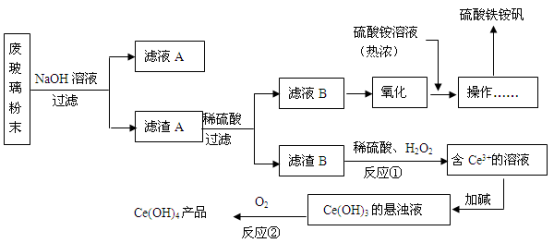
在工业上可用含SiO2、CeO2和Fe2O3的废料作原料来获得硫酸铁铵晶体【Fe2(SO4)3·2(NH4)2 SO4·3H2O】,同时可回收CeO2,工艺流程设计如下

已知: ①SiO2、CeO2不溶于稀硫酸;②酸性条件下,CeO2可与H2O2反应;③“反应Ⅰ”所得溶液中含有Ce3+;④碱性条件下,NH4+与OH-结合生成NH3·H2O。
请回答下列问题
(1)“酸浸”时未发生的反应 物质是__________________ (填化学式)。
(2)“滤液”中含有的阳离子有___________________ (填离子符号)。
(3)写出“反应Ⅰ”的化学方程式:________________________________________ 。
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是__________________ (填化学式)。
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:_____________________ 。

已知: ①SiO2、CeO2不溶于稀硫酸;②酸性条件下,CeO2可与H2O2反应;③“反应Ⅰ”所得溶液中含有Ce3+;④碱性条件下,NH4+与OH-结合生成NH3·H2O。
请回答下列问题
(1)“酸浸”时未发生的反应 物质是
(2)“滤液”中含有的阳离子有
(3)写出“反应Ⅰ”的化学方程式:
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:
19-20高一上·河南·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

 2CeT3 (有机层)+3H2SO4(水层)
2CeT3 (有机层)+3H2SO4(水层)

