多选题 较难0.4 引用1 组卷166
在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)  2NO2(g)+S(s)。
2NO2(g)+S(s)。
改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是( )
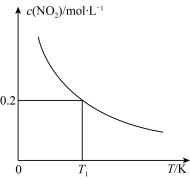
改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是( )
容器 编号 | 温度/K | 起始物质的量/mol | |||
SO2 | NO | NO2 | S | ||
Ⅰ | 0.5 | 0.6 | 0 | 0 | |
Ⅱ | T1 | 0.5 | 1 | 0.5 | 1 |
Ⅲ | T2 | 0.5 | 0.2 | 1 | 1 |

| A.该反应的ΔH<0 |
| B.T1时,该反应的平衡常数为 |
| C.容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比小于1:2 |
| D.若T2<T1,达到平衡时,容器Ⅲ中NO的体积分数小于40% |
19-20高三上·江苏常州·阶段练习
类题推荐
温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g)  2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2), v逆= v(NO)消耗= 2v (O2 )消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。
2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2), v逆= v(NO)消耗= 2v (O2 )消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。
下列说法正确的是
 2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2), v逆= v(NO)消耗= 2v (O2 )消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。
2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2), v逆= v(NO)消耗= 2v (O2 )消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。容器编号 | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
| A.T1时,该反应的平衡常数为1 |
| B.达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为 4∶5 |
| C.达平衡时,容器Ⅲ中 NO 的体积分数小于50% |
| D.当温度改变为 T2时,若 k正=k逆,则 T2> T1 |
温度为 T1 时,在三个容积均为 1 L 的恒容密闭容器中仅发生反应:2NO2(g) 2NO(g)+O2(g)(正反应吸热)。实验测得:v正= k正 c2(NO2),v逆= k逆 c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是( )
2NO(g)+O2(g)(正反应吸热)。实验测得:v正= k正 c2(NO2),v逆= k逆 c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是( )
| 容器编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
| c(NO2) | c(NO) | c(O2) | c(O2) | |
| I | 0.6 | 0 | 0 | 0.2 |
| II | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
| A.达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为 4∶5 |
| B.达平衡时,容器Ⅱ中 |
| C.达平衡时,容器Ⅲ中 NO 的体积分数小于 50% |
| D.当温度改变为 T2 时,若 k 正=k 逆,则 T2 < T1 |
温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO2(g) 2NO(g)+O2 (g) (正反应吸热)。实验测得:v正= v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是
2NO(g)+O2 (g) (正反应吸热)。实验测得:v正= v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是
| 容器编号 | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
| c(NO2) | c(NO) | c(O2) | c(O2) | |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
| A.达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为4∶5 |
| B.达平衡时,容器Ⅱ中 |
| C.达平衡时,容器Ⅲ中NO的体积分数小于50% |
| D.当温度改变为T2时,若k正=k逆,则 T2> T1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


