单选题 适中0.65 引用1 组卷93
下列说法正确的是
| A.在由水电离产生的氢离子浓度为10-13mol/L的溶液中,Ca2+、K+、Cl-、HCO3-四种离子能大量共存 |
| B.常温下,将0.2mol/L某一元碱ROH溶液和0.1mol/LHCl溶液等体积混合,混合后溶液pH<7,则该溶液c(ROH)>c(R+) |
| C.反应 |
| D.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有: |
2019高三·全国·专题练习
类题推荐
下列说法正确的是
| A.常温下将pH=2的醋酸和pH=12的NaOH溶液等体积混合,所得溶液显碱性 |
| B.已知同温时氢氟酸的电离常数大于亚硝酸的电离常数,则相同温度相同浓度的NaF溶液和NaNO2溶液的碱性:NaF溶液较强 |
| C.将等体积的盐酸和氨水混合,充分反应后所得溶液呈中性,则两溶液的物质的量浓度关系为:c(HCl)<c(NH3·H2O) |
| D.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)= c(CO32-),且c(Mg2+)·c(CO32-)=6.82×10-6 |
下列说法正确的是:
| A.若将含0.5 mol的浓硫酸溶液与含1 molNaOH的溶液混合,ΔH =- 57.3 kJ/mol |
| B.已知MgCO3的Ksp =6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+) = c( |
C.已知:C-C键能348 kJ/mol、C=C键能610 kJ/mol、C-H键能413 kJ/mol、H-H键能436 kJ/mol,则可以计算出反应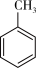 (g)+3H2(g) (g)+3H2(g)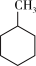 (g)的ΔH为-384 kJ/mol (g)的ΔH为-384 kJ/mol |
| D.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的pH减小 |
下列有关说法正确的是
| A.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) |
| B.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-), 且c(Mg2+)·c(CO32-)=6.82×10-6 mol•L-1 |
| C.将0.2mol/L的NH3·H2O与0.1mol/L的HCl溶液等体积混合后PH>7,则c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D.用惰性电极电解Na2SO4溶液,阳阴两极产物的物质的量之比为2:1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


