解答题-实验探究题 较难0.4 引用1 组卷157
某化学兴趣小组对碳、氮、磷等常见元素的化合物性质进行如下研究.请按要求回答问题.
 甲同学用图l所示装置
甲同学用图l所示装置 部分夹持装置略
部分夹持装置略 探究NO与
探究NO与 的反应.
的反应.
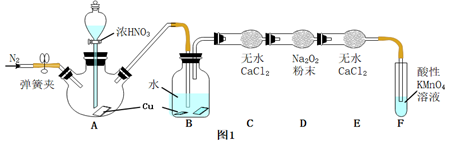
查阅资料:


酸性条件下,NO或 都能与
都能与 反应生成
反应生成 和
和
 中反应的化学方程式是
中反应的化学方程式是 ______  中观察到的主要现象是
中观察到的主要现象是 ______ ,F装置的作用是 ______ .
 在反应前,打开弹簧夹,通入一段时间
在反应前,打开弹簧夹,通入一段时间 ,目的是
,目的是 ______ .
 充分反应后,检验D装置中发生反应的实验是
充分反应后,检验D装置中发生反应的实验是 ______ .
 乙同学查阅有关弱酸的电离平衡常数:
乙同学查阅有关弱酸的电离平衡常数:
则该温度下相同pH的 、
、 、
、 、
、 溶液的物质的量浓度由大到小的顺序为
溶液的物质的量浓度由大到小的顺序为 ______  填编号
填编号 .
.
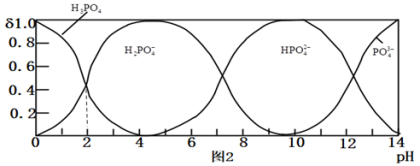
 磷酸
磷酸 为一种三元酸,其在水溶液中各种存在形式物质的量分数
为一种三元酸,其在水溶液中各种存在形式物质的量分数 随pH的变化曲线如图2:
随pH的变化曲线如图2:
 溶液中,
溶液中,
______  填“
填“ ”“
”“ ”或“
”或“ ”
” 向
向 溶液中滴入稀盐酸后,pH从10降低到5的过程中发生的主要反应的离子方程式为
溶液中滴入稀盐酸后,pH从10降低到5的过程中发生的主要反应的离子方程式为 ______ .
 由图推断
由图推断 溶液中各种微粒浓度关系是
溶液中各种微粒浓度关系是 ______  填选项字母
填选项字母
A.
B.
C.
D.
 假设在
假设在 时测得
时测得 溶液的
溶液的 ,近似计算出
,近似计算出 第一步水解的水解常数
第一步水解的水解常数 用
用 表示
表示

______  忽略
忽略 第二、第三步水解,结果保留两位有效数字
第二、第三步水解,结果保留两位有效数字 .
.


查阅资料:
酸性条件下,NO或
| 化学式 | | HCN | |
| 电离平衡常数 | | | |
则该温度下相同pH的
A.
B.
C.
D.
2019高三·全国·专题练习
类题推荐
自然界是各类物质相互依存、各种变化相互制约的复杂平衡体系,水溶液中的离子平衡是其中一个重要方面。请根据所学知识,回答下列问题。
(1)某温度下,0.1mol/L的盐酸中水电离出的 ,该温度下将
,该温度下将 的NaOH溶液与
的NaOH溶液与 的
的 溶液等体积混合,混合后溶液的
溶液等体积混合,混合后溶液的
_______ 。
(2)常温下将pH均为3,体积均为 的HA和HB溶液,分别加水稀释至体积V,pH随
的HA和HB溶液,分别加水稀释至体积V,pH随 的变化如图所示。
的变化如图所示。
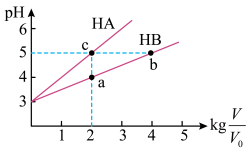
①a、b、c三点水的电离程度_______ (用“>”、“=”、“<”填空)。
②常温下,取上述pH均为3的HA和HB溶液各100mL,向其中分别加入足量的Zn粒,反应结束时HA中产生氢气的物质的量为 ,HB溶液中产生氢气的物质的量为
,HB溶液中产生氢气的物质的量为 ,则
,则
_______  (用“>”、“=”、“<”填空)。
(用“>”、“=”、“<”填空)。
(3)查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
①KSCN溶液呈弱碱性,用离子方程式解释原因_______ 。
② 溶液的水解平衡常数
溶液的水解平衡常数
_______ (保留两位有效数字)。
③同浓度的NaF溶液和 溶液相比,
溶液相比,
后者溶液中
_______ 前者溶液中 (用“>”、“=”、“<”填空)。
(用“>”、“=”、“<”填空)。
④现有25℃时等浓度的5种溶液:
A. B.
B. C.
C. D.
D. E.
E.
这5种溶液中 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:_______ (填字母)。
(1)某温度下,0.1mol/L的盐酸中水电离出的
(2)常温下将pH均为3,体积均为

①a、b、c三点水的电离程度
②常温下,取上述pH均为3的HA和HB溶液各100mL,向其中分别加入足量的Zn粒,反应结束时HA中产生氢气的物质的量为
(3)查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
| 化学式 | HF | HClO | HSCN | |||
| 电离平衡常数 | 0.13 |
②
③同浓度的NaF溶液和
后者溶液中
④现有25℃时等浓度的5种溶液:
A.
这5种溶液中
水是最常用的溶剂,许多化学反应都需要在水溶液中进行。请仔细分析并回答下列各题。
(1)用0.1mol/LNaOH溶液滴定体积均为20.00mL、浓度均为0.1mol/L盐酸和醋酸溶液,得到如下所示滴定曲线图:
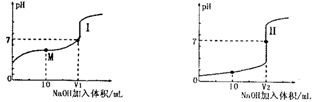
①用NaOH 溶液滴定醋酸溶液通常所选择的指示剂为________,符合其滴定曲线的是_______(填“I”或“II”);
②滴定前的上述三种溶液中,由水电离出的c(H+)最大的是_________溶液(填化学式);
③图中v1和v2大小的比较:v1_______v2 (填“>”、“<”或“=”);
④图I中M 点对应的溶液中,各离子的浓度由大到小的顺序是______________。
(2)某同学为了研究难溶电解质的溶解平衡,设计了如下实验(相关数据测定温度及实验环境均为25 ℃ ):
查阅资料:AgSCN是白色沉淀:Ksp(AgSCN)=1.0×10-12;Ksp(AgI)=8.5×10-17.
① 请结合化学用语和必要的文字解释步骤2 现象出现的原因:____________________。
②该同学根据步骤3中现象a推知,加入的AgNO3与步骤2所得溶液发生了反应,则现象a为______________(任写一点即可)。
③ 写出步骤4 中沉淀转化反应平衡常数的表达式:K=__________。
(1)用0.1mol/LNaOH溶液滴定体积均为20.00mL、浓度均为0.1mol/L盐酸和醋酸溶液,得到如下所示滴定曲线图:

①用NaOH 溶液滴定醋酸溶液通常所选择的指示剂为________,符合其滴定曲线的是_______(填“I”或“II”);
②滴定前的上述三种溶液中,由水电离出的c(H+)最大的是_________溶液(填化学式);
③图中v1和v2大小的比较:v1_______v2 (填“>”、“<”或“=”);
④图I中M 点对应的溶液中,各离子的浓度由大到小的顺序是______________。
(2)某同学为了研究难溶电解质的溶解平衡,设计了如下实验(相关数据测定温度及实验环境均为25 ℃ ):
| 操作步骤 | 现象 |
| 步骤1:向20mL0.05mol/LAgNO3溶液中加入20mL0.05mol/LKSCN溶液,充分反应后过滤 | 出现白色沉淀 |
| 步骤2:向滤液中加少量2mol/LFe(NO3)3溶液 | 溶液变红色 |
| 步骤3:向步骤2所得溶液中,加入少量3mol/LAgNO3溶液 | 现象a |
| 步骤4:取步骤1所得少量滤渣加入到适量的3mol/LKI溶液中 | 出现黄色沉淀 |
查阅资料:AgSCN是白色沉淀:Ksp(AgSCN)=1.0×10-12;Ksp(AgI)=8.5×10-17.
① 请结合化学用语和必要的文字解释步骤2 现象出现的原因:____________________。
②该同学根据步骤3中现象a推知,加入的AgNO3与步骤2所得溶液发生了反应,则现象a为______________(任写一点即可)。
③ 写出步骤4 中沉淀转化反应平衡常数的表达式:K=__________。
为了研究 的性质,某兴趣小组进行了如下实验。
的性质,某兴趣小组进行了如下实验。
Ⅰ.制备: 易潮解,
易潮解, 能升华。
能升华。
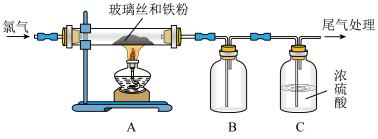
(1)实验开始前先通氯气的目的是_____ 。
(2)若用NaOH溶液处理尾气,发生反应的化学方程式为_____ 。
(3)该装置存在的主要缺点是_____ 。
Ⅱ.溶液的配制:
(4)取 固体溶于浓盐酸,再稀释至指定浓度。配制
固体溶于浓盐酸,再稀释至指定浓度。配制 溶液,需
溶液,需 溶液的体积为
溶液的体积为_____ mL,不需要使用的实验仪器有_____ (填字母)。
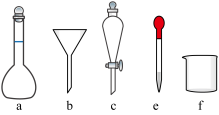
Ⅲ. 溶液的性质:
溶液的性质:
(5)向 溶液中通入
溶液中通入 至饱和,充分静置。观察到
至饱和,充分静置。观察到 溶液颜色由黄色变成血红色。静置5分钟后溶液颜色由血红色慢慢变回黄色,静置9小时后溶液慢慢由黄色变成浅绿色。
溶液颜色由黄色变成血红色。静置5分钟后溶液颜色由血红色慢慢变回黄色,静置9小时后溶液慢慢由黄色变成浅绿色。 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为_____ 。某同学想检验反应5分钟后的溶液中有 生成,应选用的试剂是
生成,应选用的试剂是_____ 。
(6)为探究实验过程中血红色物质产生的原因,该同学查阅资料发现红色物质可能是 与溶液中某种+4价含硫微粒形成的配离子(可逆反应),于是提出以下假设:
与溶液中某种+4价含硫微粒形成的配离子(可逆反应),于是提出以下假设:
假设一:血红色物质的产生与 或
或 有关
有关
假设二:血红色物质的产生与 或
或 有关
有关
该同学为验证假设进行以下实验:
①实验一:向 溶液中滴加
溶液中滴加 溶液,溶液变成血红色,且颜色比(1)实验深,再加入
溶液,溶液变成血红色,且颜色比(1)实验深,再加入
_____ ,溶液颜色由红色褪成黄色。
②实验二:将 的
的 溶液、
溶液、 溶液、
溶液、 溶液以一定体积混合,利用分光光度仪对红色物质的浓度进行检测,测得实验数据如下,吸光度越大,溶液颜色越深。
溶液以一定体积混合,利用分光光度仪对红色物质的浓度进行检测,测得实验数据如下,吸光度越大,溶液颜色越深。
表中x=_____ 。
③实验结论:血红色物质是 与
与_____ 形成的配离子。
(7)结合化学平衡解释(1)实验中出现“5分钟后溶液颜色由血红色慢慢变回黄色”现象的原因:_____ 。
Ⅰ.制备:

(1)实验开始前先通氯气的目的是
(2)若用NaOH溶液处理尾气,发生反应的化学方程式为
(3)该装置存在的主要缺点是
Ⅱ.溶液的配制:
(4)取

Ⅲ.
(5)向
(6)为探究实验过程中血红色物质产生的原因,该同学查阅资料发现红色物质可能是
假设一:血红色物质的产生与
假设二:血红色物质的产生与
该同学为验证假设进行以下实验:
①实验一:向
②实验二:将
| 序号 | V/mL | 吸光度 | ||
| 1 | 0.5 | 4.0 | 0.0 | 0.412 |
| 2 | 0.5 | 3.2 | 0.8 | 0.331 |
| 3 | 0.5 | 2.0 | 2.0 | 0.182 |
| 4 | 0.5 | 1.2 | x | 0.085 |
| 5 | 0.5 | 0.0 | 4.0 | 0.018 |
③实验结论:血红色物质是
(7)结合化学平衡解释(1)实验中出现“5分钟后溶液颜色由血红色慢慢变回黄色”现象的原因:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


