解答题-原理综合题 适中0.65 引用1 组卷120
运用元素周期律研究元素及其化合物的性质具有重要的意义。
I.部分短周期主族元素的最高价氧化物对应水化物(浓度均为0.01mol·L-1)溶液的pH和原子序数的关系如图所示。
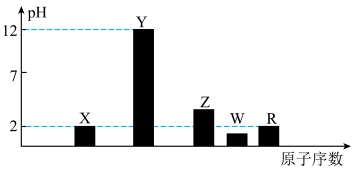
(1)元素R在周期表中的位置是_______ ;元素Z的原子结构示意图是________ 。
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为________ 。
II.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是__________ (填序号)
A. S与H2发生化合反应比C与H2化合更容易
B. 酸性:H2SO3 >H2CO3
C. CS2中碳元素为+4价,硫元素为-2价
(2)铅(Pb)、锡(Sn)、锗(Ge)与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为_________ 。
②它们+4价氢氧化物的碱性由强到弱顺序为____________ (填化学式)。
(3)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似。羰基硫(COS)的电子式为:______________________ 。
I.部分短周期主族元素的最高价氧化物对应水化物(浓度均为0.01mol·L-1)溶液的pH和原子序数的关系如图所示。

(1)元素R在周期表中的位置是
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为
II.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是
A. S与H2发生化合反应比C与H2化合更容易
B. 酸性:H2SO3 >H2CO3
C. CS2中碳元素为+4价,硫元素为-2价
(2)铅(Pb)、锡(Sn)、锗(Ge)与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为
②它们+4价氢氧化物的碱性由强到弱顺序为
(3)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似。羰基硫(COS)的电子式为:
18-19高二上·湖北宜昌·期中
类题推荐
运用元素周期律研究元素及其化合物的性质具有重要的意义。
Ⅰ.下表为元素周期表的一部分,根据表中给出的9种元素回答下列问题。
(1)原子半径最大的元素是_______ (填元素名称),画出⑦的离子结构示意图_______ 。
(2)②的最简单氢化物的空间结构为_______ 形。
(3)由元素①、④、⑥形成的化合物属于_______ 化合物(选填“离子”或“共价”)。
(4)⑤和⑨元素原子得电子能力较强的是_______ (填元素符号),请用原子结构的知识解释其原因_______ 。
Ⅱ.同主族元素性质存在一定的相似性和递变性。
(5)羰基硫(COS)可作为一种熏蒸剂,防止某些昆虫、线虫的危害,其分子结构和 相似。羰基硫(COS)的电子式为
相似。羰基硫(COS)的电子式为_______ 。
(6)下列不能说明碳、硅两种元素非金属性相对强弱的是_______ (填标号)
A.焦炭还原 制粗硅
制粗硅
B.酸性:
C.稳定性:
(7)碳、硅、锗、锡的+4价化合物是稳定的,而铅的+2价化合物是稳定的。由此推测,铅的+4价化合物具有较强的_______ 性。 与浓盐酸共热可生成
与浓盐酸共热可生成 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
Ⅰ.下表为元素周期表的一部分,根据表中给出的9种元素回答下列问题。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)②的最简单氢化物的空间结构为
(3)由元素①、④、⑥形成的化合物属于
(4)⑤和⑨元素原子得电子能力较强的是
Ⅱ.同主族元素性质存在一定的相似性和递变性。
(5)羰基硫(COS)可作为一种熏蒸剂,防止某些昆虫、线虫的危害,其分子结构和
(6)下列不能说明碳、硅两种元素非金属性相对强弱的是
A.焦炭还原
B.酸性:
C.稳定性:
(7)碳、硅、锗、锡的+4价化合物是稳定的,而铅的+2价化合物是稳定的。由此推测,铅的+4价化合物具有较强的
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网