解答题-工业流程题 较难0.4 引用3 组卷301
氯氧化铜[xCuO·yCuCl2·zH2O]在农业上用作杀菌剂。工业上用铜矿粉(主要含Cu2(OH)2CO3、Fe3O4等)为原料制取氯氧化铜的流程如下:
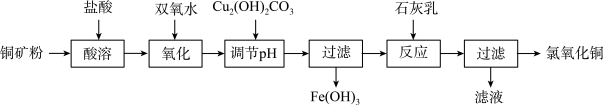
⑴“调节pH”并生成Fe(OH)3时反应的离子方程式为______ 。
⑵调节pH,要使常温溶液中c(Cu2+)≥0.022mol·L-1,而c(Fe3+)≤1×10-6mol·L-1,则应调节pH的范围为______ 。{已知Ksp[Cu(OH)2=2.2×10-20],Ksp[Fe(OH)3=1×10-36]}
⑶为测定氯氧化铜的组成,现进行如下实验:
步骤Ⅰ:称取0.4470 g氯氧化铜,放入锥形瓶,加入一定量30%的硝酸使固体完全溶解。滴加K2CrO4溶液作指示剂,用0.1000mol·L-1 AgNO3标准溶液滴定溶液中的Cl-,滴定至终点时消耗AgNO3标准溶液20.00 mL;
步骤Ⅱ:称取0.4470g氯氧化铜,放入锥形瓶,加入一定量硫酸使固体完全溶解。向溶液中加入过量的KI固体,充分反应后向溶液中滴入数滴淀粉溶液,用0.2000mol·L-1Na2S2O3标准溶液滴定,滴定至终点时消耗Na2S2O3标准溶液20.00mL。
已知步骤Ⅱ中所发生的反应如下:
2Cu2++4I-=2CuI↓+I2 2Na2S2O3+I2=2NaI+Na2S4O6
①已知Ag2CrO4为砖红色沉淀,步骤Ⅰ滴定终点时的实验现象是_______ 。
②通过计算确定氯氧化铜的化学式________________ (写出计算过程)。

⑴“调节pH”并生成Fe(OH)3时反应的离子方程式为
⑵调节pH,要使常温溶液中c(Cu2+)≥0.022mol·L-1,而c(Fe3+)≤1×10-6mol·L-1,则应调节pH的范围为
⑶为测定氯氧化铜的组成,现进行如下实验:
步骤Ⅰ:称取0.4470 g氯氧化铜,放入锥形瓶,加入一定量30%的硝酸使固体完全溶解。滴加K2CrO4溶液作指示剂,用0.1000mol·L-1 AgNO3标准溶液滴定溶液中的Cl-,滴定至终点时消耗AgNO3标准溶液20.00 mL;
步骤Ⅱ:称取0.4470g氯氧化铜,放入锥形瓶,加入一定量硫酸使固体完全溶解。向溶液中加入过量的KI固体,充分反应后向溶液中滴入数滴淀粉溶液,用0.2000mol·L-1Na2S2O3标准溶液滴定,滴定至终点时消耗Na2S2O3标准溶液20.00mL。
已知步骤Ⅱ中所发生的反应如下:
2Cu2++4I-=2CuI↓+I2 2Na2S2O3+I2=2NaI+Na2S4O6
①已知Ag2CrO4为砖红色沉淀,步骤Ⅰ滴定终点时的实验现象是
②通过计算确定氯氧化铜的化学式
19-20高三上·江苏南通·阶段练习
类题推荐
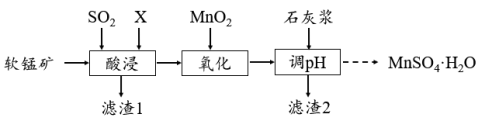
某研究小组利用软锰矿(主要成分MnO2)制备MnSO4·H2O的流程如下:
已知:①“酸浸”后的溶液pH< 1,除含Mn2+外,还含有少量Fe2+、Al3+、Ca2+等金属离子。
②下表列出相关金属离子形成氢氧化物沉淀时的pH(开始沉淀的pH按金属离子浓度为1.0 mol•L-1计算):
(1)“酸浸”时使用的酸X为___ , SO2的作用是______ 。
(2)“氧化”过程中主要反应的离子方程式是______ 。加入石灰浆调节溶液pH范围是______ 。
(3)MnSO4可用于测定水中溶解氧的含量,步骤如下:
步骤1:取100.00mL水样于锥形瓶中,迅速加入足量MnSO4溶液及碱性KI溶液,发生反应:2Mn2++O2+4OH-= 2MnO(OH)2↓,密封静置。
步骤2:向锥形瓶中加入适量稀H2SO4, MnO(OH)2与I-完全反应生成Mn2+和I2后加入几滴淀粉溶液。
步骤3:用5.000×10-3mol•L-1Na2S2O3溶液进行滴定,发生反应:I2+2 Na2S2O3= Na2S4O6+2NaI。滴定至终点时共消耗Na2S2O3溶液16.00 mL。
①步骤2中MnO(OH)2与I-反应的离子方程式为_________ 。
②步骤3中滴定终点的实验现象为______ 。
③步骤l中需迅速加入相关试剂并密封的原因是___ 。
④计算该水样中溶解氧的含量(用mg•L-1表示)___ 。(写出计算过程)

已知:①“酸浸”后的溶液pH< 1,除含Mn2+外,还含有少量Fe2+、Al3+、Ca2+等金属离子。
②下表列出相关金属离子形成氢氧化物沉淀时的pH(开始沉淀的pH按金属离子浓度为1.0 mol•L-1计算):
| 金属离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 5.8 | 8.8 |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Mn2+ | 7.3 | 10.3 |
(1)“酸浸”时使用的酸X为
(2)“氧化”过程中主要反应的离子方程式是
(3)MnSO4可用于测定水中溶解氧的含量,步骤如下:
步骤1:取100.00mL水样于锥形瓶中,迅速加入足量MnSO4溶液及碱性KI溶液,发生反应:2Mn2++O2+4OH-= 2MnO(OH)2↓,密封静置。
步骤2:向锥形瓶中加入适量稀H2SO4, MnO(OH)2与I-完全反应生成Mn2+和I2后加入几滴淀粉溶液。
步骤3:用5.000×10-3mol•L-1Na2S2O3溶液进行滴定,发生反应:I2+2 Na2S2O3= Na2S4O6+2NaI。滴定至终点时共消耗Na2S2O3溶液16.00 mL。
①步骤2中MnO(OH)2与I-反应的离子方程式为
②步骤3中滴定终点的实验现象为
③步骤l中需迅速加入相关试剂并密封的原因是
④计算该水样中溶解氧的含量(用mg•L-1表示)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网