解答题-原理综合题 较难0.4 引用1 组卷95
甲醇是重要的化工原料。在催化剂的作用下,利用合成气(主要成分为CO、CO2和H2)合成甲醇的主要化学反应如下:
Ⅰ.CO+2H2 CH3OH
CH3OH
Ⅱ.CO2+3H2 CH3OH+H2O
CH3OH+H2O
Ⅲ.CO2+H2 CO+H2O
CO+H2O
请回答下列问题:
(1)已知三种物质的标准燃烧热如下表:
①书写25℃、101kPa条件时CO燃烧热的热化学方程式____________ 。
②计算25℃、101kPa条件时反应Ⅰ的ΔH=_____ kJ·mol−1 。
(2)甲醇燃料电池(Direct Methanol Fuel Cell)属于质子交换膜燃料电池,其工作原理如图所示:
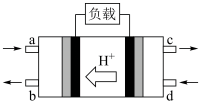
①c处产生的气体是_______________ ;
②负极的电极反应式是_______________ 。
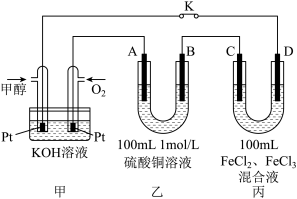
(3)下图是甲醇燃料电池工作示意图,其中A,B,D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A,B两极上产生的气体体积相同。
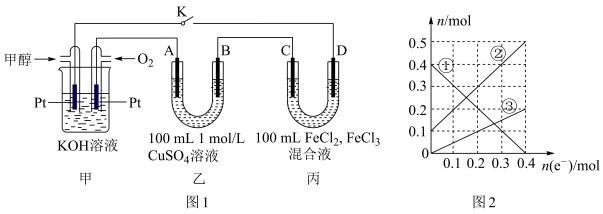
①乙中B极的电极反应式_______ 。
②乙中A极析出的气体在标况下的体积________ 。
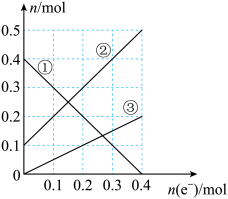
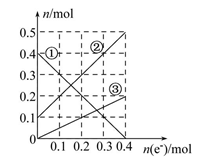
③丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则②线表示的是____ 的变化,反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要____ mL 5mol/LNaOH溶液。
(4)蓄电池是一种反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应如下:NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
①此蓄电池在充电时,电池负极应与外加电源的________ 极连接。
②放电时正极的电极反应式为_____________________ 。
(5)按如图所示装置进行下列不同的操作
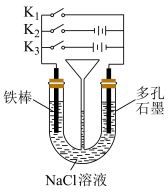
①将K1、K2、 K3分别只关闭一个,则铁的腐蚀的速度最快的是只闭合_____ (填“K1”或 “K2”或“K3”,下同),为减缓铁的腐蚀, 只闭合_____ ,该防护法称为______________ 。
②只闭合K3,当铁棒质量减少5.6g时,石墨电极消耗的气体体积为__________ L(标准状况)。
Ⅰ.CO+2H2
 CH3OH
CH3OHⅡ.CO2+3H2
 CH3OH+H2O
CH3OH+H2OⅢ.CO2+H2
 CO+H2O
CO+H2O请回答下列问题:
(1)已知三种物质的标准燃烧热如下表:
| 物质 | CO(g) | H2(g) | CH3OH(l) |
| 燃烧热(kJ·mol−1) | −283.0 | −285.8 | −726.5 |
②计算25℃、101kPa条件时反应Ⅰ的ΔH=
(2)甲醇燃料电池(Direct Methanol Fuel Cell)属于质子交换膜燃料电池,其工作原理如图所示:

①c处产生的气体是
②负极的电极反应式是
(3)下图是甲醇燃料电池工作示意图,其中A,B,D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A,B两极上产生的气体体积相同。

①乙中B极的电极反应式
②乙中A极析出的气体在标况下的体积
③丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则②线表示的是
(4)蓄电池是一种反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应如下:NiO2+Fe+2H2O
 Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。①此蓄电池在充电时,电池负极应与外加电源的
②放电时正极的电极反应式为
(5)按如图所示装置进行下列不同的操作

①将K1、K2、 K3分别只关闭一个,则铁的腐蚀的速度最快的是只闭合
②只闭合K3,当铁棒质量减少5.6g时,石墨电极消耗的气体体积为
19-20高二上·山东济南·阶段练习
类题推荐
甲醇是重要的工业原料。煤化工可以利用煤炭制取水煤气从而合成甲醇:
CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
已知①常压下反应的能量变化如图所示。
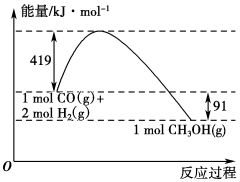
②
③CO(g)+1/2O2(g)=CO2(g)ΔH=-280 kJ/mol;
H2(g)+1/2O2(g)=H2O(l) ΔH=-284 kJ/mol
H2O(l)=H2O(g) ΔH=+44 kJ/mol
请回答下列问题:
(1)请写出表示气态甲醇燃烧热的热化学方程式_______________________ 。
(2)H—O键的键能x为________ kJ/mol。
(3)在____ (填“高温”或“低温”)情况下有利于CO和H2制备甲醇的反应自发进行。
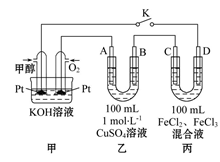
(4)某兴趣小组同学利用甲醇燃料电池探究电浮选法处理污水的一种方式:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3具有吸附性,可吸附污物而沉积下来,具有净化水的作用。装置如图所示。
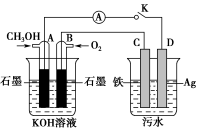
甲 乙
①写出甲池的A极电极反应式:__________________________ 。
②若乙池实验时污水中离子浓度较小,导电能力较差,净水效果不好,此时应向污水中加入适量的________ 。
A.H2SO4 B.BaSO4 C.Na2SO4 D.NaOH E.CH3CH2OH
(5)下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
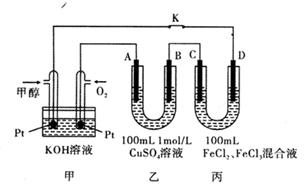
①乙中A极析出的气体在标准状况下的体积为____ 。
②丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则图中②线表示的是__________ 离子的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要__________ mL 5.0 mol/L NaOH溶液。

CO(g)+2H2(g)
 CH3OH(g)。
CH3OH(g)。已知①常压下反应的能量变化如图所示。

②
| 化学键 | H—H | H—O | O=O |
| 键能kJ/mol | 436 | x | 496 |
③CO(g)+1/2O2(g)=CO2(g)ΔH=-280 kJ/mol;
H2(g)+1/2O2(g)=H2O(l) ΔH=-284 kJ/mol
H2O(l)=H2O(g) ΔH=+44 kJ/mol
请回答下列问题:
(1)请写出表示气态甲醇燃烧热的热化学方程式
(2)H—O键的键能x为
(3)在
(4)某兴趣小组同学利用甲醇燃料电池探究电浮选法处理污水的一种方式:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3具有吸附性,可吸附污物而沉积下来,具有净化水的作用。装置如图所示。

甲 乙
①写出甲池的A极电极反应式:
②若乙池实验时污水中离子浓度较小,导电能力较差,净水效果不好,此时应向污水中加入适量的
A.H2SO4 B.BaSO4 C.Na2SO4 D.NaOH E.CH3CH2OH
(5)下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

①乙中A极析出的气体在标准状况下的体积为
②丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则图中②线表示的是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网