解答题-实验探究题 较难0.4 引用1 组卷138
苯甲酸乙酯可由苯甲酸与乙醇在浓硫酸共热下反应制得(已知苯甲酸的酸性强于碳酸),反应装置如图(部分装置省略),反应原理如下:

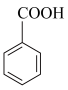 +C2H5OH
+C2H5OH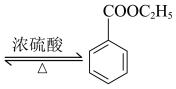 +H2O
+H2O
实验操作步骤:
①向三颈烧瓶内加入12.2 g苯甲酸、25 mL乙醇、20 mL苯及4 mL浓硫酸,摇匀,加入沸石。
②装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
③将反应液倒入盛有80 mL冷水的烧杯中,在搅拌下分批加入碳酸钠粉末至溶液无二氧化碳逸出,用pH试纸检验至呈中性。
④用分液漏斗分出有机层,水层用25 mL乙醚萃取,然后合并至有机层。用无水CaC12干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收210—213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8 mL。
可能用到的有关数据如下:
回答以下问题:
(1)反应装置中分水器上方的仪器名称是______
(2)步骤①中加浓硫酸的作用是________ ,加沸石的目的是______ 。
(3)步骤②中使用分水器除水的目的是__________ 。
(4)步骤③中加入碳酸钠的目的是____________ 。
(5)步骤④中有机层从分液漏斗的____ (选填“上口倒出”或“下口放出”)。
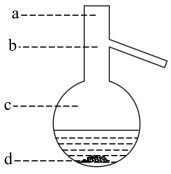
(6)蒸馏操作中温度计水银球的位置应为下图中________ (填a、b、c、d)所示。
(7)本实验所得到的苯甲酸乙酯产率______ %。

 +C2H5OH
+C2H5OH +H2O
+H2O实验操作步骤:
①向三颈烧瓶内加入12.2 g苯甲酸、25 mL乙醇、20 mL苯及4 mL浓硫酸,摇匀,加入沸石。
②装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
③将反应液倒入盛有80 mL冷水的烧杯中,在搅拌下分批加入碳酸钠粉末至溶液无二氧化碳逸出,用pH试纸检验至呈中性。
④用分液漏斗分出有机层,水层用25 mL乙醚萃取,然后合并至有机层。用无水CaC12干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收210—213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8 mL。
可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 苯甲酸 | 122 | 1.27 | 249 | 微溶于水,易溶于乙醇、乙醚 |
| 苯甲酸乙酯 | 150 | 1.05 | 211~213 | 微溶于水,溶于乙醇、乙醚 |
| 乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
| 乙醚 | 74 | 0.73 | 34.4 | 微溶于水 |
(1)反应装置中分水器上方的仪器名称是
(2)步骤①中加浓硫酸的作用是
(3)步骤②中使用分水器除水的目的是
(4)步骤③中加入碳酸钠的目的是
(5)步骤④中有机层从分液漏斗的
(6)蒸馏操作中温度计水银球的位置应为下图中

(7)本实验所得到的苯甲酸乙酯产率
19-20高二上·安徽六安·阶段练习
类题推荐
苯甲酸乙酯制备原理:苯甲酸和乙醇在浓硫酸的催化下进行酯化反应,可以生成苯甲酸乙酯与水。由于苯甲酸乙酯的沸点较高,很难蒸出,所以本实验采用加入环己烷的方法,使环己烷、乙醇和水形成三元共沸物,其沸点为62.1℃。三元共沸物经过冷凝回流形成两相,其中环己烷在上层的比例大,再流回反应瓶;水在下层的比例大,放出下层即可除去反应生成的水。装置图:

实验步骤:
①加料:在50mL圆底烧瓶中加入6.1g苯甲酸、13mL乙醇、10mL环己烷、2.0mL浓硫酸,摇匀,加沸石。按照装置图左图组装好仪器(安装分水器,分水器上端接一冷凝管),从分水器上端小心加水至分水器支管处,然后再放去一部分水使液面离分水器支管口约0.5cm。
②分水回流:将烧瓶在水浴上加热回流,开始时回流速度要慢。随着回流的进行,分水器中出现了上、中、下三层液体。当中、下层接近分水器支管时,将中、下层液体放入量筒中。
③中和:将反应液倒入盛有30mL水的烧杯中,分批加入碳酸钠粉末至溶液呈中性(或弱碱性),无二氧化碳逸出,用pH试纸检验。
④分离萃取、干燥、蒸馏:用分液漏斗分出有机层,将水层溶液用25mL乙醚萃取,然后合并至有机层。用无水MgSO4干燥,对粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收一定温度下的馏分,得产品约5.7mL。
回答下列问题:
(1)反应容器中制取苯甲酸乙酯的化学方程式为___________ ,装置图中仪器A的名称是___________ 。
(2)本实验采取了多种措施来提高酯的产率,请写出其中两种___________ 。
(3)在制备苯甲酸乙酯时,加入环己烷的作用是___________ 。
(4)用乙醚萃取后要把___________ (填字母序号)的液体合并至有机层。
a、从分液漏斗下部流出的b、从分液漏斗上口倒出的
(5)步骤4收集馏分应控制的最佳温度范围为___________ ℃。本实验的产率为___________ (保留小数点后1位)。

| 试剂 | 相对分子质量 | 密度(g/cm3) | 沸点/℃ | 在水中的溶解性 |
| 乙醇 | 46 | 0.7893 | 78.5 | 易溶 |
| 苯甲酸 | 122 | 1.2659 | 249 | 微溶 |
| 环己烷 | 84 | 0.7785 | 80 | 难溶 |
| 乙醚 | 74 | 0.7318 | 34.51 | 难溶 |
| 苯甲酸乙酯 | 150 | 1.05 | 211~213 | 微溶 |
①加料:在50mL圆底烧瓶中加入6.1g苯甲酸、13mL乙醇、10mL环己烷、2.0mL浓硫酸,摇匀,加沸石。按照装置图左图组装好仪器(安装分水器,分水器上端接一冷凝管),从分水器上端小心加水至分水器支管处,然后再放去一部分水使液面离分水器支管口约0.5cm。
②分水回流:将烧瓶在水浴上加热回流,开始时回流速度要慢。随着回流的进行,分水器中出现了上、中、下三层液体。当中、下层接近分水器支管时,将中、下层液体放入量筒中。
③中和:将反应液倒入盛有30mL水的烧杯中,分批加入碳酸钠粉末至溶液呈中性(或弱碱性),无二氧化碳逸出,用pH试纸检验。
④分离萃取、干燥、蒸馏:用分液漏斗分出有机层,将水层溶液用25mL乙醚萃取,然后合并至有机层。用无水MgSO4干燥,对粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收一定温度下的馏分,得产品约5.7mL。
回答下列问题:
(1)反应容器中制取苯甲酸乙酯的化学方程式为
(2)本实验采取了多种措施来提高酯的产率,请写出其中两种
(3)在制备苯甲酸乙酯时,加入环己烷的作用是
(4)用乙醚萃取后要把
a、从分液漏斗下部流出的b、从分液漏斗上口倒出的
(5)步骤4收集馏分应控制的最佳温度范围为
苯甲酸乙酯用于配制香水香精和人造精油,也大量用于食品中。实验室可通过反应 +CH3CH2OH
+CH3CH2OH
 +H2O制备。实验装置如图所示:
+H2O制备。实验装置如图所示:

所用试剂的性质如下表所示:
环己烷、乙醇和水可形成三元共沸物,其沸点为62.1℃(即此温度下,水、乙醇、环己烷以一定比例成为蒸汽逸出)。
实验步骤:
①向50mL圆底烧瓶中依次加入4g苯甲酸、10mL乙醇(过量)、8mL环己烷和3mL浓硫酸,摇匀,加入几粒沸石。按照图1所示实验装置组装好仪器,加热烧瓶,开始回流。开始时回流要慢,随着回流的进行,分水器中出现上下两层。当下层接近分水器支管时将下层液体放入量筒中。
②继续加热,至烧瓶内有白烟或回流下来液体无滴状(约2h),停止加热。
③将反应液倒入盛有30ml水的烧杯中,分批加入碳酸钠粉末至溶液呈中性(或弱碱性)。
④用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层。加入物质X干燥,粗产物利用图2所示装置进行蒸馏。
回答下列问题:
(1)仪器a的名称为_______ ,图2装置中冷却水的出口为_______ (填“m”或“n”)。
(2)加入环己烷的目的为_______ 。
(3)加入碳酸钠可除去的物质为_______ (填名称)。
(4)物质X应选择_______ (填选项字母)。
A.碱石灰 B.MgSO4 C.P2O5
(5)水层用25mL乙醚萃取,然后合并至有机层的目的为_______ 。
(6)蒸馏时优先蒸出的物质为_______ (填名称);若蒸馏后所得产品的质量为2.350g,则该实验的产率为_______ %(保留四位有效数字)。
 +CH3CH2OH
+CH3CH2OH +H2O制备。实验装置如图所示:
+H2O制备。实验装置如图所示:
所用试剂的性质如下表所示:
| 名称 | 相对分子质量 | 熔点、沸点/℃ | 溶解性 | ||
| 水 | 醇 | 醚 | |||
| 苯甲酸 | 122 | 122.1、249 | 微溶 | 溶 | 溶 |
| 苯甲酸乙酯 | 150 | -34.6、212.6 | 微溶 | 溶 | 溶 |
| 乙醇 | 46 | -114.1、78.3 | 混溶 | 溶 | 溶 |
| 环己烷 | 84 | 6.5、80.7 | 不溶 | 溶 | 溶 |
| 乙醚 | 74 | -116.2、34.5 | 微溶 | 溶 | 溶 |
实验步骤:
①向50mL圆底烧瓶中依次加入4g苯甲酸、10mL乙醇(过量)、8mL环己烷和3mL浓硫酸,摇匀,加入几粒沸石。按照图1所示实验装置组装好仪器,加热烧瓶,开始回流。开始时回流要慢,随着回流的进行,分水器中出现上下两层。当下层接近分水器支管时将下层液体放入量筒中。
②继续加热,至烧瓶内有白烟或回流下来液体无滴状(约2h),停止加热。
③将反应液倒入盛有30ml水的烧杯中,分批加入碳酸钠粉末至溶液呈中性(或弱碱性)。
④用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层。加入物质X干燥,粗产物利用图2所示装置进行蒸馏。
回答下列问题:
(1)仪器a的名称为
(2)加入环己烷的目的为
(3)加入碳酸钠可除去的物质为
(4)物质X应选择
A.碱石灰 B.MgSO4 C.P2O5
(5)水层用25mL乙醚萃取,然后合并至有机层的目的为
(6)蒸馏时优先蒸出的物质为
苯甲酸乙酯稍有水果气味,用于配制香水香精和人造精油,也大量用于食品中。制备原理:苯甲酸和乙醇在浓硫酸的催化下进行酯化反应,可以生成苯甲酸乙酯与水。
由于苯甲酸乙酯的沸点较高,很难蒸出,所以本实验采用加入环己烷的方法,使环己烷、乙醇和水形成三元共沸物,其沸点为62.1℃。三元共沸物经过冷凝回流形成两相,其中环己烷在上层的比例大,再流回反应瓶;水在下层的比例大,放出下层即可除去反应生成的水。
装置图:
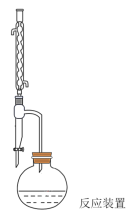

实验步骤:
①加料:在50 mL圆底烧瓶中加入6.1 g苯甲酸、13 mL乙醇、10 mL环己烷、2.0 mL浓硫酸,摇匀,加沸石。按照装置图左图组装好仪器(安装分水器,分水器上端接一冷凝管) ,从分水器上端小心加水至分水器支管处,然后再放去一部分 水使液面离分水器支管口约0.5 cm。
②分水回流:将烧瓶在水浴上加热回流,开始时回流速度要慢。随着回流的进行,分水器中出现了上、中、下三层液体。当中、下层接近分水器支管时,将中、下层液体放入量筒中。
③中和:将反应液倒入盛有30 mL水的烧杯中,分批加入碳酸钠粉末至溶液呈中性(或弱碱性),无二氧化碳逸出,用pH试纸检验。
④分离萃取、干燥、蒸馏:用分液漏斗分出有机层,将水层溶液用25 mL乙醚萃取,然后合并至有机层。用无水MgSO4干燥,对粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收一定温度下的馏分,得产品约5.7 mL。
回答下列问题:
(1)反应容器中制取苯甲酸乙酯的化学方程式为_____________ ,装置图中仪器A的名称是______ 。
(2)本实验采取了多种措施来提高酯的产率,请写出其中两种____________________ 。
(3)在制备苯甲酸乙酯时,加入环己烷的作用是________________ 。
(4)步骤3中和时,加入碳酸钠粉末要分批的原因是_____________ 。
(5)用乙醚萃取后要把____________ (填字母序号)的液体合并至有机层。
a.从分液漏斗下部流出的 b.从分液漏斗.上口倒出的
(6)步骤4收集馏分应控制的最佳温度范围为________________ ℃。本实验的产率为________ (保留小数点后1位)。
由于苯甲酸乙酯的沸点较高,很难蒸出,所以本实验采用加入环己烷的方法,使环己烷、乙醇和水形成三元共沸物,其沸点为62.1℃。三元共沸物经过冷凝回流形成两相,其中环己烷在上层的比例大,再流回反应瓶;水在下层的比例大,放出下层即可除去反应生成的水。
装置图:


| 试剂 | 相对分子质量 | 密度/(g/cm3) | 沸点/℃ | 在水中的溶解性 |
| 乙醇 | 46 | 0.7893 | 78.5 | 易溶 |
| 苯甲酸 | 122 | 1.2659 | 249 | 微溶 |
| 环己烷 | 84 | 0.7785 | 80 | 难溶 |
| 乙醚 | 74 | 0.7318 | 34.51 | 难溶 |
| 苯甲酸乙酯 | 150 | 1.05 | 211 ~ 213 | 微溶 |
实验步骤:
①加料:在50 mL圆底烧瓶中加入6.1 g苯甲酸、13 mL乙醇、10 mL环己烷、2.0 mL浓硫酸,摇匀,加沸石。按照装置图左图组装好仪器(安装分水器,分水器上端接一冷凝管) ,从分水器上端小心加水至分水器支管处,然后再放去一部分 水使液面离分水器支管口约0.5 cm。
②分水回流:将烧瓶在水浴上加热回流,开始时回流速度要慢。随着回流的进行,分水器中出现了上、中、下三层液体。当中、下层接近分水器支管时,将中、下层液体放入量筒中。
③中和:将反应液倒入盛有30 mL水的烧杯中,分批加入碳酸钠粉末至溶液呈中性(或弱碱性),无二氧化碳逸出,用pH试纸检验。
④分离萃取、干燥、蒸馏:用分液漏斗分出有机层,将水层溶液用25 mL乙醚萃取,然后合并至有机层。用无水MgSO4干燥,对粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收一定温度下的馏分,得产品约5.7 mL。
回答下列问题:
(1)反应容器中制取苯甲酸乙酯的化学方程式为
(2)本实验采取了多种措施来提高酯的产率,请写出其中两种
(3)在制备苯甲酸乙酯时,加入环己烷的作用是
(4)步骤3中和时,加入碳酸钠粉末要分批的原因是
(5)用乙醚萃取后要把
a.从分液漏斗下部流出的 b.从分液漏斗.上口倒出的
(6)步骤4收集馏分应控制的最佳温度范围为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


