解答题-工业流程题 适中0.65 引用1 组卷75
纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用。某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如下:
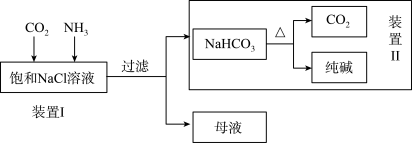
(1)工业生产纯碱的第一步是除去饱和食盐水的中SO42-、Ca2+离子,依次加入的试剂及其用量是______________ 、_______________ 、过滤、_______________ 。
(2)已知:几种盐的溶解度
①写出装置I中反应的化学方程式_____________________________________ 。
②写出装置Ⅱ中发生反应的化学方程式________________________________ 。
(3)该流程中可循环利用的物质是__________________ 。
(4)若制出的纯碱中只含有杂质NaCl。
①检验用该纯碱配制的溶液中含有Cl―的方法是_________________________ 。
②向m克纯碱样品中加入足量CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为b g,则该纯碱的纯度(质量分数)为__________ (用m、b来表示)。

(1)工业生产纯碱的第一步是除去饱和食盐水的中SO42-、Ca2+离子,依次加入的试剂及其用量是
(2)已知:几种盐的溶解度
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
| 溶解度(20°C,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
②写出装置Ⅱ中发生反应的化学方程式
(3)该流程中可循环利用的物质是
(4)若制出的纯碱中只含有杂质NaCl。
①检验用该纯碱配制的溶液中含有Cl―的方法是
②向m克纯碱样品中加入足量CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为b g,则该纯碱的纯度(质量分数)为
19-20高一上·山西长治·阶段练习
类题推荐
纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用。
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为____________________ 、____________________ 。某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如下:

已知:几种盐的溶解度
(2)①写出装置I中反应的化学方程式______________ 。
②从平衡移动角度解释该反应发生的原因______________ 。
③操作①的名称是______________ 。
(3)写出装置II中发生反应的化学方程式______________ 。
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用______________ 。
(5)该流程中可循环利用的物质是______________ 。
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行 的是______________ 。
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为

已知:几种盐的溶解度
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
| 溶解度(20°C,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
②从平衡移动角度解释该反应发生的原因
③操作①的名称是
(3)写出装置II中发生反应的化学方程式
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用
(5)该流程中可循环利用的物质是
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用。
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为_____ 、_____ 。
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

已知:几种盐的溶解度
(2)①写出装置I中反应的化学方程式_____ 。
②从平衡移动角度解释该反应发生的原因_____ 。
(3)写出装置II中发生反应的化学方程式_____ 。
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用_____ 。
(5)该流程中可循环利用的物质是_____ 。
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是_____ 。
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

已知:几种盐的溶解度
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
| 溶解度(20℃,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
②从平衡移动角度解释该反应发生的原因
(3)写出装置II中发生反应的化学方程式
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用
(5)该流程中可循环利用的物质是
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用。
(1)工业生产纯碱的第一步是除去饱和食盐水的中 离子,按先后顺序依次加入试剂的化学式为
离子,按先后顺序依次加入试剂的化学式为_______ 、_______ 。
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如下:

已知:几种盐的溶解度
(2)①写出装置I中反应的化学方程式_______ 。
②装置I的两种气体,先通_______ ,后通_______ 。
③操作①的名称是_______ 。
(3)写出装置Ⅱ中发生反应的化学方程式_______ 。
(4)请结合化学平衡说明装置III中加入磨细的食盐粉及 的作用
的作用_______ 。
(5)该流程中可循环利用的物质是_______ 。
(6)制出的纯碱中含有杂质 ,为测定其纯度,下列方案中
,为测定其纯度,下列方案中不可行 的是_______ 。
a.向m克纯碱样品中加入足量 溶液,测生成
溶液,测生成 的质量
的质量
b.向m克纯碱样品中加入足量稀 ,干燥后测生成气体的体积
,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量 溶液,测生成沉淀的质量
溶液,测生成沉淀的质量
(1)工业生产纯碱的第一步是除去饱和食盐水的中
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如下:

已知:几种盐的溶解度
| 溶解度( | 36.0 | 21.7 | 9.6 | 37.2 |
②装置I的两种气体,先通
③操作①的名称是
(3)写出装置Ⅱ中发生反应的化学方程式
(4)请结合化学平衡说明装置III中加入磨细的食盐粉及
(5)该流程中可循环利用的物质是
(6)制出的纯碱中含有杂质
a.向m克纯碱样品中加入足量
b.向m克纯碱样品中加入足量稀
c.向m克纯碱样品中加入足量
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


