填空题 适中0.65 引用1 组卷30
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)⇌2SO3(g) △H<0;
(1)写出该反应的化学平衡常数表达式K=__________
(2)降低温度,该反应K值__________ ,二氧化硫转化率___________ ,化学反应速率___________ (以上均填增大、减小或不变)。
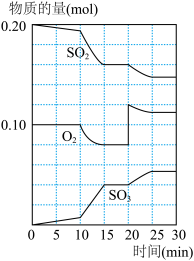
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态时间是___________________________ 。
(4)据图判断,反应进行至20min时,曲线发生变化的原因是_______________________ (用文字表达)。
(5)10min到15min的曲线变化的原因可能是____________ (填写编号)。
A、加了催化剂 B、缩小容器体积
C、降低温度 D、增加SO3的物质的量。
(6)若该反应的密闭容器为2L,则反应15min时,v(SO2)=___________
(7)为使该反应的反应速率增大,且平衡向正反应方向移动的是( )
A、及时分离出SO3气体 B、适当升高温度
C、增大O2的浓度 D、选择高效的催化剂
(1)写出该反应的化学平衡常数表达式K=
(2)降低温度,该反应K值

(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态时间是
(4)据图判断,反应进行至20min时,曲线发生变化的原因是
(5)10min到15min的曲线变化的原因可能是
A、加了催化剂 B、缩小容器体积
C、降低温度 D、增加SO3的物质的量。
(6)若该反应的密闭容器为2L,则反应15min时,v(SO2)=
(7)为使该反应的反应速率增大,且平衡向正反应方向移动的是
A、及时分离出SO3气体 B、适当升高温度
C、增大O2的浓度 D、选择高效的催化剂
19-20高二上·甘肃白银·阶段练习
类题推荐
在一定条件下,存在如下反应:2SO2(g)+ O2(g) 2SO3(g);ΔH<0
2SO3(g);ΔH<0
(1)写出该反应的化学平衡常数表达式K=_____________________________
(2)升高温度,该反应K值______ ,SO2转化率_______ ,正反应速率_____ (填增大、减小或不变)
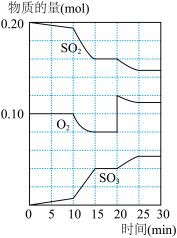
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是__________________________________

(4)据图判断,反应进行至20min时,曲线发生变化的原因 是__________ (用文字表达),10min到15min的曲线变化的原因可能是____________ (填编号)。
(5)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显_______ 性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________________ 。
 2SO3(g);ΔH<0
2SO3(g);ΔH<0(1)写出该反应的化学平衡常数表达式K=
(2)升高温度,该反应K值
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是

(4)据图判断,反应进行至20min时,曲线发生变化的原因 是
| A.加了催化剂 | B.缩小容器体积 |
| C.降低温度 | D.增加SO3物质的量 |
(5)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 2SO3(g) ΔH<0
2SO3(g) ΔH<0