解答题-原理综合题 适中0.65 引用2 组卷126
Ⅰ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K =_______ 。
(2)该反应为______ 反应(选填“吸热”、“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_____ 。
a.容器中压强不变 b.υ正(H2)=υ逆(H2O)
c. c(CO2)=c(CO) d.混合气体中 c(CO)不变
(4) 830K时,各物质浓度符合下式:2c(CO2)·c(H2)=c(CO)·c(H2O),此时该反应_______ (填“正反应方向进行”、“逆反应方向进行”或“处于平衡状态”)。
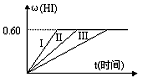
Ⅱ.将1 mol I2(g) 和2 mol H2置于2 L密闭容器中,在一定温度下发生反应: I2(g) + H2(g) 2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
(1)若5分钟该达平衡,则用H2表示的反应速率为________ 。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,则甲条件可能是____ 。(填入下列条件的序号)
①恒温条件下,缩小反应容器体积;②恒温条件下,扩大反应容器体积;③恒容条件下,降低温度;④恒容条件下,升高温度;⑤恒温恒容条件下,加入适当催化剂。
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K =
(2)该反应为
(3)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.υ正(H2)=υ逆(H2O)
c. c(CO2)=c(CO) d.混合气体中 c(CO)不变
(4) 830K时,各物质浓度符合下式:2c(CO2)·c(H2)=c(CO)·c(H2O),此时该反应
Ⅱ.将1 mol I2(g) 和2 mol H2置于2 L密闭容器中,在一定温度下发生反应: I2(g) + H2(g)
(1)若5分钟该达平衡,则用H2表示的反应速率为
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,则甲条件可能是
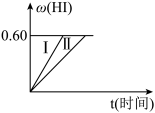
①恒温条件下,缩小反应容器体积;②恒温条件下,扩大反应容器体积;③恒容条件下,降低温度;④恒容条件下,升高温度;⑤恒温恒容条件下,加入适当催化剂。
19-20高二上·四川广元·期中
类题推荐
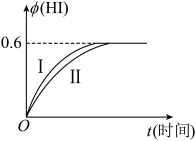
将1molI2(g)和2molH2(g)置于某2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)  2HI(g) △H<0,并在10min时达到平衡。HI的体积分数
2HI(g) △H<0,并在10min时达到平衡。HI的体积分数 (HI)随时间变化如图所示曲线(Ⅱ)。
(HI)随时间变化如图所示曲线(Ⅱ)。
(1)在此条件下,下列能说明该反应达到平衡状态的是___________(填序号)。
(2)在达平衡过程中用HI(g)表示的反应速率为___________ ;I2(g)的平衡转化率为_______________ 。
(3)在此温度下,该反应的平衡常数K=_______ (保留一位小数),若保持温度、体积不变,向已平衡的体系中再充入I2(g)和HI(g)各1mol,此时平衡___________ (填“向左移动”“向右移动”或“不移动”)。
(4)若改变反应条件,在某条件下 (HI)的变化如曲线(Ⅰ)所示,则该条件可能是
(HI)的变化如曲线(Ⅰ)所示,则该条件可能是____________ (填序号)。
①恒容条件下,降低温度
②恒温条件下,缩小反应容器体积
③恒温条件下,扩大反应容器体积
④恒温、恒容条件下,加入适当催化剂
(5)若保持温度不变,在另一相同的2L密闭容器中加入amolI2(g)、 bmolH2(g)和cmolHI(g)(a、b、c均大于0),发生反应达平衡时,HI体积分数仍为0.60,则a、b、c的关系为__________________ (用一个含a、b、c的代数式表示)。
 2HI(g) △H<0,并在10min时达到平衡。HI的体积分数
2HI(g) △H<0,并在10min时达到平衡。HI的体积分数(1)在此条件下,下列能说明该反应达到平衡状态的是___________(填序号)。

| A.混合气体密度不再变化 |
| B.反应混合物中H2的浓度不变 |
| C.混合气体的颜色不再变化 |
| D.每消耗1molH2同时消耗1molI2 |
(3)在此温度下,该反应的平衡常数K=
(4)若改变反应条件,在某条件下
①恒容条件下,降低温度
②恒温条件下,缩小反应容器体积
③恒温条件下,扩大反应容器体积
④恒温、恒容条件下,加入适当催化剂
(5)若保持温度不变,在另一相同的2L密闭容器中加入amolI2(g)、 bmolH2(g)和cmolHI(g)(a、b、c均大于0),发生反应达平衡时,HI体积分数仍为0.60,则a、b、c的关系为
在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g) CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_____________________________ ,该反应为_______________ 反应(选吸热或放热)。
若改变条件使平衡向正反应方向移动,则平衡常数_________ (填序号)
①一定不变 ②一定减小 ③可能增大 ④增大、减小、不变皆有可能
(2)能判断该反应是否达到化学平衡状态的依据是___________
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO)=c(CO2)
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验1中以v(CO2) 表示的反应速率为____________ 。实验2达到平衡所需时间比实验1所需时间短的原因是_________________________________________________________ 。
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的化学平衡常数表达式为K=
若改变条件使平衡向正反应方向移动,则平衡常数
①一定不变 ②一定减小 ③可能增大 ④增大、减小、不变皆有可能
(2)能判断该反应是否达到化学平衡状态的依据是
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO)=c(CO2)
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡 所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 2HI(g)
2HI(g)