解答题-原理综合题 适中0.65 引用1 组卷65
氮氧化物(NOx)是一种主要的大气污染物,必须进行处理。
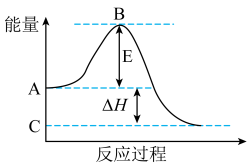
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①ΔH 1_____ 0,ΔH 3_____ 0。(填“>”或“<”)
②N2(g)+O2(g) = 2NO(g) ΔH=______ kJ·mol-1。
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) =5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是_______ (填字母)。
A.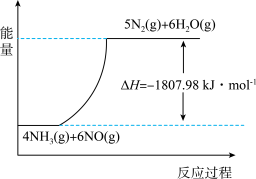
B.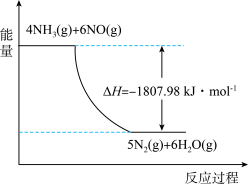
C.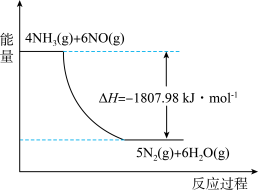
(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
H2O(l) = H2O(g) ΔH=+44 kJ·mol-1
则CH4 (g)+2NO2(g)=N2 (g)+CO2(g)+2H2O(g) ΔH=________ ,1.6 g CH4还原NO2 生成N2和液态水时放出的热量为______ kJ。
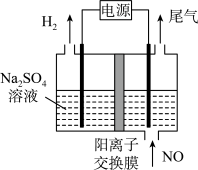
(4)利用电解法处理含氮氧化物的废气。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极),电解过程中NO转化为硝酸的化学方程式为______ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | ΔH 1 | ΔH 2 | ΔH 3 |
| 热量值kJ·mol-1 | 945 | 498 | 630 |
①ΔH 1
②N2(g)+O2(g) = 2NO(g) ΔH=
(2)利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3 (g)+6NO(g) =5N2(g)+6H2O(g) ΔH=-1807.98 kJ·mol-1,下列能表示该反应中能量变化的是
A.

B.

C.

(3)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
H2O(l) = H2O(g) ΔH=+44 kJ·mol-1
则CH4 (g)+2NO2(g)=N2 (g)+CO2(g)+2H2O(g) ΔH=
(4)利用电解法处理含氮氧化物的废气。实验室模拟电解法吸收NO,装置如图所示(均为石墨电极),电解过程中NO转化为硝酸的化学方程式为

19-20高二上·江苏扬州·期中
类题推荐
氮氧化物(NO2)是一种主要的大气污染物,必须进行处理。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①△H1___ 0,△H3____ 0。(填“>”或“<”)
②N2(g)+O2(g)=2NO(g)△H=____ kJ·mol-1。
(2)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-l
CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g)AH=-1160 kJ·mol-l
H2O(l)=H2O(g)△H=+44kJ·mol-l
CH4与NO2反应生成N2和H2O(l)的热化学方程式为_______ 。
(3)潜艇中使用的液氮-液氧燃料电池工作原理如图所示:
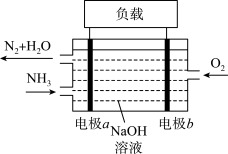
①电极a名称是______ 。
②电解质溶液中OH-离子向_____ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为_____ 。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是_____ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | △H1 | △H2 | △H3 |
| 热量值kJ/mol | 945 | 498 | 630 |
①△H1
②N2(g)+O2(g)=2NO(g)△H=
(2)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-l
CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g)AH=-1160 kJ·mol-l
H2O(l)=H2O(g)△H=+44kJ·mol-l
CH4与NO2反应生成N2和H2O(l)的热化学方程式为
(3)潜艇中使用的液氮-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OH-离子向
③电极b的电极反应式为
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是
回答下列问题:
(1)氮氧化物(NOx)是一种主要的大气污染物,必须进行处理。
①利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ΔH=-1807.98kJ·mol-1,下列能表示该反应中能量变化的是_______ (填字母)。
A.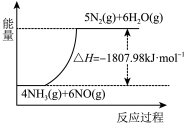 B.
B.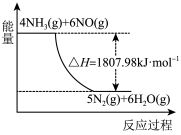 C.
C.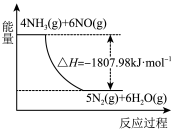
②利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ·mol-1
H2O(l)=H2O(g) ΔH=+44kJ·mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=_______ ,1.6gCH4还原NO2生成N2和液态水时放出的热量为_______ kJ。
(2)由 羟基丁酸(
羟基丁酸( )生成
)生成 丁内酯(
丁内酯(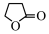 )的反应如下:
)的反应如下:

 。在25℃时,溶液中
。在25℃时,溶液中 羟基丁酸的初始浓度为0.180mol/L,随着反应的进行,测得
羟基丁酸的初始浓度为0.180mol/L,随着反应的进行,测得 丁内酯浓度随时间的变化如下表所示。
丁内酯浓度随时间的变化如下表所示。
请填写下列空白:
①在50~80min内,以 丁内酯的浓度变化表示的反应速率为
丁内酯的浓度变化表示的反应速率为_______ 。
在100min时, 羟基丁酸的转化率为
羟基丁酸的转化率为_______ 。
②在25℃时,该反应的平衡常数为K=_______ 。
③为提高平衡时 羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是
羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是_______ 。
(1)氮氧化物(NOx)是一种主要的大气污染物,必须进行处理。
①利用NH3在一定条件下与NO反应生成无污染的气体。其热化学方程式为:4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ΔH=-1807.98kJ·mol-1,下列能表示该反应中能量变化的是
A.
 B.
B. C.
C.
②利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ·mol-1
H2O(l)=H2O(g) ΔH=+44kJ·mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=
(2)由
 )的反应如下:
)的反应如下:
| t/min | 21 | 50 | 80 | 100 | 120 | 160 | 220 | |
| c(mol/L) | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
①在50~80min内,以
在100min时,
②在25℃时,该反应的平衡常数为K=
③为提高平衡时
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网