单选题 较难0.4 引用1 组卷182
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是( )

| A.Na+、Fe2+、NO3-、H+都可在该物质的溶液中大量共存 |
| B.检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色 |
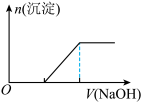
| C.向0.1mol•L-1该物质的溶液中逐滴滴加0.1mol•L-1NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示 |
| D.向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42-完全沉淀的离子方程式为Fe2++2SO42-+2Ba2++2OH-=2BaSO4↓+Fe(OH)2↓ |
2019高三·福建·专题练习
类题推荐
下列有关溶液中离子存在和转化的表达合理的是
| A.向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-=A2-+H2O |
| B.AlCl3溶液加入NaAlO2溶液中:Al3++3AlO |
| C.由水电离出的c(H+)=1×10-12mol/L的溶液中可能大量存在K+、Mg2+、Fe2+、NO |
| D.向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO |
常温下,几种难溶氢氧化物的饱和溶液中金属离子浓度的负对数与溶液的pH关系如下图所示。下列说法正确的是
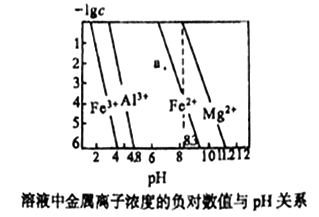
| A.a点代表Fe(OH)2饱和溶液 |
| B.Ksp[Fe(OH)3]< Ksp[Al(OH)3]< Ksp[Fe(OH)2]< Ksp[Mg(OH)2] |
| C.向0.1mol/L Al3+、Mg2+、Fe2+混合溶液中,逐滴滴加稀NaOH溶液,Mg2+最先沉淀 |
| D.在pH=7的溶液中,Fe3+、Al3+、Fe2+能大量共存 |
向一支大试管中加入5mL0.1mol·L-1KI溶液和1mL0.1mol·L-1FeCl3溶液,用力振荡,为证明I-与Fe3+可发生可逆反应,下列实验设计不正确的是( )
| A.取少量反应后的溶液于试管中,滴加淀粉溶液,观察现象 |
| B.取少量反应后溶液于试管中,滴加0.1mol·L-1KSCN溶液,观察现象 |
| C.取少量反应后溶液于试管中,滴加K3[Fe(CN)6]溶液(该溶液与Fe2+反应能产生蓝色沉淀),检验是否有Fe2+生成 |
| D.取少量反应后溶液于试管中,滴加AgNO3溶液,观察现象 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


