解答题-工业流程题 0.65 引用1 组卷85
连二亚硫酸钠(Na2S2O4),有极强的还原性,受热、遇水都会发生分解反应放出大量的热,甚至引起燃烧,不溶于乙醇,可溶于氢氧化钠水溶液并稳定存在。
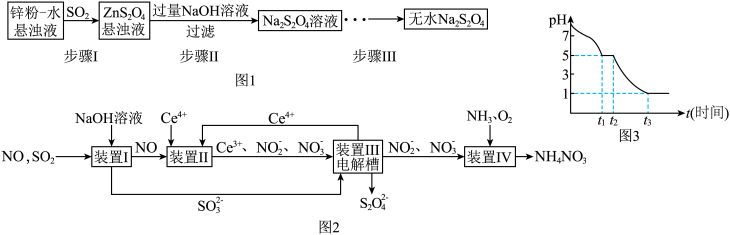
(1)锌粉法是制备Na2S2O4的一种常见方法,其原理如图1所示:
①须将锌粉和水制成悬浊液的原因是______ ;若用Na2SO3固体和某酸反应制备SO2气体,你认为下列最适宜选用的酸是 ______
A.浓盐酸 B.质量分数为70%的H2SO4
C.稀硝酸 D.质量分数为10%的稀硫酸
②步骤III过程较为复杂,其中涉及过滤、洗涤、干燥等操作,请写出洗涤过程的操作方法:______ 。
(2)吸收大气污染物SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如图2(Ce为铈元素):
①装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式______
②装置III中电解槽阴极发生的电极反应为______ 。
③已知进入装置IV的溶液中,NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置IV中通入标准状况下的O2______ L。(用含a代数式表示,计算结果保留整数)
(3)课题小组测定0.050mol•L-1Na2S2O4溶液在空气中pH变化如图3,0-t1段主要生成HSO3-,则0-t1发生离子反应方程式为______ ,t1时刻溶液中离子浓度由大到小的顺序是 ______ ,t3时溶液中主要阴离子符号是 ______ 。

(1)锌粉法是制备Na2S2O4的一种常见方法,其原理如图1所示:
①须将锌粉和水制成悬浊液的原因是
A.浓盐酸 B.质量分数为70%的H2SO4
C.稀硝酸 D.质量分数为10%的稀硫酸
②步骤III过程较为复杂,其中涉及过滤、洗涤、干燥等操作,请写出洗涤过程的操作方法:
(2)吸收大气污染物SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如图2(Ce为铈元素):
①装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式
②装置III中电解槽阴极发生的电极反应为
③已知进入装置IV的溶液中,NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置IV中通入标准状况下的O2
(3)课题小组测定0.050mol•L-1Na2S2O4溶液在空气中pH变化如图3,0-t1段主要生成HSO3-,则0-t1发生离子反应方程式为
2019高三·福建·专题练习


